
【题目】2 mol A与2 mol B混合于2 L的密闭容器中,发生反应:2A(g)+3B(g) ![]() 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是
A.v(C)=0.2 mol·L-1·s-1
B.z=3
C.B的转化率为25%
D.C平衡时的浓度为0.5 mol·L-1
科目:高中化学 来源: 题型:
【题目】SO2(g)+1/2O2(g)![]() SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= -99kJ·mol-1.请回答下列问题:
SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= -99kJ·mol-1.请回答下列问题:
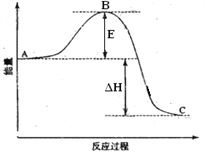
(1)图中可知A、C分别表示______________、_______________;E的大小对该反应的反应热有无影响?___________。
(2)图中△H=______________;
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成5molSO3(g)的△H=______kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第五套人民币中的1元硬币的材质为钢芯镀镍合金。下列关于1元硬币的说法中不正确的是
A. 有一定硬度,耐磨损;但硬度不是很大,否则文字和图案很难压印上去
B. 化学性质稳定,抗腐蚀
C. 每枚硬币实际价值远远高于面值1元
D. 每枚硬币实际价值低于面值1元
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。请回答下列问题:
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知,CH3OH(g)的燃烧热__________(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的汽化热为44 kJ/mol,则表示氢气燃烧热的热化学方程式为__________________________。
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃)该反应为_________反应(填“放热”或“吸热”);在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,pH = 9的NaHA溶液中各微粒的物质的量浓度关系正确的是
A.c(A2-)>c(H2A) B.c(Na+)+c(H+) =c(OH-)+c(HA-)+2c(A2-)
C.c(Na+) =c( HA-) +c(H2A) D.c(H+) =c(A2-) +c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO等有害气体。

(1)汽车尾气中NO生成过程的能量变化示意图如图。该条件下,1molN2和1molO2完全反应生成NO会_______________(填“吸收”或“放出”)___________kJ能量。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
①NiO电极上发生的是___________反应(填“氧化”或“还原”)。
②外电路中,电子流动方向是从_________电极流向_______电极(填“NiO”或“Pt”).
③Pt电极上的电极反应式为_______________________________。
(3)一种新型催化剂能使NO和CO发生反应:2NO+2CO![]() 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
实验编号 | t(℃) | NO初始浓度 | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.2×10﹣3 | 5.80×10﹣3 | 82 |
Ⅱ | 280 | 1.2×10﹣3 | b | 124 |
Ⅲ | 350 | a | 5.80×10﹣3 | 82 |
①请表中数据补充完整:a___________;b____________。
②能验证温度对化学反应速率规律的是实验____________________(填实验序号)。
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线________________(填“甲”或“乙”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00 mL 0.1000 mol·L-1 CH3COONa 溶液中逐滴加入 0.100 0 mol L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是
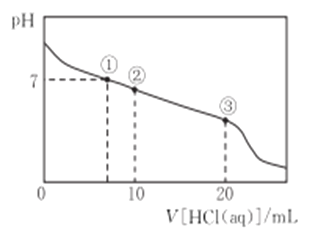
A. CH3COONa溶液中:c(H+) +c(CH3COOH)=c(OH-)+c(Na+)
B. 点①所示溶液中:c(CH3COOH) =c(Cl-)>c(OH-)=c(H+)
C. 点②所示溶液中:c(Cl-)>c(CH3COO-)>c(CH3COOH)>c(H+) >c(OH-)
D. 点③所示溶液中:c(Na+)= c(Cl-)>c(CH3COOH) >c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
A. 容器内的总压强不随时间变化
B. 断裂4molH—O键的同时,断裂4molH—H键
C. 混合气体的平均相对分子质量不变
D. 反应不再进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com