
【题目】如图是一种航天器能量储存系统原理示意图。下列说法正确的是
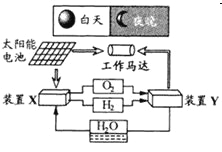
A. 该系统中只存在3种形式的能量转化
B. 装置Y中负极的电极反应式为:![]()
C. 装置X能实现燃料电池的燃料和氧化剂再生
D. 装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
【答案】C
【解析】
装置X和Y实际上是存储了部分太阳能电池产生的电能,太阳能电池利用光能转化为电能可直接用于工作;马达实现了电能与机械能的转化;在装置X中,电解水生成H2、O2,实现了电能与化学能的转化;在装置Y中构成燃料电池,化学能转化为电能,作用于马达实现了电能与机械能的转化,氢氧燃料电池的负极上应是H2参加反应,装置X能利用光能实现H2、O2、H2O的循环再生,据此回答。
A.存在能量转化形式有太阳能、机械能、化学能、电能,则不只是三种,故A错误;
B.装置Y为燃料电池,氢气在负极失电子被氧化,电极反应式是:H2-2e-+2OH-=2H2O,故B错误;
C.在装置X中,电解水生成H2、O2,能实现燃料电池的燃料和氧化剂再生,故C正确;
D.在反应过程中,有能量的损耗和热效应的产生,不可能实现化学能和电能的完全转化,故D错误。
答案选 C。


 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中的浓硫酸滴入②中,预测的现象与结论相符的是( )
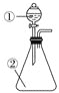
A. 若②为浓盐酸;产生大量气体产生;说明硫酸的酸性比盐酸强
B. 若②为铜片;有气泡产生,底部生成灰白色固体;说明浓硫酸有强氧化性
C. 若②为蓝色硫酸铜晶体;蓝色晶体变为白色;说明浓硫酸有吸水性,发生物理变化
D. 若②为蔗糖;白色固体变为黑色海绵状,有气体放出;说明浓硫酸有脱水性、氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组针对原电池形成条件,设计了实验方案,进行如下探究。
(1)请填写有关实验现象并得出相关结论。
编号 | 实验装置 | 实验现象 |
1 |
| 锌棒逐渐溶解,表面有气体生成;铜棒表面无现象 |
2 |
| 两锌棒逐渐溶解,表面均有气体生成;电流计指针不偏转 |
3 |
| 铜棒表面的现象是______________________,电流计指针___________________ |
①通过实验2和3,可得出原电池的形成条件是______________________________。
②通过实验1和3,可得出原电池的形成条件是______________________________。
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,从而可得出原电池形成条件是___________________。
(2)分别写出实验3中Zn棒和Cu棒上发生的电极反应式:
Zn棒:______________________________。
Cu棒:______________________________。
(3)实验3的电流是从________棒流出(填“Zn”或“Cu”),反应过程中若有0.4mol电子发生了转移,则Zn电极质量减轻___________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )


A. 图①中ΔH1=ΔH2+ΔH3
B. 图②在催化剂条件下,反应的活化能等于E1+E2
C. 图③表示醋酸溶液滴定 NaOH溶液和氨水混合溶液的电导率变化曲线
D. 图④可表示由CO(g)生成CO2(g)的过程中要放出566 kJ 热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某电池的工作原理如图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是( )
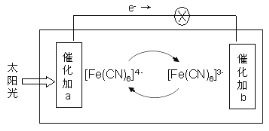
A.K+移向催化剂b
B.催化剂a表面发生的化学反应:[Fe(CN)6]4- - e- = [Fe(CN)6]3-
C.[Fe(CN)6]3-在催化剂b表面被氧化
D.电解质溶液中的[Fe(CN6)]4-和[Fe(CN6)]3-浓度基本保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸分别与三种钠盐反应,现象如图。下列分析正确的是( )
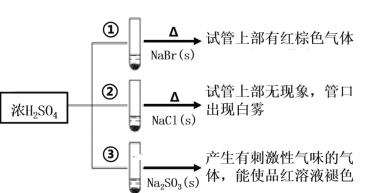
A.②中试管口白雾是HCl遇水蒸气所致,说明酸性:H2SO4>HCl
B.①和③相比可说明氧化性:Br2>SO2
C.对比①和②可以说明还原性:Br->Cl-
D.③中浓H2SO4被还原成SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)图为氢氧燃料电池原理示意图,按照此图的提示,回答以下问题:
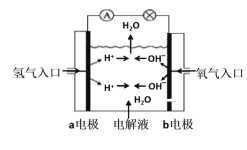
①下列叙述不正确的是___。
A.a电极是负极
B.b电极的电极反应为:4OH--4e-=2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
②若电解质溶液为KOH溶液,则电极反应式为:a极__,b极___。
(2)以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。回答下列问题:
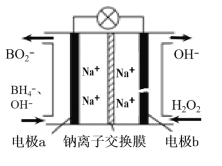
①电池放电时Na+移动方向是:__(填“从左向右”或“从右向左”)。
②电极b采用MnO2,MnO2的作用是__。
③该电池的负极反应为:__。
④每消耗3molH2O2,转移的电子数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图。(X、Y、Z、M、N、P为代号,不为元素符号)则下列说法正确的是( )
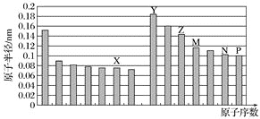
A.Z、N两种元素的离子半径相比,前者较大
B.N、P两种元素的气态氢化物的稳定性相比,前者较稳定
C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z的氧化物能分别溶解于Y的氢氧化物和P的氢化物的水溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2O4(g)![]() 2NO2(g),将装有N2O4和NO2混合气体的烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论不能说明该反应已经达到化学平衡状态的是
2NO2(g),将装有N2O4和NO2混合气体的烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论不能说明该反应已经达到化学平衡状态的是
A. 烧瓶内气体的质量不再变化
B. 烧瓶内气体的颜色不再变化
C. 烧瓶内气体的压强不再变化
D. N2O4的消耗速率与NO2的消耗速率之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com