
| A、稀硫酸与氢氧化钡溶液反应Ba2++SO42-=BaSO4↓ |
| B、铝与氢氧溶液化钠反应Al+2OH-=AlO2-+H2↑ |
| C、向Na2CO3浓溶液中缓慢滴加几滴稀盐酸CO32-+H+=HCO3- |
| D、锌粒与稀醋酸反应Zn+2H+=Zn2++H2↑ |


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、OH-、Ba2+、HCO3-、Cl- |
| B、K+、Fe2+、H+、NO3- |
| C、NH4+、Al3+、Cl-、NO3- |
| D、Mg2+、SO42-、SiO32-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 第45届世界体操锦标赛于2014年10月3日至12日在广西体育中心体育馆举行.
第45届世界体操锦标赛于2014年10月3日至12日在广西体育中心体育馆举行.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨气通入醋酸溶液中 CH3COOH+NH3═CH3COONH4 |
| B、澄清的石灰水跟盐酸反应 H++OH-═H2O |
| C、碳酸钡溶于醋酸 BaCO3+2H+═Ba2++H2O+CO2↑ |
| D、金属钠跟水反应 2Na+2H2O═2Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
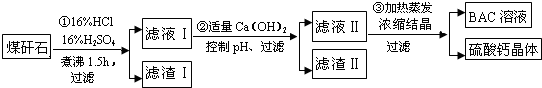
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com