
【题目】Ⅰ.现有下列十种物质:①O2;②Fe;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁胶体;⑧硫酸钠溶液;⑨稀硝酸;⑩Cu2(OH)2CO3。
(1)按物质的树状分类法填写表格的空白处:
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 |
属于该类的物质 | ② | _____ | ⑧⑨ | _____ |
(2)上述物质中属于非电解质的有_________;上述物质中能与盐酸反应的电解质有________。
Ⅱ.(1)在 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O 的反应中,氧化剂是_________,还原产物是_________,氧化产物与还原产物的质量比是_________。
(2)在反应MnO2+4HCl=MnCl2+Cl2↑+2H2O中,每生成标准状况下4.48LCl2,转移电子的数目为___________。
Ⅲ.Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程,据此回答下列问题:
将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+ _________+ ________![]() _________+ ________+H2O
_________+ ________+H2O
【答案】 ③④: ⑦ ④ ③⑥⑩ KClO3 Cl2 5:1 0.4NA Mn2++BiO3-+H+![]() MnO4-+Bi3++H2O
MnO4-+Bi3++H2O
【解析】试题分析:(1)根据物质的元素组成,可以将物质分为纯净物和混合物,纯净物中,根据组成元素的种类可以将物质分为单质和化合物,只有一种元素组成的纯净物是单质,如氧气、铁,根据化合物的性质,可以将化合物分为酸、碱、盐、氧化物,如氧化钙、二氧化碳属于氧化物,根据混合物分散质微粒直径的大小,可以将混合物分为溶液(如硫酸钠溶液、稀硝酸)浊液和胶体(如红褐色的氢氧化铁液体)三种,化合物在水溶液或是熔融态下是否导电,可以将化合物分为电解质和非电解质,如CaO、H2SO4、Ba(OH)2、Cu2(OH)2CO3属于电解质,故答案为:
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 |
属于该类的物质 | ② | ③④ | ⑧⑨ | ⑦ |
(2)在水溶液中和熔融状态下均不能导电的化合物是非电解质,非电解质包括蔗糖、酒精、非金属氧化物、NH3等,故为非电解质的是④; 电解质是在水溶液中或熔融状态下均不能导电的化合物,故是电解质的是③⑤⑥⑩,其中能和盐酸反应的是③⑥⑩,故答案为:④;③⑥⑩;
Ⅱ.(1)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,KClO3为氧化剂,HCl为还原剂,当有3mol Cl2生成时,转移5mol电子,当有1mol Cl2生成时,氧化产物与还原产物的质量之比为5/3mol:1/3mol=5:1;
(2)标准状况下的Cl24.48L,n(Cl2)=4.48L÷22.4L/mol=0.2mol,
转移的电子为0.2mol×2×[0-(-1)]=0.4mol;
Ⅲ.发生BiO3---Bi3+的反应,Bi元素由+5价降低为+3价,则还发生Mn2+→MnO4-,Mn元素由+2升高为+7,发生Mn2++BiO3-+H+→MnO4-+Bi3++H2O,由电子守恒及质量守恒定律可知,该反应为2Mn2++5BiO3-+14H+═2MnO4-+5Bi3++7H2O。


科目:高中化学 来源: 题型:
【题目】同温同压,甲容器中CO2气体与乙容器中CO气体所含的原子总数相等,则甲乙两容器的体积比为( )
A.1:2 B.2:1 C.3:2 D.2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

某学生实验需要450mL 0.2mol/L的稀H2SO4,实验员老师准备取用这批硫酸来配制。
可供选用的仪器有:a.胶头滴管;b.烧瓶;c.烧杯;d.药匙; e.量筒;f.托盘天平。
请回答下列问题:
(1)该校所购买的这批硫酸的物质的量浓度为 ;
⑵需要用量筒量取上述浓硫酸的体积为 mL,量取浓硫酸时应选用(填序号) 规格的量筒。
a.10 mL b.50 mL c.100 mL
⑶上述仪器中不需要使用的有(选填序号) ,还缺少的仪器有(写仪器名称) 。
⑷若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①硫酸溶解后未冷至室温即进行定容 ;②定容时俯视刻度线 ;
⑸定容时液面高于刻度线应采取的措施是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成分为Fe(CrO2)2]为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:

己知:铬铁矿在空气中与纯减煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,
且 Al2O3+Na2CO3![]() 2NaAlO2+ CO2↑。请回答:
2NaAlO2+ CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为___________。
(2)滤渣2的成分为_____________。
(3)将滤渣1放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是_________。
(4)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol/L以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①沉淀法:
加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于________________mol/L,后续废水处理方能达到国家排放标准。
②还原法:CrO42-![]() Cr3+
Cr3+![]() Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
(5)某高效净水剂是由K2FeO4得到的,工业上以溶液w、次氯酸钾和氢氧化钾为原料制备K2FeO4,该反应的离子方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属元素R其质量数为127,又知R离子含有74个中子,54个电子,则该元素最高化合价组成的化合物是( )
A.R(OH)3
B.R2O7
C.HRO3
D.H2R
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15 mL 2 mol·L1 Na2CO3溶液逐滴加入到40 mL 0.5 mol·L1 MCln盐溶液中,恰好将溶液中的Mn+ 完全沉淀为碳酸盐,则MCln中n值是
A. 4 B. 3 C. 2 D. 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃分子结构中含一个苯环、两个碳碳双键和一个碳碳三键,则它的分子式可能为
A. C9H12 B. C17H20 C. C20H30 D. C12H20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图是课外活动小组的同学设计的 4 个喷泉实验方案。下列有关操作不可能引发喷泉现象的是( )
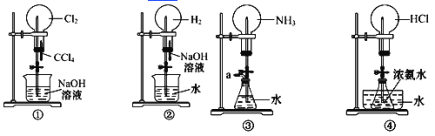
A.挤压装置①的胶头滴管使 CCl4。全部进入烧瓶,片刻后打开止水夹
B.挤压装置②的胶头滴管使 NaOH 溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的 a 处不断鼓入空气并打开止水夹
D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向一个容积不变的容器中,通入2mol SO2和2mol O2及固体催化剂,使之反应。2SO2(g)+O2(g)![]() 2SO3(g);ΔH=-196 KJ/mol。平衡时容器内气体压强为起始时的90%。此时
2SO3(g);ΔH=-196 KJ/mol。平衡时容器内气体压强为起始时的90%。此时
(1)加入2mol SO2和2mol O2发生反应,达到平衡时,放出的热量为 ;
(2)保持同一反应温度,在相同的容器中,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g),欲使平衡时SO3的体积分数为2/9,
①达到平衡时,⑴与⑵放出的热量 (填序号)。
A.一定相等 B.前者一定小 C.前者大于或等于后者
②a、b、c必须满足的关系是 、 (一个用a、c表示,另一个用b、c表示),
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com