
【题目】拆开1 mol共价键所吸收的能量或形成1 mol共价键所释放的能量称为键能。已知:H—H键能为436 kJ/mol,H—N键能为391 kJ/mol,N2 (g)+ 3H2(g) ![]() 2NH3(g) ΔH=92.4 kJ/mol,下列说法中正确的是( )
2NH3(g) ΔH=92.4 kJ/mol,下列说法中正确的是( )
A.H—H比N≡N更牢固
B.N≡N键能约为945.6 kJ/mol
C.合成氨反应选择适当的催化剂是为了提高H2的转化率
D.0.5 mol N2和1.5 mol H2在题给条件下充分反应,放出热量为46.2 kJ
【答案】B
【解析】
A、△H=反应物的键能和-生成物的键能和,-92.4KJ/mol=Q(N≡N)+3×436KJ/mol-6×391KJ/mol,Q(N≡N)=946KJ/mol,大于H-H键的键能,所以,N≡N键牢固,故A错误;
B、△H=反应物的键能和-生成物的键能和,-92.4KJ/mol=Q(N≡N)+3×436KJ/mol-6×391KJ/mol,Q(N≡N)=946KJ/mol,故B正确;
C、催化剂只能加快化学反应速率,不影响化学平衡的移动,不能提高H2的转化率,故C错误;
D、合成氨是可逆反应,反应物不能完全转化,所以0.5mol N2和1.5mol H2在题给条件下充分反应,放出热量小于46.2 kJ,故D错误.
故选:B


科目:高中化学 来源: 题型:
【题目】碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间的转化关系如图所示。已知:淀粉遇单质碘变蓝。下列说法中,不正确的是( )

A.氧化性的强弱顺序为:Cl2 >IO3-- >I2
B.一定条件下, I--与IO3--反应可能生成I2
C.向含I--的溶液中通入Cl2,所得溶液加入淀粉溶液一定变蓝
D.途径Ⅱ中若生成1mol I2,消耗5mol NaHSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油资源紧张曾是制约中国发展轿车事业,尤其是制约轿车进入家庭的重要因素。据报道,中国宣布将推广“车用乙醇汽油”。
(1)乙醇燃烧时如果氧气不足,可能还有CO生成.用下图装置正确验证乙醇燃烧产物有CO、![]() 、
、![]() ,应将乙醇燃烧产物依次通过,按气流从左至右顺序填装置编号______。
,应将乙醇燃烧产物依次通过,按气流从左至右顺序填装置编号______。
编号 | ① | ② | ③ | ④ |
装置 |
|
|
|
|
(2)实验时可观察到装置②中A瓶的石灰水变浑浊。A瓶溶液的作用是______;B瓶溶液的作用是______。
(3)装置①中所盛的是______溶液,证明燃烧产物中含有CO的实验现象是:______。
(4)装置④中所盛的固体药品是______,它可以验证的产物是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将A和B各0.32 mol充入10 L的恒容密闭容器中,发生如下反应:A(s)+B(g)![]() 2C(g) △H<0,反应过程中测定的数据如表,则下列说法正确的是
2C(g) △H<0,反应过程中测定的数据如表,则下列说法正确的是
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A.反应前2 min的平均反应速率v(C)=0.004 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前,v(逆)>v(正)
C.其他条件不变,起始时向容器中充入各0.64 mol的A和B,平衡时n(C)<0.48 mol
D.其他条件不变,向平衡体系中再充入0.32 mol B和0.16 mol C,再达到平衡时,A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
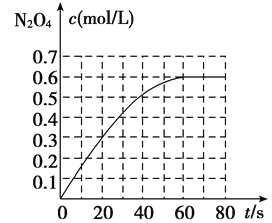
【题目】298 K时,在2 L固定体积的密闭容器中,发生可逆反应:2NO2(g) ![]() N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
A. v(正)>v(逆)
B. v(正)<v(逆)
C. v(正)=v(逆)
D. v(正)、v(逆)大小关系不确定
查看答案和解析>>
科目:高中化学 来源: 题型:
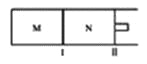
【题目】如图所示,隔板I固定不动,活塞II可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)![]() xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )
xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )
A. 若x=3,达到平衡后A的体积分数关系为:![]()
B. 若x<3,C的平衡浓度关系为:c(M)<c(N)
C. 若x>3,达到平衡后B的转化率关系为:![]()
D. x不论为何值,平衡时M、N中的平均相对分子质量都相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:C(s)+H2O(g)![]() CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
容器 | 甲 | 乙 | 丙 |
|
容积/L | 1 | 1 | V | |
温度/℃ | T1 | T2 | T1 | |
起始量 | 2 molC(s)、2 mol H2O(g) | 2 mol CO(g)、2 mol H2(g) | 6 molC(s)、 4mol H2O(g) |
下列说法正确的是( )
A.甲容器中,0~5min内的平均反应速率v(CO)=0.1 mol/(L·min)
B.乙容器中,若平衡时n(C)=0.56 mol,则T2>T1
C.温度为T1时,反应的平衡常数为K=9
D.丙容器的容积V=0.8 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。
 ,下列说法正确的是( )
,下列说法正确的是( )
A. NaOH溶液可以用氨水来代替
B. 溶液a中含有Al3+、K+、Cl-、Na+、OH-
C. 溶液b中只含有NaCl
D. 向溶液a中滴加盐酸需控制溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子数目的对应关系,完全正确的是( )
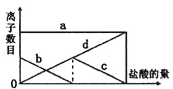
A. a:K+; b:HCO3—;c:CO32—;d:Cl—
B. a:K+; b:CO32—;c:HCO3—;d:Cl—
C. a:K+; b:CO32—;c:Cl—;d:HCO3—
D. a:K+; b:HCO3—;c:Cl—;d:CO32—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com