
【题目】在容积不变的密闭容器中进行反应:X2(g)+3Y2(g) ![]() 2Z2(g),若X2、Y2、Z2的初始物质的量浓度分别为0.10mol·L-1、0.30mol·L-1、0.20mol·L-1,当反应达到平衡时Z2的物质的量浓度不可能是
2Z2(g),若X2、Y2、Z2的初始物质的量浓度分别为0.10mol·L-1、0.30mol·L-1、0.20mol·L-1,当反应达到平衡时Z2的物质的量浓度不可能是
A. 0.05mol·L-1 B. 0.20mol·L-1 C. 0.35mol·L-1 D. 0.40mol·L-1
【答案】D
【解析】
由于该反应是可逆反应,则达到平衡时反应物或生成物的浓度不可能是0。
A.当反应达到平衡时Z2的物质的量浓度为0.05mol·L-1时,则消耗Z2,反应向逆向移动,此时c(X2)=0.175 mol·L-1,c(Y2)=0.525 mol·L-1,均不为0,故A可能;
B.当反应达到平衡Z2的物质的量浓度为0.20mol·L-1时,c(X2)=0.10mol·L-1,c(Y2)= 0.30mol·L-1,均不为0,故B可能;
C.当反应达到平衡Z2的物质的量浓度为0.35mol·L-1时,则反应向正向移动,此时c(X2)=0.025 mol·L-1,c(Y2)=0.075 mol·L-1,均不为0,故C可能;
D. 当反应达到平衡Z2的物质的量浓度为0.40mol·L-1时,反应向正向进行,此时c(X2)=0,c(Y2)=0,故D不可能;
本题答案为D。


科目:高中化学 来源: 题型:
【题目】下列有关离子反应的说法正确的是( )
选项 | 离子方程式 | 评价 |
A | 将2molCl2通入到含1mol FeI2的溶液中:2Fe2++2I-+2Cl2= 2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ | 正确;阳极氯离子放电,阴极氢离子放电 |
C | 向AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O=A1O2一 + 4NH4++ 2H2O | 正确;氨水过量,氢氧化铝能溶于过量的碱 |
D | 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O | 错误;电荷不守恒,生成物中应有亚铁离子 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不符合节能减排要求的是( )
A.将煤块粉碎提高燃料的燃烧效率
B.在汽车上安装汽车尾气催化转化装置,可使汽车尾气中的![]() 和
和![]() 发生反应:
发生反应:![]()
C.在大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃料电池汽车
D.在水力发电、火力发电、核能发电和风力发电中,要大力发展火力发电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定温度下,有下列反应发生:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g),该反应的平衡常数表达式K=________。
(2)在配制FeCl3溶液时,加入少许浓盐酸,其目的是:_____________;不断加热FeCl3溶液,蒸干其水分并灼烧固体,最后得到的物质是________。
(3)已知:Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+![]() O2(g)===Fe2O3(s)的ΔH是____________________。
O2(g)===Fe2O3(s)的ΔH是____________________。
(4)Fe(OH)2在空气中短时间内可被氧化为Fe(OH)3,发生的反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,下列说法中错误的是________(填字母)。
A.该反应是能自发进行的反应
B.该反应是熵增加的反应
C.该反应是化合反应
D.该反应是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有些汽车安装了安全气囊,气囊中装有叠氮化钠(![]() )等固体粉末。一旦汽车发生强烈的撞击,叠氮化钠将迅速分解生成钠和氮气(
)等固体粉末。一旦汽车发生强烈的撞击,叠氮化钠将迅速分解生成钠和氮气(![]() ),使安全气囊打开,起到保护作用。此后气体通过气囊上的小孔迅速消散,气囊收缩。
),使安全气囊打开,起到保护作用。此后气体通过气囊上的小孔迅速消散,气囊收缩。
(1)写出叠氮化钠发生分解反应的化学方程式:____________________。
(2)写出安全气囊中选用叠氮化钠的理由:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种将CO2和H2O转换为燃料H2、CO及CH4的装置如图所示(电解质溶液为稀H2SO4)。下列关于该装置的叙述错误的是

A. 该装置可将电能转化为化学能
B. 工作时,电极a周围溶液的pH增大
C. 电极b上生成CH4的电极反应式为CO2+8H++8e-===CH4+2H2O
D. 若电极b上只产生1 mol CO,则通过质子膜的H+数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关NA的叙述正确的是( )
A.将22.4LCl2通入水中,HClO、Cl-、ClO-的粒子数之和为2NA
B.1molAlCl3在熔融状态时含有的离子总数为4NA
C.1molNa2O2与足量CO2充分反应后转移电子数为2NA
D.一定条件下,28g的乙烯和环己烷混合气体中所含原子总数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列说法正确的是
A.某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=a+1
B.在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好无色,则此时溶液pH<7
C.NH4Cl溶液的Kw大于NaCl溶液的Kw
D.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中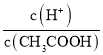 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下浓度均为0.1mol/L 的四种盐溶液,其pH 如表所示,下列说法正确的是( )
序号 | ① | ② | ③ | ④ |
溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
pH | 8.8 | 9.7 | 11.6 | 10.3 |
A. 将等浓度的CH3COOH 和HClO溶液,pH小的是HClO
B. Na2CO3和NaHCO3溶液中粒子种类不同
C. 溶液水的电离程度:①>②>④>③
D. NaHCO3溶液中:c (Na+) =c (CO32- )+c (HCO3- )+c (H2CO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com