
【题目】实验室要用NaCl固体配制100mL 2.0mol·L-1的NaCl溶液,试回答下列各题:
(1)下列仪器中,不会用到的是 _____________。
A.锥形瓶 B.100mL容量瓶 C.量筒 D.胶头滴管 E.50mL容量瓶 F.天平
(2)若要实施配制,除上述仪器外,尚缺的仪器或用品是___________________。
(3)容量瓶在使用前必须____________________________________。
(4)人们常将配制过程简述为以下各步骤:
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移
其正确的操作顺序应是_____________________________(填各步骤序号)。
(5)配制完毕后,教师指出有四位同学各进行了下列某一项错误操作,你认为这四项错误操作会导致所得溶液浓度偏高的是 (_________)
A.称量 NaCl固体时“左码右物”
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(6)通过计算可得出可用托盘天平称取NaCl固体质量是______________。若用5.0mol/L的NaCl溶液配制应用量筒量取________________mL该溶液。
【答案】ACE 烧杯、玻璃棒 检查是否漏液 BEAGCDF B 11.7克 40.0
【解析】
实验室配制100mL 2.0mol·L-1的NaCl溶液,需要的NaCl固体的质量为m=cVM=2.0mol·L-1×58.5g/mol×0.1L=11.7g;
用托盘天平称量11.7g氯化钠固体,将其放在烧杯中溶解,将冷却后的溶液沿玻璃棒引流入100mL容量瓶中,用蒸馏水洗涤烧杯和玻璃棒2-3次,将洗涤液也注入容量瓶中,向容量瓶中加水直至距刻度线1-2cm处,改用胶头滴管向容量瓶中加水直至凹液面最低点与刻度线相切,盖上瓶塞倒转摇匀,据此回答问题。
(1)由分析可知,不会用到的仪器是锥形瓶、量筒、50mL容量瓶,答案选ACE;
(2)要实施配制,除100mL容量瓶、胶头滴管外,还需要用到烧杯和玻璃棒;
(3)容量瓶在使用前必须检查容量瓶是否漏液;
(4)由分析可知,正确的操作顺序应是BEAGCDF
(5)A.称量 NaCl固体时“左码右物”,会使称得的质量偏低,导致浓度偏低,A项错误;
B.定容时俯视容量瓶刻度线,溶液体积偏小,导致浓度偏大,B项正确;
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作,没有进行洗涤的操作,使浓度偏低,C项错误;
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,增大了溶剂的量,稀释了溶液,使浓度降低,D项错误;
答案选B;
(6)由分析可知,用托盘天平称取NaCl固体质量是m=cVM=2.0mol·L-1×58.5g/mol×0.1L=11.7g;用5.0mol/L的NaCl溶液配制,利用稀释定律可计算出需要的溶液的体积V=![]() =
=![]() =0.4L,即用量筒量取40.0mL该溶液。
=0.4L,即用量筒量取40.0mL该溶液。


科目:高中化学 来源: 题型:
【题目】室温下,用0.1 mol·Lˉ1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol·Lˉ1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图,下列说法不正确的是( )

A. HX为弱酸
B. M点c(HX)—c(X-)﹥c(OH-)—c(H+)
C. 将P点和N点的溶液混合,呈酸性
D. 向N点的溶液中通入HCl至pH=7:c(Na+) ﹥c(HX)=c(Cl-) >c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无论是干重还是鲜重,组成水生动物、人体细胞的元素中含量最多的四种元素是
A.O、N、H、CaB.O、Ca、P、Mg
C.C、O、N、HD.C、Fe、Ca、P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表中评价合理的是( )
选项 | 化学反应及其离子方程式 | 评价 |
A | NaHSO4溶液与Ba(OH)2溶液反应至SO42-沉淀完全:2H++ SO42-+Ba2++2OH==BaSO4↓+2H2O | 正确 |
B | 向碳酸镁浊液中加入足量稀盐酸:CO32- +2H+ | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O==Fe(OH)3↓+3H+ | 正确 |
D | 碳酸氢钠与足量澄清石灰水反应:2HCO3-+Ca2++2OH-==CaCO3↓+CO32-+2H2O | 正确 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成。其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子。下列说法错误的是( )
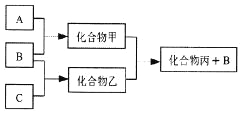
A. Z元素位于第二周期第VIA族
B. 可用排水法收集化合物乙
C. 元素X、Y、Z的原子半径大小关系为X<Z<Y
D. 化合物甲溶于化合物丙中,存在的微粒有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨水、胆矾都是中学实验室中常见的化学试剂,它们在工农业生产上也都有广泛应用。某研究性学习小组为测定氨水的浓度,并用氨水作为提纯胆矾时的试剂,根据所查阅资料设计实验如下:
查阅资料:
①甲基橙的变色范围:pH<3.1红色,pH=3.1~4.4橙色, pH>4.4黄色
②酚酞的变色范围:pH<8.2无色 ,pH=8.2~10.0粉红色,pH>10.0红色
③已知:Fe3+、Fe2+、Cu2+转化为氢氧化物时相应的pH如下表:
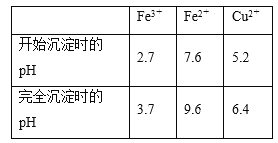
实验一 标定氨水的浓度
取25.00mL约为0.10 mol·L-1氨水于锥形瓶中,用0.1000 mol·L-1盐酸进行滴定,实验所得数据如下表所示:
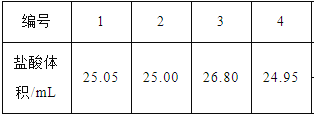
(1)滴定产物水解的离子方程式为____________________________________,由此可推知选择的滴定指示剂应为__________________。(填“甲基橙”或“酚酞”)
(2)该氨水的准确浓度为____________________mol·L-1。(精确到小数点后四位)
(3)编号3中溶液的离子浓度由大到小的顺序为__________________________________。
实验二 提纯胆矾晶体
某学习小组同学拟从含FeSO4、Fe2(SO4)3杂质的CuSO4溶液中提纯胆矾,其主要实验步骤如下:
第一步 往混合液中加入3% H2O2溶液充分反应后,再加入稀氨水调节溶液pH,过滤。
第二步 往滤液中加入稀硫酸调节溶液pH至1~2,提纯胆矾。
(4)加入3% H2O2溶液的作用是___________________________。
(5)加稀氨水调节pH应调至范围___________________________。
(6)下列物质可用来替代稀氨水的是___________________________。(填序号)
A.NaOH B.Cu(OH)2 C.CuO D.NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示装置和对应实验原理的描述均正确的是
A | B | C | D |
|
|
|
|
根据温度计读数的变化测定浓硫酸和NaOH溶液反应的反应热 | 加热固体NaHCO3制备少量的Na2CO3 | 验证牺牲阳极的阴极保护法,可证明铁被保护 | 根据小试管中液面的变化可判断铁钉发生了析氢腐蚀 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1mol/LNaOH溶液分别滴定体积均为20mL,浓度均为0.1mol/LHCl溶液和HX溶液,溶液的pH随加入的NaOH溶液体积变化如图。下列说法正确的是
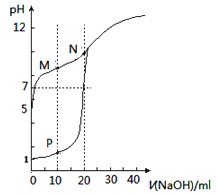
A. M点c(HX)-c(X-)>c(OH-)-c(H+)
B. N点的pH>7的原因是由于NaOH过量所致
C. HX为弱酸,且电离平衡常数Ka≈1×10-10
D. P点c(Cl-)=0.05mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mX(g)![]() nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示,下列说法错误的是( )
nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示,下列说法错误的是( )
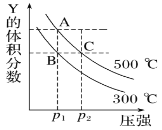
A. 该反应的ΔH>0
B. m<n+p
C. B、C两点化学平衡常数:KB>KC
D. A、C两点的反应速率v(A)<v(C)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com