
【题目】A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)D在元素周期表中的位置是___________________________。
(2)C2B的电子式是__________________。
(3)B、C、E的离子半径由大到小的顺序为__________________(用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为_________________。
(4)B的气态氢化物与H2S相比沸点高的是_________(用化学式回答);原因是___________。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式:_____________。
【答案】第三周期第IVA族 ![]() Cl->O2->Na+ HClO4>H2CO3>H2SiO3 H2O 水分子间形成氢键,可以使水沸点升高 2ClO2+5Mn2++6H2O=5MnO2↓+2Cl-+12H+
Cl->O2->Na+ HClO4>H2CO3>H2SiO3 H2O 水分子间形成氢键,可以使水沸点升高 2ClO2+5Mn2++6H2O=5MnO2↓+2Cl-+12H+
【解析】
A、B、C、D、E均是短周期元素,其原子序数依次增大,A原子最外层电子数是内层电子数的二倍,则A为碳元素,A和D同族,则D为硅元素,A和B同周期,B元素族序数是周期数的三倍,则B为氧元素,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,则C为钠元素,E是所在周期中原子半径最小的元素,则E为氯元素,据此解答。
根据以上分析可知A、B、C、D、E分别是C、O、Na、Si、Cl。则
(1)D为硅元素,在元素周期表中位于第三周期第ⅣA族;
(2)C2B为氧化钠,它的电子式是![]() ;
;
(3)电子层数越多,离子半径越大,电子层数相同时,核电荷数越多,离子半径越小,所以B、C、E离子半径的由大到小的顺序为r(Cl-)>r(O2-)>r(Na+);元素的非金属性越强,最高价氧化物对应水化物的酸性就越强,非金属性Cl>C>Si,所以酸性HClO4>H2CO3>H2SiO3;
(4)由于水分子之间有氢键且是极性分子,所以水的沸点高于H2S;
(5)用ClO2可氧化Mn2+,生成黑色沉淀MnO2,当消耗13.50g(即0.2mol)ClO2时,共转移了1mol电子,这说明氯元素化合价从+4价降低到-1价,根据电子得失守恒可写出反应的离子方程式为5Mn2++2ClO2+6H2O=Cl-+5MnO2↓+12H+。


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在NaCl、MgCl2和MgSO4三种盐配成的混合溶液中,若Na+的浓度为0.1 mol/L,Mg2+的浓度为0.25 mol/L,Cl-的浓度为0.2 mol/L, 则SO42-的物质的量浓度为( )
A.0.5 mol/LB.0.2 mol/L
C.0.45 mol/LD.0.25 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是造成大气污染的主要有害气体之一,二氧化硫尾气处理的方法之一是采用钠一钙联合处理法。
第一步:用NaOH溶液吸收SO2。2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+H2O=CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是_______(用元素符号填写)。
(2)氧和硫属于同族元素,写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:_______________________________________。
(3)NaOH的电子式为______________ 。
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式______________。
(5)钠一钙联合处理法的优点有________________。(任写一点即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知氨基酸可发生如下反应:
![]()
D、E的相对分子质量分别为162和144,可发生如下物质转化关系。如下图所示:

(1)写出B、D的结构简式:B________,D_________。
(2)写出C→E的化学方程式:_________________。
(3)写出C→D的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:_____与盐酸反应最剧烈;______与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______________________________________________________。
(3)写出次氯酸的电子式____________。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律
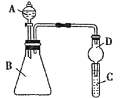
(1)仪器D的作用为_________________________________________。
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,C中加淀粉碘化钾混合溶液,观察到C中溶液_______(填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,用离子方程式表示该尾气吸收原理______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法中,正确的是
①Si可用来制造半导体材料 ②SiO2可用于制造光导纤维 ③Al(OH)3可用于治疗胃酸过多 ④氧化铁可用于制红色涂料
A.只有①B.只有②C.只有③D.都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.汽油车在行驶过程中,热能首先转化为化学能,化学能再转化为动能
B.炸药发生爆炸时化学能完全转化为热能
C.炭燃烧时化学能主要转化为光能
D.柴草燃烧时,部分化学能转化为热能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com