
【题目】(I)现有A、B两种有机物的液体混合物,如果A、B互溶,且互相不发生化学反应。在常压下,A的沸点为35℃,B的沸点为200℃。分离A、B的混合物的常用方法是:________,需要的玻璃仪器除酒精灯、温度计外有_______、________、________、________。
(II)某课外小组需要配制95mL浓度为1 mol/L的NaCl溶液
(1)需要称取NaCl固体的质量为________g。
(2)在配制1 mol/L的NaCl溶液过程中,下列情况对氯化钠溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“无影响”)。
①未经冷却趁热将溶液注入容量瓶中________;
②定容后有少量NaCl溶液洒出________;
③定容时仰视观察液面________。
(3)若预将100 mL 12mol/L的盐酸稀释为6mol/L的盐酸,需要加入水的体积为________mL。(已知:12mol/L的盐酸密度为1.19g/mL,6mol/L的盐酸密度为1.1g/mL,水的密度为1.0g/mL)。
(III)过氧化钠可用于呼吸面具中作为氧气的来源,在此过程中主要发生的化学反应方程式为_______________________;当氧气生成22.4L(标准状况下)时,转移电子数为____________。
【答案】蒸馏 牛角管 蒸馏烧瓶 冷凝管 锥形瓶 5.9 偏高 偏低 偏低 101 2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2 2NA
【解析】
(I)由信息可知,二者互溶,沸点不同,可用蒸馏法分离,以此来解答。
(II)配制95mL浓度为1 mol/L的NaCl溶液需要使用100mL容量瓶;根据m=cVM计算氯化钠的质量,根据c=n/V结合实验操作分析误差;根据稀释过程中溶质的物质的量不变计算。
(III)过氧化钠可与水或二氧化碳反应产生氧气,据此书写方程式,结合氧元素的化合价变化计算转移电子数。
(I)二者互溶,沸点不同,分离上述A、B的混合物,常用的方法是蒸馏,需要的玻璃仪器有酒精灯、温度计、牛角管、蒸馏烧瓶,还有冷凝管和锥形瓶;
(II)(1)配制95mL浓度为1 mol/L的NaCl溶液需要使用100mL容量瓶,则需要NaCl固体的质量为0.1L×1mol/L×58.5g=5.85g,由于托盘天平只能读数到0.1g,则需要称取NaCl固体的质量为5.9g。
(2)①未经冷却趁热将溶液注入容量瓶中,冷却后溶液体积减少,浓度偏高;
②定容后有少量NaCl溶液洒出,溶质减少,浓度偏低;
③定容时仰视观察液面,溶液体积增加,浓度偏低。
(3)设需要加入水的体积为x mL,根据稀释过程中溶质的物质的量不变可知![]() ,解得x=101;
,解得x=101;
(III)过氧化钠可与水或二氧化碳反应产生氧气,因此过氧化钠可用于呼吸面具中作为氧气的来源,在此过程中主要发生的化学反应方程式为2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2;过氧化钠中氧元素化合价从-1价部分升高到0价,部分降低到-2价,则当氧气生成22.4L(标准状况下)即1mol氧气时,转移电子数为2NA。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】“保护环境”是我国的基本国策之一.下列做法不应该提倡的是( )
A.采取低碳、节俭的生活方式
B.严禁排放未经处理的有毒工业废水
C.经常使用一次性筷子、塑料袋等
D.按照规定对生活废弃物进行分类放置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:

下列有关叙述不正确的是
A. 贝诺酯分子中有2种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. lmol乙酰水杨酸最多消耗3molNaOH
D. 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氮基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5mol/L的盐酸,右图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是
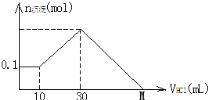
A. 70mL B. 130mL C. 120mL D. 100mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业上使用的印刷电路板,是在敷有铜膜的塑料板上以涂层保护所要的线路,然后用三氯化铁浓溶液作用掉(腐蚀)未受保护的铜膜后形成的。某工程师为了从使用过的腐蚀废液(含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,准备采用下列步骤:
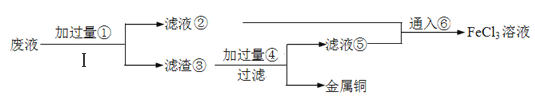
(1)步骤Ⅰ的操作名称:________;所需玻璃仪器:_________、_________、__________。
(2)写出FeCl3溶液与铜箔发生反应的离子方程式:______________________。
(3)检验废腐蚀液中是否含有Fe3+所需试剂名称:___________、实验现象:__________。
(4)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:________________,此转化的化学方程式为:______________________________。
(5)写出③中所含物质:_________⑥发生反应的离子方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡,则原混合溶液中钾离子物质的量浓度为( )
A. 2(2b-a)/V mol·L-1 B. (2b-a)/V mol·L-1 C. 2(b-a)/V mol·L-1 D. (b-a)/V mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法表示下列反应的电子转移情况并将其改写成离子方程式: 3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,______________,离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为酸性介质中,金属铜与氢叠氮酸(HN3) 构成的原电池,总反应方程式为: 2Cu+2Cl-+HN3+3H+=2CuCl(s)+N2↑+NH4+。下列叙述错误的是( )
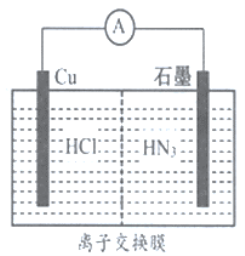
A. 离子交换膜为阳离子交换膜
B. 若将盐酸换成NaCl,电池的运行效率将会下降
C. 负极的电极反应式为:Cu-e-=Cu+
D. 当外电路中流过0.1mol电子时,交换膜左侧离子减少0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,2体积AB2气体和1体积B2气体恰好化合成2体积的C气体,则C的化学式可能为( )
A.AB2
B.AB3
C.A3B
D.A2B3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com