
【题目】“保护环境”是我国的基本国策之一.下列做法不应该提倡的是( )
A.采取低碳、节俭的生活方式
B.严禁排放未经处理的有毒工业废水
C.经常使用一次性筷子、塑料袋等
D.按照规定对生活废弃物进行分类放置
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
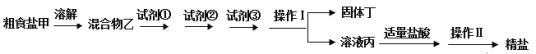
(1)操作Ⅰ需要用到的玻璃仪器有________,操作Ⅱ的名称是________。
(2)试剂①、②、③其实是三种物质:饱和Na2CO3溶液、BaCl2溶液、NaOH溶液,这三种物质的加入顺序可能有多种情况,下列选项中正确的是________。
A.饱和Na2CO3溶液、BaCl2溶液、NaOH溶液
B.BaCl2溶液、饱和Na2CO3溶液、NaOH溶液
C.NaOH溶液、BaCl2溶液、饱和Na2CO3溶液
D.饱和Na2CO3溶液、NaOH溶液、BaCl2溶液
(3)固体丁是混合物,除含有泥沙、CaCO3、BaSO4外,还含有________(填化学式)。
(4)在混合物乙中分别加入试剂①、②、③的过程中,判断滴加BaCl2溶液已过量的方法是:加入BaCl2溶液后,静置,在上层清液中,________。
(5)若先用适量盐酸调节pH值再进行操作Ⅰ,将对实验结果产生影响,其原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三种等体积等物质的量浓度的NaOH溶液。若将甲蒸发一半水,在乙中通入少量CO2,丙不变,然后用等浓度的H2SO4溶液滴定,用甲基橙作指示剂。完全反应后,所需溶液体积是( )
A.甲=丙>乙 B.丙>乙>甲 C.乙>丙>甲 D.甲=乙=丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钪(Sc)及其化合物在电子、宇航、超导等方面有着广泛的应用。某工厂的钛白水解工业废酸中,Sc3+浓度为18mg/L,还含有大量的TiO2+、Fe3+、H+、SO42-等。下图为从该工业废酸中提取Sc2O3的一种流程。

回答下列问题:
(1)在钛白水解工业废酸中,加入双氧水是为了使TiO2+转化为难萃取的[Ti(O2)(OH(H2O)4]+。[Ti(O2)(OH(H2O)4]+中Ti的化合价为+4,其中非极性键的数目为_______。
(2)钪的萃取率(E%)与O/A值[萃取剂体积(O)和废酸液体积(A)之比]的关系如左下图,应选择的最佳O/A值为_______;温度对钪、钛的萃取率影响情况见右下表,合适的萃取温度为10-15℃,其理由是_____________________。

(3)洗涤“油相“可除去大量的钛离子。洗染水是用浓硫酸、双氧水和水按一定比例混合而成。混合过程的实验操作为________________。
(4)25℃时,用氨水调节滤液的pH,当pH=3.5时,滤渣II的主要成分是_______;当pH=6时,滤液中Sc3+的浓度为________。(Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31)
(5)写出用草酸(H2C2O4)“沉钪”得到Sc2(C2O4)3的离子方程式_____________。
(6)若从1m3该工厂的钛白水解度酸中提取得到24.4gSc2O3,则钪的提取率为______(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究氨气及氨水的还原性,某兴趣小组同学设计了以下探究活动。
I.探究氨气的还原性
该兴趣小组同学利用以下装置(夹持,加热仪器略)探究氯气与氨气的反应,其中A、F分别为氯气和氨气的发生装置,B为纯净干燥的氯气与氨气反应的装置。
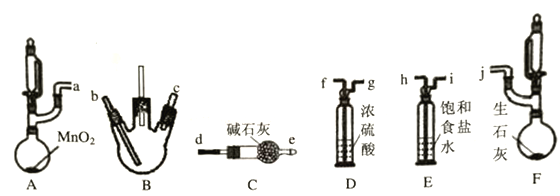
请回答下列问题:
(1)上述装置接口的连接顺序为a接h、i接f、g接___、____接___、____接j,其中装置D的作用是____________。
(2)若氨气足量,装置B中出现的现象为____________。
II.探究氨水的还原性
该兴趣小组同学探究不同条件下高锰酸钾溶液与氨水的反应,实验如下:
实验 | 操作 | 现象 |
① | 取2mL.0.01mol/LKMnO4溶液于试管中,加入新开封1mL浓氨水,加入半滴管蒸馏水,振荡,用橡皮塞塞住。 | 产生棕褐色物质(MnO2),约10min后溶液紫红色变浅 |
② | 取2mL0.01mol/LKMnO4溶液于试管中,加入新开封1mL浓氨水,加入半滴管1:5的硫酸,振荡,用橡皮塞塞住。 | 产生棕褐色物质(MnO2),溶液紫红色立刻变浅,约2min后溶液紫红色完全退去 |
③ | 取2mL0.1mol/LKMnO4溶液于试管中,加入新开封ImL浓氨水,加入半滴管蒸馏水,振荡,用橡皮塞塞住。 | 产生棕褐色物质(MnO2),约10min后溶液紫红色变浅 |
④ | 取2mL0.1mol/LKMnO4溶液于试管中,加入新开封1mL浓氨水,加人半滴管1:5的硫酸,振荡,用橡皮塞塞住。 | 产生棕褐色物质(MnO2),溶液紫红色立刻变浅,约5min后溶液紫红色完全退去 |
(3)实验①中氧化产物为N2,写出该反应的离子方程式:_________。
(4)实验①②说明________________。
(5)实验②比实验④反应速率_____(填“快“或“慢”),原因是_________。
(6)1:5的硫酸溶液(密度为ρ2g·cm-3),可用质量分数为98%的浓硫酸(密度为ρ1g·cm-3)和
蒸馏水按体积比1:5配成,则该1:5的硫酸溶液的物质的量浓度为_____mol/L。(用含ρ1、ρ2的式子表示)
(7)由实验I、II可得出的结论是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快的是
A. v(H2)=0.lmol /(L·min)
B. v(N2) =0.1mol /(L·min)
C. v(NH3)=0.15mol / (L·min)
D. v (N2)=0.02mol /(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质比较不正确的( )
A.热稳定性:HCl>HBr
B.沸点:H2O>H2S
C.碱性:Ca(OH)2>Mg(OH)2
D.酸性:H3PO4>H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)现有A、B两种有机物的液体混合物,如果A、B互溶,且互相不发生化学反应。在常压下,A的沸点为35℃,B的沸点为200℃。分离A、B的混合物的常用方法是:________,需要的玻璃仪器除酒精灯、温度计外有_______、________、________、________。
(II)某课外小组需要配制95mL浓度为1 mol/L的NaCl溶液
(1)需要称取NaCl固体的质量为________g。
(2)在配制1 mol/L的NaCl溶液过程中,下列情况对氯化钠溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“无影响”)。
①未经冷却趁热将溶液注入容量瓶中________;
②定容后有少量NaCl溶液洒出________;
③定容时仰视观察液面________。
(3)若预将100 mL 12mol/L的盐酸稀释为6mol/L的盐酸,需要加入水的体积为________mL。(已知:12mol/L的盐酸密度为1.19g/mL,6mol/L的盐酸密度为1.1g/mL,水的密度为1.0g/mL)。
(III)过氧化钠可用于呼吸面具中作为氧气的来源,在此过程中主要发生的化学反应方程式为_______________________;当氧气生成22.4L(标准状况下)时,转移电子数为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com