
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第12期 总第168期 人教课标版(选修4) 题型:022
硫化物据其溶解性可以分三类:①易溶于水的有
K2S、(NH4)2S等;②易溶于非氧化性强酸、不溶于水的有FeS、ZnS;③大部分的硫化物既不溶于水也不溶于非氧化性强酸,如HgS、Ag2S、CuS、Cu2S.其中,Ag2S、CuS、Cu2S能溶于硝酸发生氧化还原反应,而HgS只能溶于王水(硝酸与盐酸的混合液).氢硫酸溶液中存在下列平衡: H2S(1)将硫化氢通入硫酸铜溶液中生成硫酸的原因是________.
(2)难溶电解质在水溶液里存在着溶解平衡,在常温下,溶液中各离子浓度其系数次方的乘积在一定温度下是一个常数,该常数叫溶度积(Ksp).溶液中各离子浓度(其系数次方)的乘积大于溶度积时则出现沉淀;反之沉淀溶解.已知在常温下,FeS的Ksp=6.25×10-18,H2S饱和溶液中c(H+)与c(S2-)之间存在如下关系:[c(H+)]2·c(S2-)=1.0×10-22.在该温度下,将适量FeS投入硫化氢饱和溶液中,欲使溶液中c(Fe2+)为1 mol/L,应调节溶液的pH为________.
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
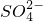
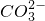
查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com