
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
| 20.01+19.99+20.00 |
| 3 |
| 1 |
| 10 |
| 0.0294 |
| 0.15 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体积为11.2L |
| B、摩尔质量是16 g/mol |
| C、质量为32g |
| D、约含有3.01×1023个氧气分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.
(1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.| ①所有的离子方程式均可以表示一类反应 | |
| ②酸碱中和反应均可表示为H++OH-═H2O | |
| ③离子方程式中凡是难溶性酸、碱、盐均要标“↓”符号 |
查看答案和解析>>
科目:高中化学 来源: 题型:
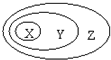 下表中所示物质或概念间的从属关系符合如图的是
下表中所示物质或概念间的从属关系符合如图的是| X | Y | Z | |
| A | 钠元素 | 主族元素 | 短周期元素 |
| B | 电解质 | 化合物 | 纯净物 |
| C | 氢氧化铁 | 胶体 | 分散系 |
| D | 置换反应 | 氧化还原反应 | 放热反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石墨比金刚石稳定 |
| B、金刚石比石墨稳定 |
| C、相同物质的量的石墨比金刚石的总能量高 |
| D、两者互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com