
【题目】下图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g、h分别代表某种化学元素。请依据这8种元素回答下列问题。

(1)上述8种元素的单质中常温下为气态,且密度最小的是______(填化学式)。
(2)f元素的原子结构示意图为_______。
(3)c的最高价氧化物对应水化物的化学式为______。
(4)hg的电子式为_______。
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是______(填化学式)。
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为__________。
(7)f元素的最简单氢化物的水溶液显____性(填“酸”或“碱”),请写出该氢化物久置在空气中变质的化学方程式________。
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为__________。
【答案】 H2 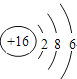 HNO3
HNO3 ![]() H2O>NH3>CH4 2Al+2KOH+2H2O=2KAlO2+3H2↑ 酸 2H2S+O2=2S↓+2H2O 5ClO-+2As+6OH-=2AsO43-+5Cl-+3H2O
H2O>NH3>CH4 2Al+2KOH+2H2O=2KAlO2+3H2↑ 酸 2H2S+O2=2S↓+2H2O 5ClO-+2As+6OH-=2AsO43-+5Cl-+3H2O
【解析】根据元素周期表的结构以及各元素在周期表中的位置,a、b、c、d、e、f、g、h分别代表H、C、N、O、Al、S、Cl、K元素。用元素周期律和相关化学用语作答。
根据元素周期表的结构以及各元素在周期表中的位置,a、b、c、d、e、f、g、h分别代表H、C、N、O、Al、S、Cl、K元素。
(1)上述8种元素的单质中常温下为气态,且密度最小的是H2。
(2)f为S元素,S的核电荷数为16,S原子核外有16个电子,根据原子核外电子排布规律,S的原子结构示意图为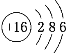 。
。
(3)c为N元素,N原子最外层有5个电子,N元素的最高化合价为+5价,N的最高价氧化物为N2O5,N的最高价氧化物对应水化物的化学式为HNO3。
(4)hg为KCl,KCl中只含离子键,KCl的电子式为![]() 。
。
(5)b、c、d三种元素的最简单氢化物依次为CH4、NH3、H2O,CH4分子间不存在氢键,NH3分子间、H2O分子间存在氢键,且H2O分子间氢键强于NH3分子间氢键,b、c、d三种元素的最简单氢化物的沸点由高到低的顺序为H2O![]() NH3
NH3![]() CH4。
CH4。
(6)元素e的单质为Al,h为K元素,h的最高价氧化物对应的水化物为KOH,Al与KOH溶液反应的化学方程式为2Al+2KOH+2H2O=2KAlO2+3H2↑。
(7)f为S元素,S原子的最外层有6个电子,S的最低负价为-2价,f元素的最简单氢化物为H2S,H2S的水溶液为氢硫酸,氢硫酸显酸性。H2S在空气中久置被空气中氧气氧化成S,反应的化学方程式为O2+2H2S=2S↓+2H2O。
(8)gd-为ClO-,As在碱性溶液中可被ClO-氧化成AsO43-,则ClO-被还原成Cl-,反应可写成As+ClO-→AsO43-+Cl-,在反应中As元素的化合价由0价升至+5价,Cl元素的化合价由+1价降至-1价,根据得失电子守恒可配平为2As+5ClO-→2AsO43-+5Cl-,结合碱性溶液、原子守恒和电荷守恒,反应的离子方程式为2As+5ClO-+6OH-=2AsO43-+5Cl-+3H2O。


 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】短周期金属元素A~E在元素周期表中的相对位置如表所示,下面判断正确的是( )

A. 氢氧化物的化学式及其碱性:COH>D(OH)2>E(OH)3
B. 金属性:A>C
C. 原子半径:C<D<E
D. 最外层电子数:A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组在实验室里制备某些气体,并探究相关物质的性质,需要的仪器如下图所示,部分装置可重复选取。请回答下列问题:
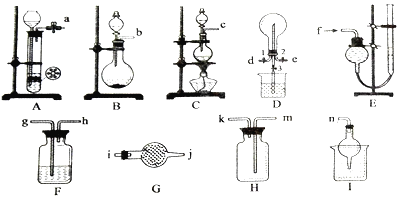
(1)制备并收集纯净的氨气。
①所选装置正确的连接顺序为_________________(填接口编号)。
②简述检验氨气的操作方法___________________________________________。
(2)氧气的制备及性质实验。
①制备装置中发生反应的离子方程式是_______________________。
②将纯净的氯气通入事先放入铁粉的两通硬质玻璃管中,加热制取三氯化铁(极易吸水),则在玻璃管右侧需要直接连接一个_____________装置。若将制得的三氯化铁配制成溶液,请简述操作方法____________________。
③可以用E装置收集并测量氯气的体积,其操作为___________。
(3)标准状况下,在D中可以发生反应3Cl2+2NH3=N2+6HCl。首先在烧瓶中收集满氯气,然后关闭止水夹1、3,打开止水夹2,通入NH3至上述反应恰好完全进行并关闭止水夹2。若此时仅打开止水夹3,D中烧瓶中的现象为____________,试计算烧瓶内所得溶液的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2H2(g)+02(g)=2H2O(l)过程中的能量变化如图所示,下列有关说法中正确的是

A. H1<0 B. H2为该反应的反应热
C. H3为氢气的燃烧热 D. H1=H3-H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱落酸是一种抑制生长的植物激素,因能促使叶子脱落而得名,其结构简式如下图所示,则有关脱落酸的说法中正确的是
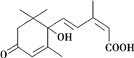
A. 脱落酸的分子式为C15H18O4
B. 脱落酸只能和醇类发生酯化反应
C. 1 mol 脱落酸最多可以和2 mol 金属钠发生反应
D. 1 mol脱落酸最多可以和2 mol 氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿佛加德罗常数的值,下列说法正确的是( )
A. 标准状况下,将6.72L的NO2通入足量的水中转移电子数为0.3NA
B. 常温常压下,22.4LCCl4含有NA个CCl4分子
C. 1 mol Na与足量O2反应,生成Na2O和Na2O2混合物,转移的电子数为NA
D. 18 g D2O所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯的产量可用来衡量一个国家的石油化工发展水平。下列关于乙烯的说法正确的是
A.与苯互为同分异构体
B.分子中存在碳碳双键
C.能使溴的四氯化碳溶液褪色
D.能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是( )

A. 电流从右侧电极经过负载后流向左侧电极
B. 负极发生的电极反应式为N2H4+4OH--4e-=N2↑+4H2O
C. 该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜必需选用阳离子交换膜
D. 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体感科电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH为电解质。下列关于该燃料电池的叙述不正确的是

A. 电流从右侧电极经过负载流向左侧电极
B. 负极发生的电极反应式为N2H4+4OH--4e-=N2+4H2O
C. 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D. 该燃料电池持续放电时,正极发生氧化反应,碱性减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com