
【题目】化学反应中的能量变化,通常表现为热量的变化,如Ba(OH)2·8H2O 与NH4Cl的反应要吸收热量,在化学上叫作吸热反应。其原因是( )。
A.反应物NH4Cl所具有的能量比较低
B.反应物Ba(OH)2·8H2O所具有的能量比较低
C.反应物所具有的总能量高于生成物所具有的总能量
D.反应物所具有的总能量低于生成物所具有的总能量低
科目:高中化学 来源: 题型:
【题目】pH=2.1 的两种酸溶液 A、B 各 1 mL,分别加水稀释到 100 mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )

A.若 a<4.1,则 A、B 都是弱酸
B.稀释后,A 酸溶液的酸性比 B 酸溶液强
C.若 a=4.1,则 A 是强酸,B 是弱酸
D.A、B 两种酸溶液的物质的量浓度一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氢气跟氧气的反应中,破坏1 mol H2中的化学键消耗的能量为x,破坏1 mol O2中的化学键消耗的能量为y,形成1 mol H2O中的化学键释放的能量为z。则下列关系正确的是( )。
A.x+y>z B.x+y<z
C.2x+y<2z D.2x+y>2z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示两个常见固氮反应的平衡常数对数值(lgK)与温度的关系:
①N2+3H2![]() 2NH3;②N2+O2
2NH3;②N2+O2![]() 2NO
2NO
根据图中的数据判断下列说法正确的是 ( )
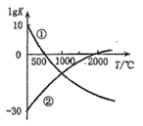
A.只有反应①是放热反应
B.升温,反应①的速率减小反应②的速率增大
C.可以在常温下利用反应①进行工业固氮
D.曲线的交点表示反应①和反应②体系中 N2 的转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F( )是重要的化工原料,其一种合成路线如下:
)是重要的化工原料,其一种合成路线如下:

(1)写出C的官能团名称_________,③的反应类型是____________, A的核磁共振氢谱中峰面积的比为___________。
(2)写出①的化学方程式_____________________________________________________。
(3)D的结构简式为___________________________________。
(4)芳香族化合物化学式C8H8O2,满足下列条件的同分异构体有____________种。
①能发生银镜反应 ②苯环上一氯取代物只有两种
(5)参照上述合成路线,设计由乙烯合成2-丁醇的合成路线(用合成路线流程图表示,并注明反应条件,合成过程中只有无机试剂可任选)
________________________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟是自然界中广泛分布的元素之一。由于氟的特殊化学性质,它和其他卤素在单质及化合物的制备与性质上存在较明显的差异。
Ⅰ.化学家研究发现,SbF5能将MnF4从离子[MnF6]2-的盐中反应得到,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在 423 K 的温度下制备F2的化学方程式:_________________________。

现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。
已知KHF2是一种酸式盐,写出阴极上发生的电极反应式________________________。电解制氟时,要用镍铜合金隔板将两种气体产物严格分开的原因是___________。
Ⅱ.①卤化氢的熔沸点随相对分子质量增加而升高,而HF熔沸点高于HCl的原因是________________________。HF的水溶液是氢氟酸,能用于蚀刻玻璃,其化学反应方程式为:________________________
②已知25 ℃时,氢氟酸(HF)的电离平衡常数Ka=3.6×10-4。
某pH=2的氢氟酸溶液,由水电离出的c(H+)=___________mol/L;若将0.01 mol/L HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度大小关系为:________________________。
③又已知25 ℃时,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol/L HF溶液中加入 1 L 0.2 mol/L CaCl2 溶液,通过列式计算说明是否有沉淀产生:______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳条结寒翠,请君添暖衣.深秋及寒冬的清晨,我们芜湖市经常出现大雾天气,雾中小液滴直径范围是( )
A.小于1nm
B.在1~100nm间
C.大于100nm
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃、101 kPa 下:①2Na(s)+![]() O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1
O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s)ΔH2=-511 kJ·mol-1下列说法正确的是 ( )
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)=2Na2O(s) ΔH=-317 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g) ![]() xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x=
(2)从反应开始到10s,B的平均反应速率为
(3)从反应开始到40s达平衡状态,A的平均反应速率为
(4)平衡时容器中B的体积分数为
(5)该温度下此反应的平衡常数表达式为 数值是
(6)下列各项能表示该反应达到平衡状态是
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量 n(A)∶n(B) =2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com