
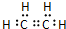 ,C中所含官能团的名称羟基;
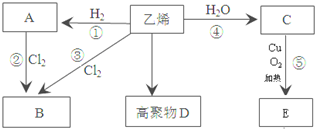
,C中所含官能团的名称羟基;分析 乙烯与水发生加成反应生成C为CH3CH2OH,乙醇氧化得E为CH3COOH,乙烯与氢气发生加成反应生成A为CH3CH3,乙烯与氯气发生加成反应生成B为ClCH2CH2Cl,乙烷与氯气发生取代反应可以得到ClCH2CH2Cl,乙烯发生加聚反应生成高聚物D为 ,据此解答.
,据此解答.
解答 解:乙烯与水发生加成反应生成C为CH3CH2OH,乙醇氧化得E为CH3COOH,乙烯与氢气发生加成反应生成A为CH3CH3,乙烯与氯气发生加成反应生成B为ClCH2CH2Cl,乙烷与氯气发生取代反应可以得到ClCH2CH2Cl,乙烯发生加聚反应生成高聚物D为 ,
,
(1)乙烯的电子式为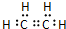 ,C为CH3CH2OH,C中所含官能团的名称是羟基,
,C为CH3CH2OH,C中所含官能团的名称是羟基,
故答案为: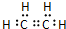 ;羟基;
;羟基;
(2)反应④的反应方程式为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,属于加成反应,
反应⑤的反应方程式为:2CH3CH2OH+O2$→_{△}^{铜}$2CH3CH2O+2H2O,属于氧化反应;
故答案为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,加成反应;2CH3CH2OH+O2$→_{△}^{铜}$2CH3CH2O+2H2O,氧化反应;
(3)反应②为乙烷与氯气的取代,反应条件为光照,反应③为乙烯与氯气的加成反应,若要制取物质ClCH2CH2Cl,最好采用反应③,因为反应②产物有多种,而反应③产物纯净,
故答案为:光照;③;③产物纯净;
(4)①以稀硫酸溶液为电解质溶液,甲烷燃料电池的总反应方程式为CH4+2O2$\stackrel{点燃}{→}$2H2O+CO2,正极电极反应式为:O2+4e-+2H2O═4OH-,
故答案为:CH4+2O2$\stackrel{点燃}{→}$2H2O+CO2;O2+4e-+2H2O═4OH-;
②5.6L O2的物质的量为:$\frac{5.6L}{22.4L/mol}$=0.25mol,转移电子的物质的量为:0.25mol×4=1mol,故答案为:1;
③原电池内部阳离子移向正极,阴离子移向负极,故氢离子从负极区流向正极区,故答案为:b.
点评 本本题考查了有机物的推断,涉及酯、醇、醛、羧酸之间的转化,解题的关键是熟练掌握乙烯的性质,答题时注意烯烃、卤代烃、醇、醛、羧酸、酯之间的转化关系及反应条件,灵活运用知识解答问题.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
| A. | H3PO2溶于水的电离方程式为:H3PO2?3H++PO23- | |
| B. | H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O | |
| C. | 将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的还原产物为H3PO4 | |
| D. | 用惰性电极电解NaH2PO2溶液,其阳极反应式为:H2PO2-4e-+2H2O=O2↑+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:| 滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 1 | 20 | 1.02 | 21.03 | |
| 2 | 20 | 2.00 | 25.00 | |
| 3 | 20 | 0.60 | 20.60 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)<c(OH-)<c(CH3COO-)<c(Na+) | B. | c(H+)<c(OH-)<c(Na+)<c(CH3COO-) | ||
| C. | c(H+)<c(CH3COO-)<c(OH-)<c(Na+) | D. | c(OH-)<c(CH3COO-)<c(H+)<c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
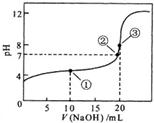 常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000mol/L CH3COOH溶液的滴定曲线如图.下列说法不正确的是( )
常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000mol/L CH3COOH溶液的滴定曲线如图.下列说法不正确的是( )| A. | 点①所示溶液中:2c(Na+)=c(CH3COOH)+c(CH3COO-) | |
| B. | 点②所示溶液中:c(Na+)=c(CH3COO-) | |
| C. | 点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定性检验SO32-,可用HNO3酸化的BaCl2溶液 | |
| B. | 配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度 | |
| C. | 检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液 | |
| D. | 检验氧化铁中的氧化亚铁,先用硫酸溶液溶解,然后加入盐酸酸化的高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com