
分析 (1)金属钠露置在空气中,表面变暗是因为钠与氧气反应生成氧化钠;
(2)钠在空气中加热生成过氧化钠;
(3)钠与水反应生成氢氧化钠和氢气;
(4)将金属钠投入CuSO4溶液中,反应生成氢氧化铜沉淀,硫酸钠和氢气;
(5)铁与水蒸气反应生成四氧化三铁和氢气;
(6)铝与NaOH溶液反应生成偏铝酸钠和氢气.
解答 解:(1)钠与氧气反应生成氧化钠,方程式:4Na+O2=2Na2O,
故答案为:4Na+O2=2Na2O;
(2)钠在空气中加热生成过氧化钠,方程式:2Na+O2 $\frac{\underline{\;点燃\;}}{\;}$Na2O2,
故答案为:2Na+O2 $\frac{\underline{\;点燃\;}}{\;}$Na2O2;
(3)将金属钠投入水中,钠与水反应生成氢氧化钠和氢气,离子方程式:2Na+2H2O=2Na++OH-+H2↑;
故答案为:2Na+2H2O=2Na++OH-+H2↑;
(4)将金属钠投入CuSO4溶液中,反应生成氢氧化铜沉淀,硫酸钠和氢气,离子方程式:2Na+2H2O+Cu2+=Cu(OH)2↓+H2↑+2Na+;
故答案为:2Na+2H2O+Cu2+=Cu(OH)2↓+H2↑+2Na+;
(5)铁与水蒸气反应生成四氧化三铁和氢气,化学方程式:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(6)Al与NaOH溶液反应生成偏铝酸钠和氢气,离子反应为2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑,
故答案为:2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑.
点评 本题考查离子反应方程式的书写,为高频考点,明确钠及其化合物的性质以及发生的化学反应是解答本题的关键,题目难度中等.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:解答题
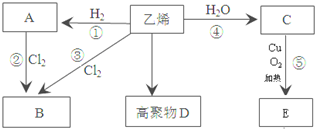
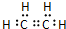 ,C中所含官能团的名称羟基;
,C中所含官能团的名称羟基;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
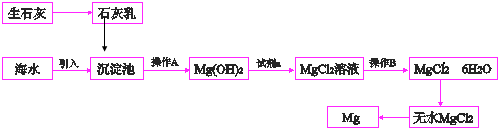
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧是将化学能只转化为热能 | |
| B. | 浓硫酸溶于水发热,所以该反应为放热反应 | |
| C. | 反应物的总能量高于生成物的总能量是放热反应 | |
| D. | 吸热反应是断裂化学键吸收的总能量小于形成化学键放出的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去AlCl3溶液中的FeCl3杂质的方法:先加入足量浓氨水,过滤,再加入过量盐酸,得到纯净AlCl3溶液 | |
| B. | 可以用金属钠和MgCl2溶液反应置换金属Mg;可以通过化合反应制备Fe(OH)3 | |
| C. | 对某溶液进行焰色反应,火焰呈黄色,则证明该溶液中含有钠盐,可能有钾盐 | |
| D. | 配制氯化铁溶液时,将氯化铁固体溶解在较浓的盐酸中再加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
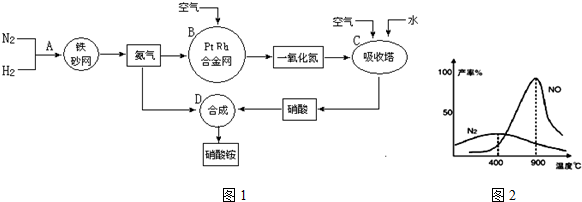
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 验证某有机物属于烃,完成的实验只要证明它完全燃烧后的产物只有H2O和CO2 | |
| B. | 煤干馏得到的煤焦油可以分离出苯,苯是无色无味的液态烃 | |
| C. | 黄酒中存在的某些微生物可以使部分乙醇氧化,转化为乙酸,酒就有了酸味 | |
| D. | 乙烯使酸性高锰酸钾溶液,溴的四氯化碳溶液褪色,由于乙烯发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com