
【题目】矿业废水中Al3+含量的测定和处理是环境保护的重要课题。
(1)向矿业废水中加入NaOH溶液至沉淀不再溶解,再加入一定量的NaHCO3溶液搅拌,反应生成丝钠铝石[NaAl(OH)2CO3]沉淀,过滤除去。写出加入NaHCO3溶液生成丝钠铝石沉淀的离子方程式:____________________________________。
(2) 为确定加入NaHCO3溶液的量,需测定矿业废水中Al3+的含量。工业上常采用EDTA络合滴定法,步骤如下:
步骤1:CuSO4标准液的配制与标定。取一定量胆矾溶于水,加入适量稀H2SO4,转移到1 L容量瓶中定容。准确量取25.00 mL所配溶液置于250 mL锥形瓶中,用0.005 0 mol·L-1EDTA标准液滴定至终点。重复3次实验,平均消耗EDTA标准液10.00 mL 。
步骤2:样品分析。取10.00 mL矿业废水置于250 mL锥形瓶中,加入一定体积柠檬酸,煮沸;再加入0.005 0 mol·L-1的EDTA标准液20.00 mL,调节溶液pH至4.0,加热;冷却后用CuSO4标准液滴定至终点,消耗CuSO4标准液30.00 mL。(已知:Cu2+、Al3+与EDTA反应的化学计量比均为1∶1)
步骤1中,重复3次实验的目的是____________________________。
② Fe3+也可与EDTA反应,步骤2中加入的柠檬酸是作为掩蔽剂,消除Fe3+的干扰。若该矿业废水样品中含有Fe3+,而上述实验中未加入柠檬酸,则测定的Al3+含量将________(填“偏大”“偏小”或“无影响”)。
③计算该矿业废水中Al3+的含量____________(用mg·L-1表示)(写出计算过程)。
【答案】AlO2-+2HCO3-+Na+===NaAl(OH)2CO3↓+CO32- 减小实验误差,提高标定的CuSO4标准液浓度的准确性 偏大 108 mg·L-1
【解析】
(1)矿业废水中含Al3+,加入过量NaOH得到AlO2-,再加入一定量的NaHCO3溶液得到丝钠铝石沉淀;
(2)可由步骤1得出CuSO4标准溶液的浓度,步骤2中用CuSO4标准溶液滴定的EDTA标准液为与Al3+反应后剩下的EDTA标准液,结合Cu2+、Al3+与EDTA反应的化学计量比均为1∶1建立关系式进行计算。
(1)根据题干信息可知,矿业废水中含Al3+,加入过量NaOH溶液后,Al3+转化为AlO2-,再加入一定量的NaHCO3溶液得到丝钠铝石[NaAl(OH)2CO3]沉淀,反应的离子反应方程式为AlO2-+2HCO3-+Na+===NaAl(OH)2CO3↓+CO32-,故答案为:AlO2-+2HCO3-+Na+===NaAl(OH)2CO3↓+CO32-;
(2)①为避免实验的偶然误差,需要进行重复实验,提高CuSO4标准液浓度的准确性,故答案为:减小实验误差,提高标定的CuSO4标准液浓度的准确性;
②若该矿业废水样品中含有Fe3+,而上述实验中未加入柠檬酸,则Fe3+与EDTA反应,使得消耗的EDTA标准液体积偏大,从而使得测定的Al3+含量偏大,故答案为:偏大;
由步骤1,CuSO4标准溶液的浓度![]() ,步骤2中用CuSO4标准溶液滴定的EDTA标准液为与Al3+反应后剩下的EDTA标准液,已知消耗CuSO4标准液30.00 mL,且Cu2+与EDTA反应的化学计量比为1∶1,则与Al3+反应后剩下的EDTA标准液的物质的量为
,步骤2中用CuSO4标准溶液滴定的EDTA标准液为与Al3+反应后剩下的EDTA标准液,已知消耗CuSO4标准液30.00 mL,且Cu2+与EDTA反应的化学计量比为1∶1,则与Al3+反应后剩下的EDTA标准液的物质的量为![]() ,则消耗的EDTA的物质的量
,则消耗的EDTA的物质的量![]() ,又Al3+与EDTA反应的化学计量比也为1∶1,则
,又Al3+与EDTA反应的化学计量比也为1∶1,则![]() ,则该废水中Al3+的含量为
,则该废水中Al3+的含量为![]() ,故答案为108mg/L。
,故答案为108mg/L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定条件下向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,图1表示各物质浓度随时间的变化,图2表示速率随时间的变化。t2、t3、t4、t5时刻后各改变一种条件,且改变条件均不同。若t4时刻改变条件是压强,则下列说法错误的是
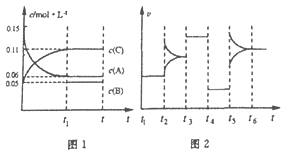
A. 若t1=15s,则前15s的平均反应速率v(C)=0.004mol·L-1·s-1
B. 该反应的化学方程式为:3A(g) ![]() B(g)+2C(g)
B(g)+2C(g)
C. t2、t3、t5时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度
D. B的起始物质的量为0.04mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学方法除去下列物质中混有的少量杂质,其中括号内为杂质,写出除杂需加入的试剂(用化学式表示)以及发生反应的离子方程式。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式___;
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式____;
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式____;
(4)气体CO2(HCl)除杂发生反应的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德。某种兴奋剂的结构简式如图所示。有关该物质的说法中正确的是

A. 该物质遇FeCl3溶液呈紫色,且属于苯酚同系物
B. 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C. 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4mol和7mol
D. 该分子中所有碳原子可以共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,利用FeCl2、NH4H2PO4、Li2CO3和苯胺(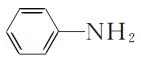 )制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
)制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
(1)Fe2+基态核外电子排布式为________。
(2) N、P、O三种元素的电负性由大到小的顺序为________。
(3) CO32-中心原子轨道的杂化类型为________;与CO32-互为等电子体的一种分子为________(填化学式)。
(4) 1 mol苯胺分子中含有σ键的数目为________;苯胺与甲苯的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某有机物的结构表示为![]() ,其名称是________________________。
,其名称是________________________。
(2)写出下列反应的化学方程式:
①草酸能使酸性高锰酸钾溶液褪色:____________________________________。
②把浓硝酸、浓硫酸和甲苯混合加热制备TNT:______________________________。
③溴乙烷在一定条件下发生消去反应:__________________________________。
(3)某烃A分子中碳的质量分数为90.57%,在某温度下V L该烃的蒸气质量是相同状况下V L H2质量的53倍,则烃A的分子式为______________;若烃A分子中含有苯环,且苯环上的一氯代物只有一种,则A的结构简式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是化学中常用的思维方法。下列推理正确的是
A.lmol晶体硅含Si-Si键的数目为2NA,则1mol金刚砂含C-Si键的数目也为2NA
B.Ca(HCO3)2溶液中加入过量的NaOH溶液,发生化学反应的方程式:![]()
则Mg(HCO3)2溶液中加入过量的NaOH溶液,发生化学反应的方程式: ![]()
C.标准状况下,22.4 L CO2中所含的分子数目为NA个,则22.4 LCS2中所含的分子数目也为NA个
D.NaClO溶液中通人过量CO2发生了反应:![]() ,则Ca(ClO)2溶液中通入过量CO2发生了:
,则Ca(ClO)2溶液中通入过量CO2发生了:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾已经成为部分城市发展的障碍。雾霾形成的最主要原因是人为排放,其中汽车尾气污染对雾霾的“贡献”逐年增加。回答下列问题:
(1)汽车尾气中含有NO,N2与O2生成NO的过程如下:

①1molO2与1molN2的总能量比2molNO的总能量___(填“高”或“低”)。
②N2(g)+O2(g)═2NO(g)的△H=___。
③NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g)2CO2(g)+N2(g)△H=akJmol﹣1,但该反应速率很慢,若使用机动车尾气催化转化器,可以使尾气中的NO与CO转化成无害物质排出。上述反应在使用“催化转化器”后,a值___(选填“增大”“减小”或“不变”)。
(2)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H1。如图是该反应的能量变化图:

①通过图中信息可判断反应CH3OH(g)+H2O(g)═CO2(g)+3H2(g)的△H1___(选填“>”“=”或“<”)0
②图中途径(Ⅱ)的条件是___,途径(Ⅰ)的反应热___(选填“>”“=”或“<”)途径(Ⅱ)的反应热。
③已知下列两个热化学方程式:
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(g)△H2
H2(g)+![]() O2(g)═H2O(g)△H3
O2(g)═H2O(g)△H3
△H1、△H2、△H3三者的关系式为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据化学能和热能、电能相关的知识,请回答下列问题:
I.已知31 g白磷(P4)变为31 g红磷(P)时释放能量。上述变化属于__________变化(填“物理”或“化学”);稳定性白磷_________红磷(填“>”或“<”);
II.氢气是一种清洁能源,在我国航天工程中也有应用。
(1)已知1g氢气燃烧生成气态水放出热量121kJ,其中断裂1molH—H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH—O键放出热__。
(2)航天技术上使用的氢-氧燃料电池原理可以简单看作下图“氢-氧燃料电池的装置图” 则:
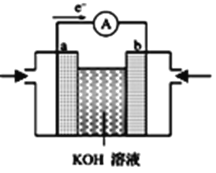
①a极为电池的______(填“正极”或“负极”);溶液中OH-移向_______电极(填“a”或“b”)。
②放电时,b电极附近pH_______。(填增大、减小或不变)。
③如把H2改为甲烷,总反应为:CH4+ 2O2 + 2OH- = CO32- + 3H2O,则负极电极反应式为:_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com