
用NA表示阿伏加德罗常数,下列叙述中正确的有几项
①78g Na2O2与足量的二氧化碳反应,转移电子数目为NA
②足量Fe与标况下22.4L的氯气反应转移电子数目为2NA
③常温常压下16gO2与O3混合气中含有氧原子数目为NA
④0.2mol/LNaOH溶液中OH-的数目为0.2NA
A.1项 B.2项 C.3项 D.4项
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:填空题
(12分)硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,其流程示意图如下:

(1)若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为 。
(2)上述流程中采用稀碱液比用热水更好,理由是 。
(3)常温下,取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)= mol·L-1。
(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示)。为使除汞效果最佳,应控制的条件是:x= ,pH控制在 范围。

②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有 。
(5)常温下利用Fe2+、Fe3+的相互转化,可将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省郴州市高三第二次月考理综化学试卷(解析版) 题型:选择题
现有CuO和Fe3O4的混合物7.6g,向其中加入1mol/L的H2SO4溶液100 mL恰好完全反应,若将15.2 g该混合物用足量CO还原,充分反应后剩余固体质量为:
A.13.6g B.12g C.6g D.3.2 g
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省荆州市部分县市高三上学期期末统考理综化学试卷(解析版) 题型:选择题
现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法正确的是
A.简单阳离子的氧化性:Y>X
B.气态氢化物的稳定性:Z>M
C.简单离子半径由大到小的顺序是:Z>M>Y
D.等浓度X2Z与Y2Z的溶液中,水的电离程度:X2Z>Y2Z
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省南阳市高三上学期期末理综化学试卷(解析版) 题型:选择题
将11.2g的Mg—Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体。再向所得溶液中加入过量的NaOH溶液,产生21.4g沉淀.推断气体x的成分可能是
A.0.3molNO2
B.0.2molNO2和0.1molN2O4
C.0.1molNO、0.2molNO2和0.05molN2O4
D.0.6molNO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高三上学期期末理综化学试卷(解析版) 题型:实验题
(15分)对叔丁基苯酚 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:

步骤l:组装仪器,用量筒量取2.2 mL叔丁基氯(过量),称取1.6 g苯酚,搅拌使苯酚完全溶解,并装入滴液漏斗。
步骤2:向X中加入少量无水AlCl3固体作催化剂,打开滴液漏斗旋塞,迅速有气体放出。
步骤3:反应缓和后,向X中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,得到粗产物,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器X的名称为 。
(2)步骤2中发生主要反应的化学方程式为 。该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是 。
(3)图中倒扣漏斗的作用是 。苯酚有腐蚀性,能使蛋白质变性,若其溶液沾到皮肤上可用 洗涤。
(4)在取用苯酚时发现苯酚冻结在试剂瓶中,可采取的措施为____ 。
(5)下列仪器在使用前必须检查是否漏液的是 (填选项字母)。
A.量筒
B.容量瓶
C.滴定管
D.分液漏斗
E.长颈漏斗
(6)本实验中,对叔丁基苯酚的产率为 。(请保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高三上学期期末理综化学试卷(解析版) 题型:选择题
有机物C4H8Cl2的结构中只含有一个甲基的同分异构体有几种(不考虑立体异构)
A.3 B.4 C.7 D.8
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:选择题
反应CO2(g)+2NH3(g) CO(NH2)2(s)+H2 O(g) △H<0,达到平衡时,下列说法正确的是
CO(NH2)2(s)+H2 O(g) △H<0,达到平衡时,下列说法正确的是
A.加入催化剂,平衡常数不变
B.减小容器体积,正、逆反应速率均减小
C.增大CO(NH2)2的量,CO2的转化率减小
D.降低温度,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:选择题
正、负极都是碳材料的双碳性电池,电池充、放电过程为2nC+LiA  CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
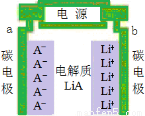
A.a是电池的负极
B.放电时,A-离子向b极移动
C.放电时,负极的电极反应式是nC-e-+A-= CnA
D.充电时,电解质中的离子浓度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com