
【题目】将一定量的氯气通入50mL 10.00 mol·L-1的氢氧化钠浓溶液中,加热少许时间后,溶液中只有NaCl、NaClO、NaClO3三种溶质。下列说法正确的是
A.与NaOH反应的氯气物质的量:0.25mol<n(Cl2)<0.5mol
B.若反应中转移的电子为n mol,则0.25<n<0.5
C.溶液中n(Na+):n(Cl-)可能为7:5
D.溶液中n(NaCl):n(NaClO):n(NaClO3)可能为10:2:1
【答案】C
【解析】
n(NaOH)=10.00mol/L×0.05L=0.5mol
A. 若氯气和NaOH只发生反应2NaOH+Cl2=NaCl+NaClO+H2O,则消耗氯气为0.25mol,若只发生反应6NaOH+3Cl2=5NaCl+NaClO3+3H2O,消耗的氯气为0.25mol,所以与NaOH反应的氯气物质的量为0.25mol,故A错误;
B. 氯气和NaOH反应有2NaOH+Cl2=NaCl+NaClO+H2O、6NaOH+3Cl2=5NaCl+NaClO3+3H2O,当生成NaCl和NaClO时转移电子最少,0.5molNaOH消耗0.25molCl2,生成0.25molNaCl转移电子的物质的量为0.25mol;当生成NaCl和NaClO3时转移电子数目最多,0.5molNaOH消耗0.25molCl2,生成0.42molNaCl转移电子的物质的量为0.42mol,所以如果反应中转移的电子为nmol,则0.25<n<0.42,故B错误;
C. 若氯气和NaOH只发生反应2NaOH+Cl2=NaCl+NaClO+H2O,生成0.25mol NaCl和0.25mol NaClO,n(Na+)=0.5mol,n(Cl-)=0.25mol,n(Na+):n(Cl-)=2:1;若只发生反应6NaOH+3Cl2=5NaCl+NaClO3+3H2O,生成![]() mol NaCl和
mol NaCl和![]() mol NaClO,n(Na+)=
mol NaClO,n(Na+)= ![]() ,n(Cl-)=
,n(Cl-)= ![]() mol,n(Na+):n(Cl-)=0.5:
mol,n(Na+):n(Cl-)=0.5:![]() =6:5,;若两个反应都存在,2>
=6:5,;若两个反应都存在,2>![]() >
>![]() ,故C正确;
,故C正确;
D. NaCl为氯气得电子的产物,NaClO和NaClO3为氯气失电子的产物,根据得失电子守恒,若溶液中n(NaCl):n(NaClO):n(NaClO3)可能为10:2:1,反应中得到电子总物质的量为10×1=10mol,反应中失去电子总物质的量为2×1+1×5=7mol;得失电子不守恒,故D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.1 mol O2的体积是22.4 L
B.1.7 g NH3中含有的质子数约为6.02×1023
C.8 g S在足量O2中完全燃烧转移的电子数约为3.01×1023
D.0.5 mol·L1NaCl溶液中含有Cl的物质的量为0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100 mL FeBr2溶液中通入标准状况下2.24 L Cl2,溶液中有![]() 的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为( )
的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为( )
A.4 mol L-1B.![]() mol L-1C.
mol L-1C.![]() mol L-1D.
mol L-1D.![]() mol L-1
mol L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与50 mL 0.1 mol·L-1的Na2CO3溶液中Na+的物质的量相同的溶液是( )
A.50 mL 0.2 mol·L-1的NaCl溶液B.100 mL 0.2 mol·L-1的NaCl溶液
C.25 mL 0.1 mol·L-1的Na2SO4溶液D.50 mL 0.1 mol·L-1的NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
A. 用敞口容器称量KOH且时间过长
B. 配置前先向容量瓶中加入少量蒸馏水
C. 容量瓶盛过KOH溶液,使用前未洗涤
D. 溶解后快速转移到容量瓶,然后加足量蒸馏水,定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了为锂电池发展作出突出贡献的三位科学家。某废旧锂电池正极主要由LiFePO4、铝箔、炭黑等组成,Fe、Li、P具有极高的回收价值,具体流程如下:

(1)过程ⅰ生成NaAlO2溶液的离子方程式是__。
(2)过程ⅱ中HCl/H2O2的作用是__。
(3)浸出液X的主要成分为 Li+、Fe3+、H2PO4-等。过程ⅲ控制碳酸钠溶液浓度20%、温度85 ℃、反应时间3 h条件下,探究pH对磷酸铁沉淀的影响,如图所示。
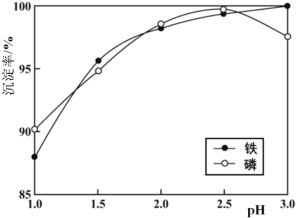
①综合考虑铁和磷沉淀率,最佳pH为__。
②结合平衡移动原理,解释过程ⅲ中pH增大,铁和磷沉淀率增大的原因__。
③当pH>2.5后,随pH增加,磷沉淀率出现了减小的趋势,解释其原因__。
(4)LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应制取,共沉淀反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示。分别滴加NaOH溶液(c=0.1 mol·L-1)至pH=7。消耗NaOH溶液的体积为Vx、Vy则( )
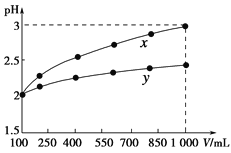
A.x为弱酸,Vx<VyB.x为强酸,Vx>Vy
C.y为弱酸,Vx<VyD.y为强酸,Vx>Vy
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定碳酸钠纯度(只含有少量氯化钠),学生设计了如下两个实验方案。
[方案1]称取![]() 样品,置于小烧杯中,加适量水完全溶解;向小烧杯中加入足量氢氧化钡溶液,过滤,洗涤、干燥沉淀,称量沉淀的质量为19.700克,计算。
样品,置于小烧杯中,加适量水完全溶解;向小烧杯中加入足量氢氧化钡溶液,过滤,洗涤、干燥沉淀,称量沉淀的质量为19.700克,计算。
(1)写出生成沉淀的反应方程式__________________。
(2)过滤操作需要的玻璃仪器__________________。
(3)计算碳酸钠的质量分数为______________(保留两位小数)。
[方案2]用下图装置,排液法测定![]() 的体积,并根据样品质量和
的体积,并根据样品质量和![]() 的体积计算
的体积计算
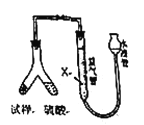
(4)为了减小测定![]() 的体积误差,量气管中加入的液体
的体积误差,量气管中加入的液体![]() 为______(填化学式)。
为______(填化学式)。
(5)通过实验,测得该试样中碳酸钠的质量分数偏高,产生这种现象的原因可能是______。
A.测定气体体积时未冷却至室温
B.气体进入量气管前未用浓硫酸干燥
C.![]() 型管中留有反应生成的气体
型管中留有反应生成的气体
D.反应结束后读数时水准管的水面高于量气管的水面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Rozerem用于治疗难以入睡型失眠症,是首个没有列为特殊管制的非成瘾失眠症治疗药物,合成该有机物过程中涉及如下转化,下列说法不正确的是( )
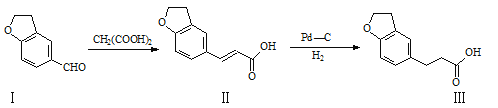
A.化合物Ⅰ、Ⅱ均能使酸性KMnO4溶液褪色
B.Ⅱ→Ⅲ的反应为加成反应
C.1mol化合物Ⅱ最多能与5molH2发生加成反应
D.与化合物Ⅰ互为同分异构体,且分子中含有2个醛基的芳香族化合物有9种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com