
【题目】目前工业上有一种方法是用CO2生产燃料甲醇(CH3OH)。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
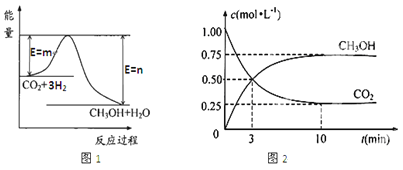
(1)该反应为_________热反应,原因是_____________________。
(2)下列能说明该反应已经达到平衡状态的是_________(填序号)
A.v (H2)=3v(CO2) B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH) D.容器内气体密度保持不变
E.CH3OH 中1 mol H—O键断裂的同时2 mol C=O键断裂
F. 混合气体的平均摩尔质量不变
(3)在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=________。 达平衡时容器内平衡时与起始时的压强比____________。
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应为________________,
与铅蓄电池相比,当消耗相同质量的负极物质时,甲醇燃料电池的理论放电量是铅蓄电池的___________倍(保留小数点后1位)。
【答案】 放热 生成物的能量低于反应物的能量 BCEF 0.225 5:8 CH3OH-6e-+H2O=6H++CO2 19.4
【解析】(1)由图可知,反应物的总能量大于生成物的总能量,则该反应为放热反应;(2)A.v (H2)= 3v(CO2) ,始终存在,不能判断正逆反应速率关系,不能判定平衡状态,A错误;B.该反应为气体体积不等的反应,则容器内气体压强保持不变,达到平衡状态,B正确;C.v逆(CO2)= v正(CH3OH) ,可知正逆反应速率相等,能判定平衡状态,C正确;D.混合气体的质量、体积不变,则容器内气体密度始终保持不变,不能判定平衡状态,D错误;E.1mol H-O键断裂的同时2mol C=O键断裂,可知正逆反应速率相等,能判定平衡状态,E正确;F.混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,但物质的量是变化的,所以混合气体的平均摩尔质量不变说明反应达到平衡状态,F正确;答案选BCEF;(3)CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
开始 1 3 0 0
转化 0.75 2.25 0.75 0.75
平衡 0.25 0.75 0.75 0.75
从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=2.25mol/L÷10min=0.225mol/(L·min);达平衡时容器内平衡时与起始时的压强之比为(0.25+0.75+0.75+0.75):(1+3)=5:8;
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应式为CH3OH-6e-+H2O=6H++CO2;铅蓄电池中负极材料为Pb,氧化为PbSO4,甲醇燃料电池中负极通入甲醇,氧化生成CO2,相同质量提供电子数目之比为![]() =32:621,则甲醇燃料电池的理论放电量是铅蓄电池的621/32=19.4倍。
=32:621,则甲醇燃料电池的理论放电量是铅蓄电池的621/32=19.4倍。


科目:高中化学 来源: 题型:
【题目】一定条件下进行反应:COCl2(g) ![]() Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法不正确的是( )
A. 使用恰当的催化剂能加快该反应速率
B. 该条件下,COCl2的最大转化率为60%
C. 6s时,反应达到最大限度即化学平衡状态
D. 生成Cl2的平均反应速率,0~2s比2~4s快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的有机化工原料。
(1)已知:
①C2H4(g)+H2O(g) ![]() C2H5OH(g) ΔH1=-45.5kJ/mol
C2H5OH(g) ΔH1=-45.5kJ/mol
②2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH2=-23.9kJ/mol
CH3OCH3(g)+H2O(g) ΔH2=-23.9kJ/mol
③C2H4OH(g) ![]() CH3OCH3(g) ΔH3=+50.7kJ/mol
CH3OCH3(g) ΔH3=+50.7kJ/mol
请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:_____________。
(2)合成甲醇的反应为:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。

①温度升高甲醇的体积分数增大的原因是___________;
②根据图像判断ΔH________________(填“>”、“<”或“=”)0。
(3)某研究小组提出将4CH3OH+6NO2+8OH-=3N2+4CO32-+12H2O设计成原电池,以实现污染物的利用,装置如图乙所示(图中电极均为多孔的惰性电极)。

①电极A的名称是_____________。
②写出原电池电极B的电极反应式:___________。
③若用该电池对铁制品表面镀铜,反应一段时间后,铁制品质量增加64g,理论上处理NO2的质量为________g。
(4)为了研究甲醇转化为二甲醚的反应条件,某研究与小组在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2=-23.9KJ/mol。
CH3OCH3(g)+H2O(g) ΔH2=-23.9KJ/mol。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
Ⅰ | T1 | 0.20 | 0.080 | 0.080 |
Ⅱ | T1 | 0.40 | a | a |
Ⅲ | T2 | 0.20 | 0.090 | 0.090 |
①T1温度下该反应的平衡常数K=_______;反应温度T1_________T2(填“大于”或“小于”。)
②容器Ⅱ中a=______。
③下列说法能说明反应达到平衡状态的是___________(填字母)。
A.容器中气体压强不再变化
B.用CH3OH 和CH3OCH3表示的反应速率之比为2:1
C.混合气体的密度不变
D.容器内CH3OH和CH3OCH3的浓度之比为2:1
E.单位时间内生成2molCH3OH 的同时生成1mol H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含铜样品的主要成分为a CuCO3·bCu(OH)2(a、b均为最简正整数)。为测定其化学组成和Cu元素的质量分数。甲乙两个实验小组查阅资料,设计了不同的实验方案(假定杂质对实验无干扰)。
Ⅰ.甲组同学利用一下方法测定:
①在一定质量的样品中加入过量的稀硫酸,过滤,测量产生气体的体积
②在滤液中加过量的NaOH稀溶液,过滤
③灼烧②中所得滤渣、直至残留固体恒重
(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是_____,滤渣应在_____(填仪器名称)中进行灼烧。
(2)利用右图装置测量气体体积,读数时应注意:
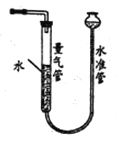
①恢复至室温;②__________;③平视且视线与凹液面最低点相切。
若操作无误,但气体体积测量结果仍然明显偏低,合理的改进措施是____________。
(3)甲组同学在处理实验数据时,将常温常压下测得的气体体积VL换算成V/22.4mol进行计算,则计算所得a值将_______(填“偏大”、“偏小”或“无影响”)。
Ⅱ.乙组同学利用下图装置进行测量(夹持及加热装置略去):
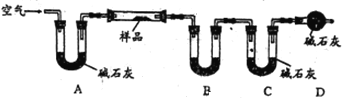
(4)U型管B中的药品是_________,D的作用是_________。
(5)若样品的质量为20g,充分反应后测得B中固体质量增加了0.9g,C中固体质量增加了4.4g,则样品中主要成分的化学式为___________,样品中铜元素的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的钠进行下列实验,其中生成氢气最多的是 ( )
A.将钠投入到足量水中 B.将钠用铝箱包好并刺一些小孔,再放入足量的水中
C.将钠放入足量硫酸铜溶液中 D.将钠放入足量稀盐酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用或转化NO2、SO2、CO、NO等污染性气体是人们共同关注的课题。
Ⅰ.某化学课外小组查阅资料后得知:2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g)![]() N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) H1<0
N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) H1<0
②N2O2(g)+O2(g)![]() 2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) H2<0
2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) H2<0
请回答下列问题:

(1)反应2NO(g)+O2(g)![]() 2NO2(g)的H=________________(用含H1和H2的式子表示)。一定温度下,反应2NO(g)+O2(g)
2NO2(g)的H=________________(用含H1和H2的式子表示)。一定温度下,反应2NO(g)+O2(g)![]() 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=_____________________。
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=_____________________。
(2)决定2NO(g)+O2(g)![]() 2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________E2(填“>”、“<”或“=”)。
2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________E2(填“>”、“<”或“=”)。
Ⅱ.(3)反应N2O4(g)![]() 2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是_______________,理由是__________________________________________________________________________________________。
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是_______________,理由是__________________________________________________________________________________________。
(4)在25℃时,将a mol·L-1的氨水溶液与0.02 mol·L-1 HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示250C时NH3·H2O的电离常数Kb=_________________。用质量分数为17%,密度为0.93 g/cm3的氨水,配制200 mL a mol·L-1的氨水溶液,所需原氨水的体积V=___________mL。
(5)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_________,阴极的电极反应式是__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神舟号”载人航天器中宇航员所在的轨道和返回仓都是密封的,宇航员吸入氧气、呼出二氧化碳,如果二氧化碳浓度过高,会使宇航员困乏,呼吸频率加快,严重的还会窒息,为解决此问题,应在航天仓中加入( )
A.Na2O2 B.Na2CO3
C.NaOH D.高压氧气瓶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com