
����Ŀ��������֪ij��Ӧ�з�Ӧ����������У�KMnO4��H2SO4��MnSO4��H2C2O4��K2SO4��H2O��һ��δ֪��X��
(1)��֪0.5 molH2C2O4�ڷ�Ӧ��ʧȥ1 mol��������X����X�Ļ�ѧʽΪ______________��
(2)���������ͻ�ԭ������ƽ��ϵ���������з����У����õ����ű������ת�Ƶķ������Ŀ��
___________________________
������ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+���ӹ�ҵ��ˮ�л������������ͽ���ͭ�Ĺ���������ͼ��ʾ��
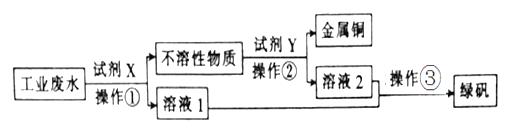
(1)ͼ�в�����Ϊ______________��������Ϊ_______________________________��
(2)�Լ�XΪ______���ѧʽ�����������漰�����ӷ�Ӧ����ʽΪ___________________��
���𰸡�CO2 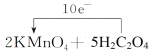 ���� ����Ũ������ȴ�ᾧ Fe Fe + 2H+ = Fe2+ + H2��
���� ����Ũ������ȴ�ᾧ Fe Fe + 2H+ = Fe2+ + H2��
��������
����1����֪0.5mol H2C2O4�ڷ�Ӧ��ʧȥ1mol��������X��̼Ԫ�ػ��ϼ�Ϊx��KMnO4����ԭΪMnSO4����ϵ����غ�������̼Ԫ�ػ��ϼۣ�2��[x-��+3��]��0.5mol=1��x=+4�������ɵ�XΪCO2��
��2�����������ǿ�����ԣ�����ѡ�����������������H2C2O4��C�Ļ��ϼ�Ϊ+3�ۣ�CO2��C�Ļ��ϼ�Ϊ+4�ۣ�Ҫѡ��ʧ���ӵ���������ԭ��������ѡ��H2C2O4����ԭ�����ɸ����������������������μӷ�Ӧ�����ݷ�Ӧǰ��Ԫ���غ㣬ˮ���������У�
�÷�Ӧ�л��ϼ۵ı仯Ϊ��KMnO4��MnSO4��MnԪ����+7����+2�ۣ�һ��KMnO4���ӵ�5�����ӣ�H2C2O4��CO2��CԪ����+3����+4�ۣ�һ��H2C2O4ʧȥ2�����ӣ����Ե�ʧ���ӵ���С������Ϊ10������KMnO4�ļ�����Ϊ2��H2C2O4�ļ�����Ϊ5������Ԫ�ظ���ԭ���غ���ƽ���ʷ�ӦΪ��2KMnO4+5H2C2O4+3H2SO4=2MnSO4+10CO2��+8H2O+K2SO4���õ����ű������ת�Ƶķ������ĿΪ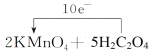 ��
��
��ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+����������ͼ�п���֪������ɻ�������������ͭ���ȼӹ������۰�ͭ�û����������Լ�XΪ���ۣ�����1�ǹ��ˣ����������������û�����ͭ���й����������������ᣬ���˼��õ�����ͭ����Һ2ΪFeSO4������Һ1�ϲ�����Ũ������ȴ�ᾧ�õ��̷���
(1)ͼ�в�����Ϊ���ˣ�������Ϊ����Ũ������ȴ�ᾧ��
(2)�Լ�XΪFe���������漰�����ӷ�Ӧ����ʽΪFe + 2H+ = Fe2+ + H2����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̪���ҹ������з���һ���������Ƽ���ȱѪ���������ҩ���ϳɶ���̪(J)��һ��·�����£�
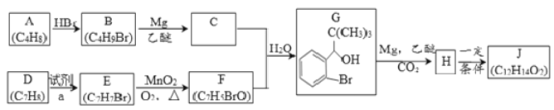
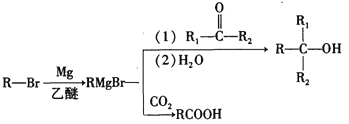
��֪��
(1) D����E�ķ�Ӧ����Ϊ________��
(2) F�Ĺ���������Ϊ________��
(3) E�ĺ�����ͬ���칹�干��________ ��(��E)��
(4) J��һ�����������г����������һ����Ԫ����J�Ľṹ��ʽΪ________ ��H��һ�������»������ɸ߷��ӻ�����K��H����K�Ļ�ѧ����ʽΪ________��
(5) �����}������д������ȩ�ͱ�Ϊԭ�ϣ��ϳ�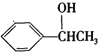 ��·������ͼ(�����Լ���ѡ)��
��·������ͼ(�����Լ���ѡ)��
_______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA�ǰ����ӵ�������ֵ������˵����ȷ����
A. ���³�ѹ�£�11.2 LHCl�����к��еķ�����Ϊ0.5NA
B. ���³�ѹ�£�5.6 g N2��CO������������е�ԭ����Ϊ0.4NA
C. ��0.2 mol FeCl3�Ƴɽ��壬���ý���������Ϊ0.2NA
D. 50 mL12 mol/L����������Fe��Ӧ��ת�Ƶ�����Ϊ0.3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����±�������ѧ���ַ�����ijԪ�ص�һ��ԭ�ӣ�����ԭ�Ӻ�����161�����ӣ�������Ϊ272����Ԫ�ص�ԭ������Ϊ�� ��
A.111
B.161
C.272
D.433
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���Ľṹ��ʽ�ɱ�ʾΪ![]() �����й��ڸ����ʵ�˵������ȷ����(����)
�����й��ڸ����ʵ�˵������ȷ����(����)
A. �����������12��̼ԭ�Ӵ���ͬһƽ���� B. ������һ�ȴ�����4��
C. ������������10��̼ԭ�Ӵ���ͬһƽ���� D. �����Ǽױ���ͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ�Ĺ���Ԫ�ء�
��1����λ��Ԫ�����ڱ��õ�_____________�壬���̬ԭ����δ�ɶԵ��ӵĸ���Ϊ______��
��2��[Fe(H2NCONH2)]6(NO3)3�������������������غ���������һ����Ҫ�������û�������Fe3+�ĺ�������Ų�ʽΪ____________________�������ǽ���Ԫ�صĵ縺���ɴ�С��˳����____________________��
��3�����ط����С�̼ԭ��Ϊ________�ӻ��������ЦҼ���м�����Ŀ֮��Ϊ____________________��
��4��FeO������NaCl����ṹ���ƣ��Ƚ�FeO��NaCl�ľ����ܴ�С������Ҫ֪����������______��
��5��Co(NH3)5BrSO4���γ������ܵ������ṹ�ֱ�Ϊ[Co(NH3)5Br]SO4��[Co(SO4)(NH3)5]Br����֪Co3������λ����6��Ϊȷ���ܵ������Ľṹ���ֶ�����������������ʵ�飺�ڵ�һ���������Һ�м���������Һ������ɫ�������ڵڶ����������Һ�м�����������Һ��������ɫ��������ڶ�������������Ϊ____________________��
��6����������̼�ܽ��ڦã�Fe���γɵ�һ�ּ�϶�����壬���ԣ��侧��Ϊ���������ṹ������ͼ��ʾ��������ʵĻ�ѧʽΪ____________________���������ܶ�Ϊdg��cm3���������������̼ԭ�ӵľ���Ϊ____________________pm������٤��������ֵ��NA��ʾ��д����ļ���ʽ���ɣ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ���������ֵ��������������ȷ����
A. 1mol NH3�����е�ԭ����ΪNA
B. ���³�ѹ�£�22.4L����������ԭ����Ϊ2NA
C. ���³�ѹ�£�14 g ��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪNA
D. 1 L 0.1mol��LNaCl��Һ��������Na+ ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����գ�
(1)��֪4.5g��X����������������ԼΪ9.03��1022����������Ħ������Ϊ___________����״�������Ϊ_______________��
(2)��״���£���CO��CO2��ɵ�6.72L������������Ϊ9.6g���˻������CO��CO2�����ʵ���֮��Ϊ_________���û��������ܶ�����ͬ״���������ܶȵ�___________����

(3)ij���Ľṹʾ��ͼ��ͼ��ʾ����x��y < 10ʱ��������______________ (ѡ����������������������������ԭ����) ����y��1������ԭ��M��y��6������ԭ��N����ʱ���γɻ�����Ļ�ѧʽΪ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ����ֳЭ����������һ�����õ绯ѧԭ�����������ˮ�ʵķ�������װ����ͼ��ʾ��
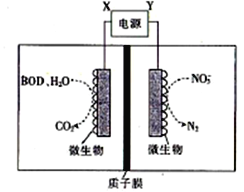
����˵���������
A. XΪ��Դ����
B. ����װ���ڸ����½�������Ч�ʽ�����
C. ��BODΪ������(C6H12O6)����1mol�����DZ���ȫ����ʱ�������ϵ缫������24mole-
D. ����1molNO3-����ԭ������6molH+ͨ������ĤǨ����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com