
【题目】(1)元素周期表体现了元素周期律,即元素的性质随着_________的递增呈现___________的变化。
(2)元素周期表前四周期元素中失电子能力最强的元素是___________(填元素符号,下同),得电子能力最强的元素是___________。
(3)短周期元素X、Y、Z在周期表中的位置关系如图所示,则
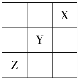
①Y、Z元素的气态氢化物的稳定性__________>__________(填化学式)。
②三种元素形成的单质中熔点最高的是___________(填化学式)。
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下1molC3H8发生如下反应:①C3H8→C2H4+CH4②C3H8→C3H6+H2如果C3H8的转化率为80%,且混合气体中m(CH4)=m(H2),则下列说法正确的是( )
A. 反应后混合气体的平均相对分子质量为35.2
B. 两种烯烃物质的量之比,即n(C2H4)/n(C3H6)为1∶1
C. 将混合气体通入溴的四氯化碳溶液,溶液增重128g
D. 两种烯烃物质的量之和,即n(C2H4)+n(C3H6)为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙是某同学设计的两套制取二氧化碳的发生装置,对两套装置分析正确的是

A. 此时甲装置中的止水夹M处于打开状态
B. 甲装置气体导出过程中容器内外气压相等
C. 甲装置不具有启普发生器的功能
D. 乙装置N处添加止水夹可以与甲装置具有相同功能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表有个横行,叫周期,每一周期中元素原子的相同,元素周期表中有列,第ⅥA族处在第列,同一主族从上到下,元素的非金属性依次(填增强或减弱).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以用离子方程式2H++CO32﹣=H2O+CO2↑来表示的化学反应是( )
A.硝酸和碳酸氢钠溶液的反应
B.稀硫酸和碳酸钾溶液的反应
C.醋酸和碳酸钠溶液的反应
D.盐酸和碳酸钡溶液的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL 0.200 0 mol/LNH4Cl溶液中逐滴加入0.2000 mol/LNaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。下列说法正确的是
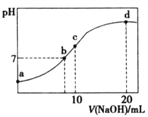
A. a点溶液中:c(H+)+c(NH3·H2O)=c(OH-)+c(NH4+)
B. b点溶液中:c(Cl-)=c(Na+)>c(H+)=c(OH-)
C. c点溶液中:c(NH3·H2O)+ c(NH4+)= c(Cl-)+ c(OH-)
D. d点溶液中:c(Cl-)> c(NH3·H2O)> c(OH-)> c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表回答问题:
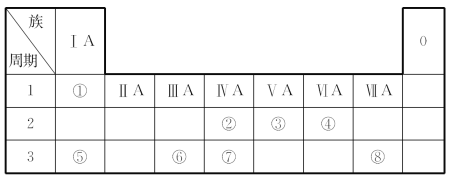
(1)元素⑦在周期表中的位置是___________________。
(2)元素①和⑤的原子序数相差 。
(3)写出元素⑤形成的常见化合物与元素⑧形成的单质反应的化学方程式________________。
(4)写出元素③形成的不同化合价的化合物的化学式(写出四个)________________________,
其中能与元素⑥形成的单质反应的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是人们最近提出的一个新概念,主要内容之一是指从技术、经济上设计可行的化学反应,尽可能减少对环境的负作用。下列化学反应符合绿色化学概念的是( )
A.制CuSO4:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
B.制CuSO4:2Cu+O2![]() 2CuO;CuO+H2SO4(稀)===CuSO4+H2O
2CuO;CuO+H2SO4(稀)===CuSO4+H2O
C.制Cu(NO3)2:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
D.制Cu(NO3)2:Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com