
【题目】以粉煤灰(主要含3Al2O3·2SiO2、SiO2,还含有少量CaO、Fe2O3等物质)为原料制取Al2O3的流程如图:
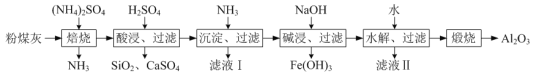
(1)当(NH4)2SO4和3Al2O3·2SiO2的配比a(a=![]() )不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=___时,3Al2O3·2SiO2的利用率最高。
)不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=___时,3Al2O3·2SiO2的利用率最高。
(2)“沉淀、过滤”所得滤渣为Fe(OH)3和Al(OH)3,生成Fe(OH)3的离子反应方程式为___。
(3)“碱浸”加入NaOH发生反应的离子方程式为___。
(4)“水解、过滤”可得到Al(OH)3沉淀,升高温度有利于水解的原因是___。该步骤可将加水改成通入过量的___气体。
(5)流程中,可以回收并循坏利用的物质除NH3外,还有___和___。
【答案】8 Fe3++3NH3+3H2O=Fe(OH)3↓+3NH4+ OH-+Al(OH)3=AlO2-+2H2O 水解为吸热反应,升高温度有利于平衡正向进行 CO2 NaOH (NH4)2SO4
【解析】
粉煤灰、(NH4)2SO4进行灼烧处理,把3Al2O3·2SiO2转化为NH4Al (SO4)2,且当(NH4)2SO4和3Al2O3·2SiO2的配比a(a=![]() )不同时各产物含量不同,如图a=8时,体系中NH4Al (SO4)2含量最高,此时3Al2O3·2SiO2的利用也率最高。加硫酸进行酸浸,过滤,滤液中含有Al3+、Fe3+以及其他可溶性离子,通入氨气生成沉淀Al(OH)3和Fe(OH)3,滤液Ⅰ为(NH4)2SO4,加入氢氧化钠进行碱浸取过滤,滤渣为Fe(OH)3滤液Ⅱ为NaOH 和NaAlO2,加水水解得到Al(OH)3沉淀,煅烧得氧化铝。
)不同时各产物含量不同,如图a=8时,体系中NH4Al (SO4)2含量最高,此时3Al2O3·2SiO2的利用也率最高。加硫酸进行酸浸,过滤,滤液中含有Al3+、Fe3+以及其他可溶性离子,通入氨气生成沉淀Al(OH)3和Fe(OH)3,滤液Ⅰ为(NH4)2SO4,加入氢氧化钠进行碱浸取过滤,滤渣为Fe(OH)3滤液Ⅱ为NaOH 和NaAlO2,加水水解得到Al(OH)3沉淀,煅烧得氧化铝。
(1)根据分析,当(NH4)2SO4和3Al2O3·2SiO2的配比a=8时,体系中NH4Al (SO4)2含量最高,此时3Al2O3·2SiO2的利用也率最高。
(2)通入氨气“沉淀、过滤”所得滤渣为Fe(OH)3和Al(OH)3,生成Fe(OH)3离子反应方程式:Fe3++3NH3+3H2O=Fe(OH)3↓+3NH4+;
(3)根据分析,“碱浸”加入NaOH发生反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O;
(4)“水解、过滤”可得到Al(OH)3沉淀,水解过程是吸热的,升高温度促进AlO2-水解;该步骤可将加水改成通入过量的酸性气体二氧化碳(CO2+AlO2-+2H2O= HCO3- +Al(OH)3↓);
(5)流程中,滤液Ⅰ为(NH4)2SO4,滤液Ⅱ含有NaOH ,故可以回收并循坏利用的物质除NH3外,还有(NH4)2SO4和NaOH。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态S原子电子占据最高能级的电子云轮廓图为__________形。
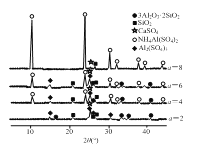
(2)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为________。
(3)气态三氧化硫以单分子形式存在,其分子的立体构型为__________形,其中共价键的类型有__________种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为__________。
(4)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为____________g/cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为__________nm。
所形成的正八面体的体心,该正八面体的边长为__________nm。
晶胞有两个基本要素:
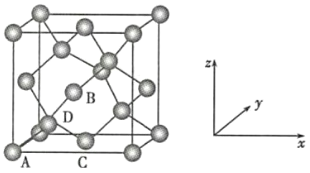
(6)晶胞的一个基本要素:原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为__________。
,0)。则D原子的坐标参数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“![]() ”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是无色具有水果香味的液体,沸点为77.2 ℃,实验室某次制取乙酸乙酯用醋酸14.3 mL、95%乙醇23 mL,还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合的氯化钙溶液。主要装置如图所示:
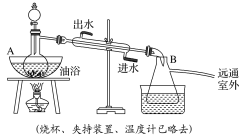
实验步骤:
①先向A中的蒸馏烧瓶中注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙醇和冰醋酸注入分液漏斗里待用。这时分液漏斗里醋酸和乙醇的物质的量之比约为5∶7。
②加热油浴保温约135~145 ℃。
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,调节加入速率使蒸出酯的速率与进料速率大体相等,直到加料完成。
④保持油浴温度一段时间,至不再有液体馏出后,停止加热。
⑤取下B中的锥形瓶,将一定量饱和Na2CO3溶液分批少量多次地加到馏出液里,边加边振荡,至无气泡产生为止。
⑥将⑤的液体混合物分液,弃去水层。
⑦将饱和CaCl2溶液(适量)加入分液漏斗中,振荡一段时间后静置,放出水层(废液)。
⑧分液漏斗里得到的是初步提纯的乙酸乙酯粗品。
试回答:
(1)实验中浓硫酸的主要作用是_____。
(2)用饱和Na2CO3溶液洗涤粗酯的目的是______。如果用NaOH溶液代替Na2CO3溶液将引起的后果是____。
(3)用饱和CaCl2溶液洗涤粗酯的目的是_____。
(4)在步骤⑧所得的粗酯里还含有的杂质是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将NO2和O2的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同压下),则原混合气体中氧气的体积为( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铜片(含少量杂质铁)为原料制取Cu(NO3)2溶液的实验流程如图:

(1)“酸洗”的目的是除去铜片表面难溶的Cu2(OH)2SO4,写出“酸洗”时反应的离子方程式:___。
(2)“水洗”后检验铜片表面是否洗涤干净的方法是___。
(3)“酸溶”时的装置如图所示,烧杯内所发生的反应为:
NO+NO2+2OH-=2NO2-+H2O
2NO2+2OH-=NO2-+NO3-+H2O

①“酸溶”时为防止反应过于剧烈,可以采取的方法有___和___。
②通入空气的作用是___、___。
(4)“调节pH=3~4,并保温3个小时”的目的是___。
(5)烧杯中所得溶液经多步处理得到NaNO3固体。设计以烧杯中所得溶液为原料,制取NaNO3固体的实验方案:___。
[已知3NaNO2+2HNO3=3NaNO3+2NO↑+H2O;NaNO3的溶解度随温度变化如图所示。实验中必须使用的试剂:硝酸和NaOH溶液]。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)熔点-54.1℃、沸点69.2℃,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。
(1)SO2Cl2中S的化合价为_______,SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为________________。
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(夹持装置未画出)。
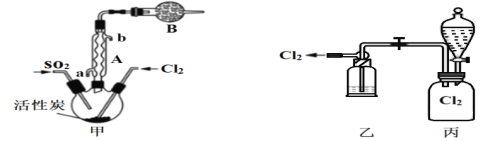
①仪器A的名称为___________,装置乙中装入的试剂_____________,装置B的作用是_______________________。
②装置丙分液漏斗中盛装的最佳试剂是________(选填字母)。
A.蒸馏水 B.10.0 mol/L浓盐酸
C.浓氢氧化钠溶液 D.饱和食盐水
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。
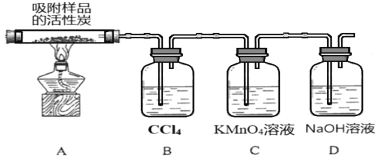
①加热时A中试管出现黄绿色,装置B的作用是 ____________。
②装置C中的现象是___________,反应的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃通过催化加氢后得到2-甲基丁烷,该烃不可能是( )
A. 3-甲基-1-丁炔B. 2-甲基-1-丁炔
C. 3-甲基-1-丁烯D. 2-甲基-1-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:Y+X→甲(g),Y+Z→乙(g)。甲为10电子分子,Z为黄绿色气体。甲、乙可化合生成离子化合物。
(1)X 的电子式是__________,甲的结构式是__________。实验室制备Z的化学方程式___________________。
(2)写出Y+X→甲的化学方程式___________________。
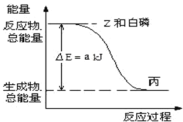
(3)已知常温下,![]() 为液体,
为液体,![]() 为固体。白磷
为固体。白磷![]() 在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
已知1mol白磷固体和Z气体反应,生成固态丁时,放热b kJ,则1mol固态丁转化为液态丙时的反应热![]() _____。
_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com