
【题目】在一定条件下,将NO2和O2的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同压下),则原混合气体中氧气的体积为( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A.①②B.②③C.③④D.①④
【答案】D
【解析】
根据NO2和O2混合气体倒立于水槽中可能发生的化学反应,若12 mL气体都是NO2,根据化学反应:3NO2+2H2O=2HNO3+NO,剩余气体为4mL,反应后剩余2 mL气体,可知有氧气过量和二氧化氮过量的两种情况;当氧气过量时,化学方程式为:4NO2+O2+2H2O=4HNO3,根据反应系数,可知氧气的体积;当二氧化氮过量时,则剩余气体是一氧化氮,反应方程式为4NO2+O2+2H2O=4HNO3和3NO2+H2O=2HNO3+NO,据此分析。
若氧气过量,则剩余2mL无色气体为氧气,设参加反应的氧气的体积为x,则有:![]()
4x+x=12mL-2mL=10mL,解得:x=2mL
原混合气体中氧气的体积为:2mL+2mL=4mL;
若NO2过量,则剩余2mL无色气体为NO,设氧气的体积为y,![]()

![]() ,解得:y=1.2mL,即原混合物中含有1.2mL氧气。
,解得:y=1.2mL,即原混合物中含有1.2mL氧气。
答案选D。


科目:高中化学 来源: 题型:
【题目】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
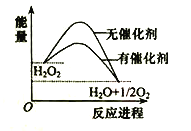
A. 加入催化剂,减小了反应的热效应
B. 加入催化剂,可提高H2O2的平衡转化率
C. H2O2分解的热化学方程式:H2O2 → H2O + O2 + Q
D. 反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是
A.食物中的营养物质主要包括:糖类、油脂、蛋白质、维生素、无机盐和水
B.燃烧相同体积的管道煤气(主要成分CO和H2)和天然气,管道煤气消耗氧气体积大
C.油脂没有固定的熔沸点,是食物中产生能量最高的营养物质
D.金属钠和碳酸钠溶液都可以用来区分乙醇、乙酸和苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:
2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:

(1)写出下列物质的官能团名称:B:____________________;D:____________________。
(2)反应④的化学方程式为________________________________________________,反应类型:________。
(3)某学习小组设计物质B催化氧化的实验装置如下,根据图2装置回答问题。

①装置甲锥形瓶中盛放的固体药品可能为________(填字母)。
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_______________________________。
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用下图装置探究草酸亚铁晶体(FeC2O4·2H2O)的分解产物,下列说法错误的是
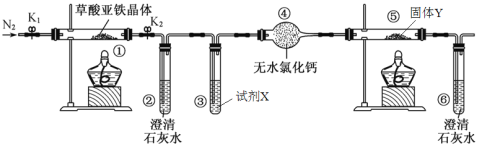
A. 实验前通入N2的作用是排出装置内的空气
B. ②、⑥中澄清石灰水的作用均是为了检验CO2气体
C. 装置中试剂X为NaOH溶液,固体Y为CuO固体
D. 将①中所得固体溶于KSCN溶液,可以检验其中铁元素的化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
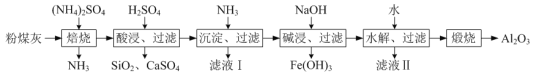
【题目】以粉煤灰(主要含3Al2O3·2SiO2、SiO2,还含有少量CaO、Fe2O3等物质)为原料制取Al2O3的流程如图:
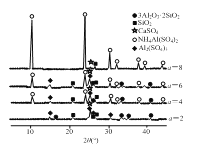
(1)当(NH4)2SO4和3Al2O3·2SiO2的配比a(a=![]() )不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=___时,3Al2O3·2SiO2的利用率最高。
)不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=___时,3Al2O3·2SiO2的利用率最高。
(2)“沉淀、过滤”所得滤渣为Fe(OH)3和Al(OH)3,生成Fe(OH)3的离子反应方程式为___。
(3)“碱浸”加入NaOH发生反应的离子方程式为___。
(4)“水解、过滤”可得到Al(OH)3沉淀,升高温度有利于水解的原因是___。该步骤可将加水改成通入过量的___气体。
(5)流程中,可以回收并循坏利用的物质除NH3外,还有___和___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家开发出了多种太阳能电池,除晶体硅太阳能电池外,还有GaAs太阳能电池、铜铟镓硒薄膜太阳能电池等。
(1)基态Ga原子的电子排布式为________。
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因________________。
(3)H2Se分子的键角_______H2O分子的键角(选填“>”、“=”或“<”)。写出与SeO3互为等电子体的一种阴离子_____________(写化学式)。
(4) AsF3分子的立体构型为__________;AsF3是极性分子,理由是_________________。
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有__________________。
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:
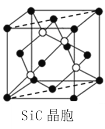
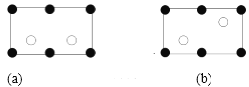
金刚砂中硅原子的杂化轨道类型为_______,沿晶胞图中虚线方向的切面图为__________(填标号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时NO(g)和O2(g)反应生成NO2(g)的体系中,n(NO)随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为________。
(2)如图中表示O2变化曲线的是________,用O2表示从0~2s内该反应的平均速率v=________。
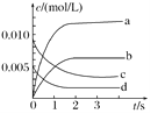
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内气体总质量保持不变
c.v逆(NO)=2v正(O2) d.容器内气体密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,固定容积的密闭容器中发生反应A(g)+3B(g)![]() 2C(g)+2D(s),下列叙述不是反应达到平衡状态标志的是( )
2C(g)+2D(s),下列叙述不是反应达到平衡状态标志的是( )
①2υ正(B)=3υ逆(C) ②单位时间内生成amol A,同时生成3amol B
③A、B、C的浓度不再变化 ④混合气体密度不随时间变化而变化
⑤混合气体的总压强不再变化 ⑥密闭容器中C的体积分数不变
⑦单位时间内消耗amol A,同时生成3amol B ⑧A、B、C、D的分子数之比为1∶3∶2∶2
A.②⑧B.②⑤⑧C.①③④⑦D.②⑤⑥⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com