
【题目】在一定温度下,固定容积的密闭容器中发生反应A(g)+3B(g)![]() 2C(g)+2D(s),下列叙述不是反应达到平衡状态标志的是( )
2C(g)+2D(s),下列叙述不是反应达到平衡状态标志的是( )
①2υ正(B)=3υ逆(C) ②单位时间内生成amol A,同时生成3amol B
③A、B、C的浓度不再变化 ④混合气体密度不随时间变化而变化
⑤混合气体的总压强不再变化 ⑥密闭容器中C的体积分数不变
⑦单位时间内消耗amol A,同时生成3amol B ⑧A、B、C、D的分子数之比为1∶3∶2∶2
A.②⑧B.②⑤⑧C.①③④⑦D.②⑤⑥⑧
【答案】A
【解析】
对于A(g)+3B(g)![]() 2C(g)+2D(s);
2C(g)+2D(s);
①不同物质表示的正逆反应速率之比等于化学计量数之比,可逆反应到达平衡状态,2υ正(B)=3υ逆(C),即υ正(B):υ逆(C)=3:2,说明到达平衡,①是反应达到平衡状态标志,故不选①;
②单位时间内a mol A生成,同时生成3a mol B,在任何情况下都成立,②不是反应达到平衡状态标志,故选②;
③A、B、C的浓度不再变化,说明达到平衡状,③是反应达到平衡状态标志,故不选③;
④混合气体密度不再变化,说明达到平衡状态,④是反应达到平衡状态标志,故不选④;
⑤达到平衡后,A、B、C气体的物质的量及体积不再随时间的变化而变化,故混合气体的总压强不再变化,⑤是反应达到平衡状态标志,故不选⑤;
⑥未达到平衡状态时,混合气体的体积分数是发生变化的,若混合气体的体积分数不再变化,说明达到了平衡状态,⑥是反应达到平衡状态标志,故不选⑥;
⑦单位时间消耗a mol A,反映的是正反应速率,同时生成3a mol B,反映的是逆反应速率,且化学反应速率之比等于化学计量数之比,故正逆反应速率相等,说明达到平衡状态,⑦是反应达到平衡状态标志,故不选⑦;
⑧平衡时各物质的量之比取决于物质的起始物质的量和转化率,故A、B、C、D的分子数之比不一定为1∶3∶2∶2,不能判断反应是否平衡,⑧不是反应达到平衡状态标志,故选⑧;
故本题选A。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,将NO2和O2的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同压下),则原混合气体中氧气的体积为( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
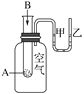
(1)该反应________(填“放出”或“吸收”)热量。
(2)如图能正确表示该反应中能量变化的是___________。
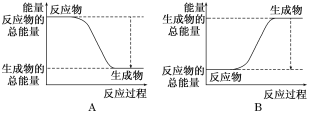
(3)写出一个符合题中条件的化学方程式:_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固定容积的密闭容器中进行如下反应:2SO2(g)+O2(g)![]() 2SO3(g),已知反应过程中某一刻SO2、O2、SO3浓度分别为0.2mol/L、0.2mol/L、0.2mol/L,达到平衡时浓度可能是( )
2SO3(g),已知反应过程中某一刻SO2、O2、SO3浓度分别为0.2mol/L、0.2mol/L、0.2mol/L,达到平衡时浓度可能是( )
A.SO2、O2分别为0.4mol/L、0.3mol/L
B.O2为0.05mol/L
C.SO2、SO3浓度均为0.15mol/L
D.SO2为0.24mol/L、SO3为0.16mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中充有2molSO2和一定量的O2,发生反应2SO2(g)+O2(g)![]() 2SO3(g)。当反应进行到4min时,测得此时SO2为0.4mol,则2min时密闭容器中SO3的物质的量为( )
2SO3(g)。当反应进行到4min时,测得此时SO2为0.4mol,则2min时密闭容器中SO3的物质的量为( )
A.1.6molB.1.2molC.大于1.6molD.小于1.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:Y+X→甲(g),Y+Z→乙(g)。甲为10电子分子,Z为黄绿色气体。甲、乙可化合生成离子化合物。
(1)X 的电子式是__________,甲的结构式是__________。实验室制备Z的化学方程式___________________。
(2)写出Y+X→甲的化学方程式___________________。
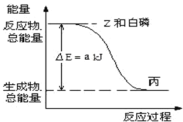
(3)已知常温下,![]() 为液体,
为液体,![]() 为固体。白磷
为固体。白磷![]() 在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
已知1mol白磷固体和Z气体反应,生成固态丁时,放热b kJ,则1mol固态丁转化为液态丙时的反应热![]() _____。
_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1:1。请回答:
(1)组成A分子的原子的核外电子排布式是________________;
(2)B的分子式分别是 ___________;C分子的立体结构呈_________ 形,该分子属于_____________分子(填“极性”或“非极性”);
(3)向D的稀溶液中加入少量氯化铁溶液,反应的化学方程式为_____________________________
(4) 若将1molE在氧气中完全燃烧,只生成1molCO2和2molH2O,则E的分子式是 __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A是制取溴苯的实验装置,B、C是改进后的装置。请仔细分析,对比三个装置,回答下列问题:


(1)写出三个装置中发生反应的主要化学方程式:________________。写出B中右边试管中所发生反应的化学方程式:__________________。
(2)装置A和C均采用了长玻璃导管,其作用是_______、____________。
(3)在实验B、C装好仪器及药品后要使反应开始,应对装置B进行的操作是________________;应对装置C进行的操作是_______________________。
(4)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是_________________。
(5)B中采用了洗气瓶吸收装置,其作用是______________________,反应后洗气瓶中可能出现的现象是_______________。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是_____________________;_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学用图所示装置制取氨,并探究其性质。
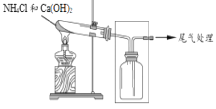
(1)制取氨气的化学方程式是______。
(2)采用图示的方法收集氨气,是因为氨气的密度比空气 ______(填“大”或“小”)。
(3)将蘸有浓盐酸的棉球放在玻璃片上,用集满NH3的集气瓶扣住棉球,可观察到的现象是______。
(4)甲同学设计了下图所示的装置进行尾气处理,乙同学认为该设计不合理,请画出正确的尾气吸收图______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com