
【题目】测定硫酸铜晶体中结晶水含量的实验中,下列哪个仪器是不需要的
A. 蒸发皿 B. 研钵 C. 干燥器 D. 坩埚
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】对于反应A+B =C,下列条件的改变一定能使化学反应速率加快的是
A. 增加A的物质的量B. 升高体系的温度
C. 减少C的物质的量D. 增加体系的压强
查看答案和解析>>
科目:高中化学 来源: 题型:
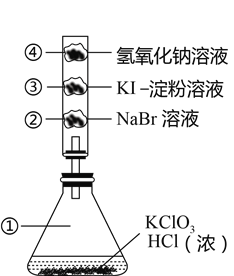
【题目】已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内分别装有滴有不同溶液的白色棉球,反应一段时间后,对图中指定部分颜色描述正确的是( )
选项 | ① | ② | ③ | ④ |
A | 黄绿色 | 白色 | 紫色 | 白色 |
B | 黄绿色 | 橙色 | 紫色 | 黄绿色 |
C | 黄绿色 | 橙色 | 蓝色 | 白色 |
D | 黄绿色 | 橙色 | 蓝色 | 黄绿色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素。其相关信息如下
元素 | 相关信息 |
A | A原子的1s 轨道上只有l 个电子 |
B | B是电负性最大的元素 |
C | C的基态原子2p轨道中有三个未成对电子 |
D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答下列问题:
(1)写出E元素原子基态时的电子排布式__。
(2)C元素的第一电离能比氧元素的第一电离能_____(填“大”或“小”)。
(3)CA3分子中C原子的杂化轨道类型是__。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有_____(填序号)。
① 配位键 ② 金属键 ③ 极性共价键 ④非极性共价键 ⑤ 离子键 ⑥ 氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______(填字母)
a.平面正方形 b.正四面体 c.三角锥形 d. V 形
(5)B与D可形成离子化合物,其晶胞结构如下图所示。其中D离子的配位数为____, 若该晶体的密度为ag/cm3,则B与D间最短距离是______cm (写出表达式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用氟碳铈矿(主要成分CeCO3F)提取CeCl3的一种工艺流程如下:

请回答下列问题:
(1)CeCO3F中,Ce元素的化合价为_______。
(2)酸浸过程中用稀硫酸和H2O2替换HCl不会造成环境污染。写出稀硫酸、H2O2与CeO2反应的离子方程式:____________。
(3)向Ce(BF4)3为中加入KCl溶液的目的是_________。
(4)若溶液中的Ce3+沉淀完全,此时溶液的pH为_______(己知Ksp[Ce(OH)3]=1×10-20)
(5)加热CeCl3·6H2O和NH4Cl的固体混合物可得到无水CeCl3,其中NH4Cl的作用是________。
(6)准确称取0.7500g CeCl3样品置于锥形瓶中,加入适量过硫酸铵[(NH4)2S2O8]溶液将Ce3+氧取化为Ce4+,然后用0.1000mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗25.00mL标准溶液.(己知:Fe2++Ce4+= Ce3++Fe3+)
①已知:过二硫酸的结构式为![]() ,其中S元素的化合价为:______。 过硫酸铵[(NH4)2S2O8]溶液将Ce3+氧化为Ce4+的离子方程式为:_____________。
,其中S元素的化合价为:______。 过硫酸铵[(NH4)2S2O8]溶液将Ce3+氧化为Ce4+的离子方程式为:_____________。
②该样品中CeCl3的质量分数为____________。
③若使用久置的(NH4)2Fe(SO4)2标准溶液进行滴定,测得该CeCl3样品的质童分数将______ (填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F原子序数依次增大.A的阳离子就是一个质子:B原子的最外层电子数是所在周期数的2倍;C、D在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体:E与A同一主族:F原子的K、L层电子数之和比K、M层电子数之和多l。A、D、E三种元素可形成化合物甲,B、D、E三种元素可形成化合物乙。请回答:
(1)C2的结构式为_______________。
(2)由上述元素组成的既含极性健又含非极性键的无机化合物分子的电子式为__________。
(3)A的单质与D的单质在强酸性条件下构成燃料电池,其正极反应式为__________。
(4)常温下,甲与乙的水溶液pH均为9,这两种溶液中由水电离出的OH-的物质的量浓度c(OH -)甲:c(OH-)乙= ________。
(5)将2.4gB的单质在足量D的单质中燃烧,所得气体通入1L 0.3mol/L的甲溶液中,完全吸收后,溶液中的溶质为______。溶液中所含离子的物质的量 浓度由大到小的顺序为______。
(6)由A、B、C、D四种元素组成的无机酸的酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应进行到一定程度会达到化学平衡状态,如K2Cr2O7溶液中存在平衡:Cr2![]() (橙色)+H2O
(橙色)+H2O![]() 2Cr
2Cr![]() (黄色)+2H+。平衡时各种物质含量保持不变,达到一种相对的静止(如平衡时,每消耗1molH2O同时也会生成1molH2O)。外界条件改变时,平衡状态会被破坏而发生移动(如消耗的水多于生成的水,则平衡向正向移动),平衡移动符合勒夏特列原理,即如果改变可逆反应的条件(如浓度、压强、温度等),化学平衡就被破坏,并向减弱这种改变的方向移动。现在用K2Cr2O7溶液进行下列实验:
(黄色)+2H+。平衡时各种物质含量保持不变,达到一种相对的静止(如平衡时,每消耗1molH2O同时也会生成1molH2O)。外界条件改变时,平衡状态会被破坏而发生移动(如消耗的水多于生成的水,则平衡向正向移动),平衡移动符合勒夏特列原理,即如果改变可逆反应的条件(如浓度、压强、温度等),化学平衡就被破坏,并向减弱这种改变的方向移动。现在用K2Cr2O7溶液进行下列实验:

已知:C2H5OH遇到氧化剂容易被氧化。
结合实验,下列说法不正确的是 ( )
A. ①中溶液橙色加深,③中溶液变黄 B. ②中Cr2![]() 被C2H5OH还原
被C2H5OH还原
C. 对比②和④可知K2Cr2O7酸性溶液氧化性弱 D. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com