
| A、0.16 | B、0.08 |
| C、0.04 | D、0.02 |
 2HI(g)
2HI(g)| C 2(HI) |
| C(H 2)C(I 2) |
| 0.16 2 |
| 0.02×0.02 |
 2HI(g)
2HI(g)| 2(0.20-x)×2(0.20-x) |
| x×x |


科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
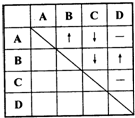 为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成.).
为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成.).查看答案和解析>>
科目:高中化学 来源: 题型:
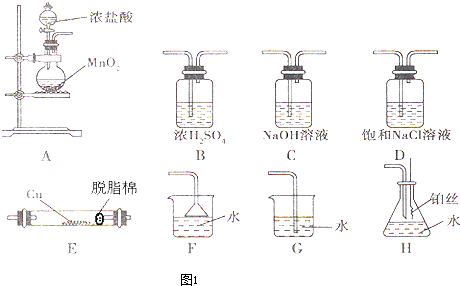
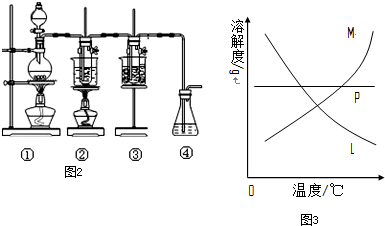
查看答案和解析>>
科目:高中化学 来源: 题型:
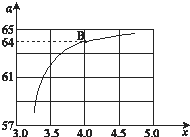 工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下:| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①②④ |
| C、①②④⑤ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)在一定条件下,在水溶液中 1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)的相对大小如图所示.
(1)在一定条件下,在水溶液中 1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)的相对大小如图所示.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(HF) |
| c(H+).c(F-) |
| c(HF) |
| A、①③④ | B、②③④ |
| C、③④⑤ | D、②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4干燥 |
| ①足量饱和NaHCO3溶液 |
| ②浓H2SO4干燥 |
A、x=
| ||
B、y=
| ||
| C、x=y | ||
D、y=
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com