
【题目】高能LiFePO4电池多应用于公共交通,结构如图所示。电池中间是聚合物的隔膜,其主要作用是在反应过程中只让Li+通过,原理如下:(1x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC。下列说法错误的是( )
LiFePO4+nC。下列说法错误的是( )

A.放电时,Li+向正极移动
B.放电时,电子由负极→用电器→正极
C.充电时,阴极反应为xLi++nC+xe-=LixCn
D.充电时,阳极质量增重
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】T℃时,在20.00mL0.10mol·L-1的一元酸HR溶液中滴入0.10mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。
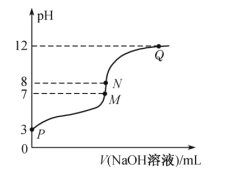
下列说法不正确的是( )
A..T℃时,HR电离常数Ka≈1.0×10-5
B.M点对应的NaOH溶液体积为20.00mL
C.N点与Q点所示溶液中水的电离程度:N>Q
D.M点所示溶液中c(Na+)=c(R-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理锂离子二次电池正极废料铝钴膜(含有LiCoO2、Al等)的一种工艺如下:

下列有关说法不正确的是
A. 碱浸的目的是溶解铝B. 酸溶时H2 O2被还原
C. H2SO4/H2O2可改用浓盐酸D. 铝、钴产物可再利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,a L密闭容器中放入1molN2和3molH2发生N2+3H2![]() 2NH3的反应,下列选项中能说明反应已达到平衡状态的是
2NH3的反应,下列选项中能说明反应已达到平衡状态的是
A.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
B.2v(H2)=3v(NH3)
C.单位时间内1个N≡N键断裂的同时,有6个N-H键断裂
D.单位时间消耗0.1molN2的同时,生成0.2molNH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学习小组的同学设计实验,制备(NH4)2Fe(SO4)26H2O并探究其分解规律。实验步骤如下:
Ⅰ.称取7.0g工业废铁粉放入烧杯中,先用热的Na2CO3溶液洗涤,再水洗,最后干燥。
Ⅱ.称取6.0g上述处理后的铁粉加入25mL某浓度硫酸中加热,加热过程中不断补充蒸馏水,至反应充分。
Ⅲ.冷却、过滤并洗涤过量的铁粉,干燥后称量铁粉的质量。
Ⅳ.向步骤Ⅲ的滤液中加入适量(NH4)2SO4晶体,搅拌至晶体完全溶解,经一系列操作得干燥纯净的(NH4)2Fe(SO4)26H2O。
V.将(NH4)2Fe(SO4)26H2O脱水得(NH4)2Fe(SO4)2,并进行热分解实验。
已知在不同温度下FeSO47H2O的溶解度如表:
温度(℃) | 1 | 10 | 30 | 50 |
溶解度(g) | 14.0 | 17.0 | 25.0 | 33.0 |
回答下列问题:
(1)步骤Ⅰ用热的Na2CO3溶液洗涤工业废铁粉的目的是__,步骤Ⅱ中设计铁粉过量,是为了__,加热反应过程中需不断补充蒸馏水的目的是__。
(2)步骤Ⅲ中称量反应后剩余铁粉的质量,是为了__。
(3)(NH4)2Fe(SO4)2分解的气态产物可能有N2、NH3、SO2、SO3及水蒸气,用下列装置检验部分产物。

①检验气态产物中的SO2和SO3时,装置连接顺序依次为__(气流从左至右);C中盛放的试剂为__。
②装置A的作用是__。
③检验充分分解并冷却后的瓷舟中铁的氧化物中是否含有二价铁,需用到的试剂为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,二氧化碳可合成低碳烯烃,缓解温室效应、充分利用碳资源。
(1)已知:①C2H4(g)+2O2(g)=2CO2(g)+2H2(g) ΔH1
②2H2(g)+O2(g)=2H2O(1) ΔH2
③H2O(1)=H2O(g) ΔH3
④2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH4
C2H4(g)+4H2O(g) ΔH4
则ΔH4=___(用ΔH1、ΔH2、ΔH3表示)。
(2)反应④的反应温度、投料比[![]() =x]对CO2平衡转化率的影响如图所示。
=x]对CO2平衡转化率的影响如图所示。
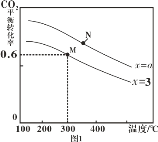
①a__3(填“>”、“<”或“=”);M、N两点反应的平衡常数KM__KN(填填“>”、“<”或“=”)
②M点乙烯体积分数为__;(保留2位有效数字)
③300℃,往6L反应容器中加入3molH2、1molCO2,反应10min达到平衡。求0到10min氢气的平均反应速率为__;
(3)中科院兰州化学物理研究所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。
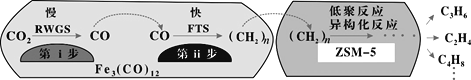
催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表。
助剂 | CO2转化率 (%) | 各产物在所有产物中的占比(%) | ||
C2H4 | C3H6 | 其他 | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
①欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加__助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是__;
②下列说法正确的是__;
a.第ⅰ步所反应为:CO2+H2![]() CO+H2O
CO+H2O
b.第ⅰ步反应的活化能低于第ⅱ步
c.催化剂助剂主要在低聚反应、异构化反应环节起作用
d.Fe3(CO)12/ZSM-5使CO2加氢合成低碳烯烃的ΔH减小
e.添加不同助剂后,反应的平衡常数各不相同
(4)2018年,强碱性电催化还原CO2制乙烯研究取得突破进展,原理如图所示。
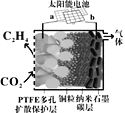
①b极接的是太阳能电池的__极;
②已知PTFE浸泡了饱和KCl溶液,请写出阴极的电极反应式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶胞是晶体结构中可重复出现的最小的结构单元,C60晶胞结构如下图所示,下列说法正确的是( )
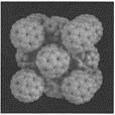
A. C60摩尔质量是720
B. C60与苯互为同素异形体
C. 在C60晶胞中有14个C60分子
D. 每个C60分子周围与它距离最近等距离的C60分子有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:
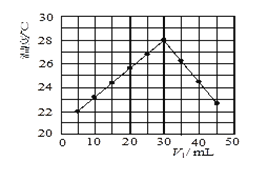
(1)研究小组做该实验时环境温度__________(填“高于”、“低于”或“等于”)22 ℃,判断的依据是____________
(2)由题干及图形可知,V1/V2=__________时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为___________mol/L。
(3)若通过实验测定及有关计算知此反应共放出Q kJ的热量,请写出此反应的热化学方程式:____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气含氮氧化物(NOX)、碳氢化合物(CXHY)、碳等,直接排放容易造成“雾霾”。因此,不少汽车都安装尾气净化装置(净化处理过程如图)。下列有关叙述,错误的是
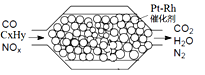
A. 尾气造成“雾霾”与汽油未充分燃烧有关
B. 尾气处理过程,氮氧化物(NOX)被还原
C. Pt-Rh催化剂可提高尾气净化反应的平衡转化率
D. 使用氢氧燃料电池作汽车动力能有效控制雾霾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com