
【题目】X、Y、Z、R、Q是五种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,X、Y、R最外层电子数之和为8,Q的单质为黄绿色有害气体。请回答下列问题:
(1)Z在元素周期表中的位置为________。
(2)Y和Z元素的原子半径由大到小的顺序为_____(写元素符号)。Y和Z的气态氢化物中稳定性较强的是_______(填化学式)
(3) Y单质的电子式为________,用电子式表示RQ2的形成过程__________
(4)X、Z两元素形成的原子个数比为1∶1的化合物中含有的化学键类型为________。
(5)Y的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式_______。
【答案】第二周期第ⅥA族 N > O H2O ![]()
![]() 极性键 非极性键 NH3 + HNO3 = NH4NO3
极性键 非极性键 NH3 + HNO3 = NH4NO3
【解析】
X是原子半径最小的元素,故X为氢元素;Y的气态氢化物能使湿润的红色石蕊试纸变蓝,故Y为氮元素;Z为地壳中含量最多的元素,故Z为氧元素;X、Y、R最外层电子数之和为8,则R最外层电子数为8-1-5=2,再根据X、Y、Z、R、Q是五种短周期元素,原子序数依次增大,确定R为Mg,Q的单质为黄绿色有害气体,故Q为氯元素。
总结上面X为氢元素、Y为氮元素、Z为氧元素、R镁元素、Q为氯元素;
(1)Z为氧元素,最外层6个电子,在元素周期表中的位置为第二周期第ⅥA族;
答案:第二周期第ⅥA族
(2)同一周期从左到右原子半径逐渐减小,非金属性增强,故氮原子半径大于氧原子半径;非金属性越强,气态氢化物越稳定,Y(NH3)和Z(H2O)的气态氢化物中稳定性较强的是H2O;
答案:N > O H2O
(3) Y单质为N2,两个氮原子之间存在三个共用电子对,电子式为![]() ,用电子式表示RQ2(MgCl2)的形成过程:
,用电子式表示RQ2(MgCl2)的形成过程:![]() ;
;
答案:![]()
![]()
(4)X、Z两元素形成的原子个数比为1∶1的化合物为H2O2,结构式为H-O-O-H,因此含有的化学键类型为极性键、非极性键;
答案:极性键 非极性键
(5)Y的气态氢化物(NH3)与其最高价氧化物对应的水化物(HNO3)反应化合成盐,化学方程式为NH3 + HNO3 = NH4NO3;
答案:NH3 + HNO3 = NH4NO3


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:
【题目】下列各组反应(表中物质均为反应物),反应刚开始时,放出H2的速率最大的是( )
A | Mg 0.1mol | 6mol· L—1硝酸10mL | 60℃ |
B | Mg 0.1mol | 3mol·L—1盐酸10mL | 60℃ |
C | Fe 0.1mol | 3mol·L—1盐酸10mL | 60℃ |
D | Mg 0.1mol | 3mol·L—1硫酸10mL | 60℃ |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用,如果设法提高化学反应的限度,下面的说法错误的是( )
A. 能够节约原料和能源 B. 能够提高产品的产量
C. 能够提高经济效益 D. 能够提高化学反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生反应:2HI(g)![]() H2(g)+I2(g),0~15 s内c(HI)由0.1 mol/L降到0.07 mol/L,则下列说法正确的是 ( )
H2(g)+I2(g),0~15 s内c(HI)由0.1 mol/L降到0.07 mol/L,则下列说法正确的是 ( )
A. 当HI、H2、I2浓度之比为2∶1∶1时,说明该反应达平衡
B. c(HI)由0.07 mol/L降到0.05 mol/L所需的反应时间小于10 s
C. 升高温度正反应速率加快,逆反应速率减慢
D. 0~15s内用I2表示的平均反应速率为:v(I2)=0.001 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当有人出现水杨酸反应(头痛、眩晕、恶心、耳鸣)时,医生可采取在静脉中注射下列( )
A.1.25%的NH4Cl溶液B.0.9%的NaHCO3溶液
C.70%的酒精D.10%的链霉素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是相同条件下N2的2倍。
(1)求该有机物的分子式。
(2)该有机物链状同分异构体的结构简式为: 。
(3)若在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,离子不存在。图为H3PO4(图中用H3A表示)在加入强酸或强碱溶液后,平衡时溶液中各微粒浓度的对数值(lgc)-pH图。下列说法不正确的是( )
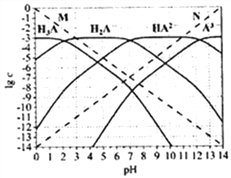
A. H3PO4、H2PO4-、HPO42-、PO43-不能在同一溶液中大量共存
B. H3PO4电离平衡常数Ka2≈1×10-7
C. 图中虚线M、N分别代表H+和OH-
D. pH=10时,溶液中存在关系:c(HPO42-)>c(OH-)>c(PO43-)>c(H2PO4-)>c(H3PO4)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A2(g)+3B2(g)===2C(g)来说,以下化学反应速率的表示中,反应速率最快的是( )
A. v(B2)=0.8 mol/(Ls)B. v(A2)=0.4 mol/(Ls)
C. v(C)=0.6 mol/(Ls)D. v(B2)=1 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)为紫黑色粉末,是一种新型高效消毒剂。K2FeO4易溶于水,微溶于浓KOH溶液,在0 ℃~5 ℃的强碱性溶液中较稳定。一般制备方法是先用Cl2与KOH溶液在20 ℃以下反应生成KClO(在较高温度下则生成KClO3),KClO再与KOH、Fe(NO3)3溶液反应即可制得K2FeO4。实验装置如图所示:
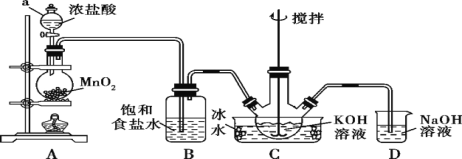
回答下列问题:
(1)制备KClO。
①仪器a的名称是________________;装置B吸收的气体是________。
②装置C中三颈烧瓶置于冰水浴中的目的是______________;装置D的作用是_____________。
(2)制备K2FeO4。
①装置C中得到足量KClO后,将三颈烧瓶上的导管取下,加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度,搅拌,当溶液变为紫红色,该反应的离子方程式为________________________________。
②向装置C中加入饱和________溶液,析出紫黑色晶体,过滤。
(3)测定K2FeO4纯度。测定K2FeO4的纯度可用滴定法,滴定时有关反应的离子方程式为:
a.FeO42-+CrO2-+2H2O═CrO42-+Fe(OH)3↓+OH-
b.2CrO42-+2H+═Cr2O72-+H2O
c.Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
称取2.0g制备的K2FeO4样品溶于适量KOH溶液中,加入足量的KCrO2,充分反应后过滤,滤液在250mL容量瓶中定容.取25.00mL加入稀硫酸酸化,用0.10 molL-1的(NH4)2Fe(SO4)2标准溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液的体积为24.00mL,则该K2FeO4样品的纯度为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com