
【题目】化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
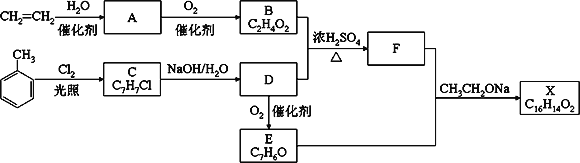
已知:RX![]() ROH;RCHO+CH3COOR’
ROH;RCHO+CH3COOR’![]() RCH=CHCOOR’ 请回答:
RCH=CHCOOR’ 请回答:
(1) A中官能团的名称是______________________。
(2) B +D→F的化学方程式________________________________________________。
(3) X的结构简式_________________。
(4) 与F互为同分异构体又满足下列条件的有_______种。
①遇到氯化铁溶液会显紫色,②会发生银镜反应 ③苯环上有三个取代基
在其它同分异构体中核磁共振氢谱有六组峰,氢原子数比符合1:2:2:2:2:1的结构为______________(写出一种即可)。
(5)根据上面合成信息及试剂,写出以乙烯为原料(无机试剂任选),写出合成CH3CH=CHCOOCH2CH3路线_____________________。
【答案】 羟基 ![]()
![]() 20
20 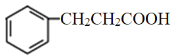 、
、 、
、 、
、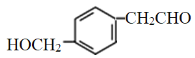 CH2=CH2
CH2=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3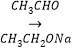 CH3CH=CHCOOCH2CH3
CH3CH=CHCOOCH2CH3
【解析】乙烯与水在催化剂作用下发生加成反应生成乙醇,故A是乙醇,乙醇催化氧化最终生成乙酸,故B是乙酸;甲苯在光照条件下与氯气发生的是取代反应,C水解生成D,则D为醇,由D能被氧化为E,且结合给出的信息可知E应为醛类,即甲苯与氯气发生的是甲基上的取代,那么C为![]() ,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为
,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为![]() ,即E为
,即E为![]() ,据此推断得出F为
,据此推断得出F为![]() ,因此X为
,因此X为![]() ;据此解答。
;据此解答。
(1)据以上分析可知,A为乙醇,官能团的名称是羟基;
(2)根据以上分析可知B+D→F是酯化反应,反应的化学方程式为![]() 。
。
(3)根据以上分析可知X的结构简式为![]() 。
。
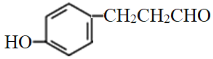
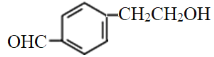
(4)F为![]() ,与F互为同分异构体又满足下列条件的为①遇到氯化铁溶液会显紫色,一定含有酚羟基;②会发生银镜反应,含有醛基;③苯环上有三个取代基;所以苯环上分别连有-OH、-CHO、–CH2CH3的结构有10种;苯环上分别连有-OH、-CH2-CHO、-CH3的结构有10种,共计有20种;在其它同分异构体中核磁共振氢谱有六组峰,氢原子数比符合1:2:2:2:2:1的结构可能有羧酸类(环上一个取代基且含有羧基)、醛类(环上有2个取代基,含有醛基、羟基),共有4种结构如下:
,与F互为同分异构体又满足下列条件的为①遇到氯化铁溶液会显紫色,一定含有酚羟基;②会发生银镜反应,含有醛基;③苯环上有三个取代基;所以苯环上分别连有-OH、-CHO、–CH2CH3的结构有10种;苯环上分别连有-OH、-CH2-CHO、-CH3的结构有10种,共计有20种;在其它同分异构体中核磁共振氢谱有六组峰,氢原子数比符合1:2:2:2:2:1的结构可能有羧酸类(环上一个取代基且含有羧基)、醛类(环上有2个取代基,含有醛基、羟基),共有4种结构如下: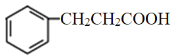 、
、 、
、 、
、 ;
;
(5)乙烯水化制乙醇,乙醇氧化制乙醛,最终氧化为乙酸,乙酸和乙醇生成乙酸乙酯,根据信息可知,乙酸乙酯与乙醛发生反应生成CH3CH=CHCOOCH2CH3;合成流程如下:CH2=CH2![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3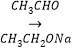 CH3CH=CHCOOCH2CH3。
CH3CH=CHCOOCH2CH3。


科目:高中化学 来源: 题型:
【题目】我国是世界上最大的钨储藏国。金属钨可用于制造灯丝、超硬模具和光学仪器。在工业上常采用高温还原WO3法制取金属钨。回答下列问题:
(1)白钨矿(主要成分是CaWO4)与盐酸反应生成沉淀,灼烧沉淀即可得到WO3,上述两步反应的化学方程式为_________________、__________________。
(2)T℃时,WO3经如下的四步反应生成W。每一步反应的焓变和平衡常数如下: WO3(s)+0.1H2(g)![]() WO2.9(s)+0.1H2O(g) △H1 K1
WO2.9(s)+0.1H2O(g) △H1 K1
WO2.9(s)+0.18H2(g)![]() WO2.72(s)+0.18H2O(g) △H2 K2
WO2.72(s)+0.18H2O(g) △H2 K2
WO2.72(s)+0.72H2(g)![]() WO2(s)+0.72H2O(g) △H3 K3
WO2(s)+0.72H2O(g) △H3 K3
WO2(s)+2H2(g)![]() W(s)+2H2O(g) △H4 K4
W(s)+2H2O(g) △H4 K4
则该温度下,WO3(s)+3H2(g)![]() W(s)+3H2O(g) △H=_________,K=__________。
W(s)+3H2O(g) △H=_________,K=__________。
(3)T1℃时,将一定质量WO3和8.0gH2置于2L密闭容器中,发生反应: WO3(s)+3H2(g)![]() W(s)+3H2O(g),混合气体各组分物质的量之比随时间变化的关系如图所示:
W(s)+3H2O(g),混合气体各组分物质的量之比随时间变化的关系如图所示:

①T1℃时,H2的平衡转化率a=_________%,反应平衡常数K=__________。
②若在4min时降低并维持温度为T2℃,则该反应的△H_______0,若在8min时缩小容器容积,则![]() _________1.3。(填“>”“ <”或“=”)
_________1.3。(填“>”“ <”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然碱组成可表示为xNa2CO3·yNaHCO3·zH2O。取m g该天然碱配成1L溶液M。取出100mLM向其中加入50mL1 mol·L-1盐酸,两者恰好完全反应生成NaCl,同时产生CO2的体积为672mL(标准状况下),下列推断正确的是( )
A. m g该天然碱中含0.3molNa2CO3 B. m g该天然碱中含0.3molNa+
C. 溶液M中c(Na+)=0.5 mol·L-1 D. 该天然碱中x:y:z=2:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中溴含量约为65mg·L-1,从海水中提取溴的工业流程如下:
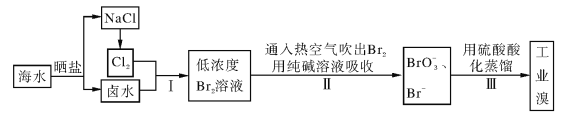
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是____。
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的________。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:_____
![]() Br2+
Br2+![]() CO32-===
CO32-===![]() BrO3-+
BrO3-+![]() Br-+
Br-+![]() CO2↑
CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:__________。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是_____。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硫酸、氨水的密度与所加水量的关系如下图所示:

现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶液 | 溶质的物质的量浓度 | 溶液的密度/g·cm-3 |
硫酸 | 4 mol·L-1 | ρ1 |
2 mol·L-1 | ρ2 | |
氨水 | 4 mol·L-1 | ρ3 |
2 mol·L-1 | ρ4 |
(1)ρ1、ρ2、ρ3、ρ4由大到小的顺序为:________。
(2)表中2 mol·L-1氨水的质量分数为:________。
(3)将4 mol·L-1的氨水与2 mol·L-1的硫酸等体积混合,所得溶液呈______性(填“酸”、“碱”、“中”);溶液中离子浓度从大到小的顺序是:___________________。
(4)将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是______。
A.>15% B.=15% C.<15% D.无法判断
(5)100g浓度为4 mol·L-1的硫酸溶液与_____mL水混合,可以使硫酸的物质的量浓度减小到2 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】均由两种短周期元素组成的A、B、C三种化合物分子,都含有18个电子,它们分子中所含原子的数目依次为2、3、4。A和C分子中,其原子个数比都为1:1,B分子中原子个数比为1:2。由两种短周期元素组成的双核D离子中含有10个电子,它与A、B分子均能反应,生成一种常见的10电子分子E。请回答下列问题:
(1)C的化学式为_____。A的还原性______B的还原性(填“大于”或“小于”)
(2)写出B与D在溶液中反应的离子方程式__________。
(3)气态的A分子遇到某10电子分子会产生白烟,请写出该白烟成分的电子式_______;该白烟的水溶液与浓的含D离子的溶液在受热条件下反应的离子方程式为_________。
(4)写出一个含有18电子的五原子分子的化学式_______,其中的一种元素形成的单质可被含D离子的溶液腐蚀,发生反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将BaSO4放入水中不能导电,所以硫酸钡不是电解质
B.NaCl溶液能导电,所以NaCl溶液是电解质
C.NH3溶于水能导电,所以NH3是电解质
D.固态的NaCl不导电,熔融态NaCl可以导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
半导体材料磷化硼(BP)可由BBr3和PBr3在高温下合成。回答下列问题:
(1)基态P原子的价电子排布式为__________,同周期中第一电离能比P 小的元素有______种。
(2)在水中的溶解度BBr3_______PBr3(填“ >”或“ <”),原因是_____________。
(3)一定温度下PBr5能形成阴、阳离子个数比为1:1的导电熔体,经测定其中P—Br键键长均相等。写出该导电熔体中阳离子的电子式:_________,其中P原子的杂化轨道类型是_______。
(4)已知磷化硼晶体中P原子作A1型最密堆积,B原子填入四面体空隙中,相邻P原子和B原子核间距为d cm,则该晶体中每个B原子周围有_____个B原子与它距离最近,晶体密度为____g·cm-3(NA表示阿伏加德罗常数的值),若某个P原子的坐标为(0,0,0),则晶胞中其余P原子的坐标为__________(写出一个即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com