
����Ŀ����t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵����ȷ����
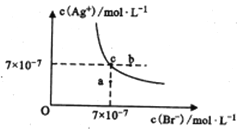
A. ͼ��a���Ӧ����ϵ�н���AgBr��������
B. ����NaBr���壬AgBr���ܽ�ȼ�С��AgBr��KspҲ��С
C. ��AgBr������Һ�м������NaBr����ʹ��Һ��c��䵽b��
D. ��t��ʱ��AgCl(s)+Br��(aq) ![]() AgBr(s)+Cl��(aq)��ƽ�ⳣ��K��816
AgBr(s)+Cl��(aq)��ƽ�ⳣ��K��816
���𰸡�D
��������
A. a��λ�������·���c(Ag+)c(Br��)< Ksp����Ӧ����ҺΪ��������Һ����A����
B. ��һ���¶��£�KspΪһ��������B����
C. AgBr![]() Ag+(aq)+Br��(aq)���������NaBr��c(Br��)����ʹ�ܽ�ƽ�������ƶ���c(Ag+)Ӧ��С������Ȼ���������ƶ������ܵ�b�㣬��C����
Ag+(aq)+Br��(aq)���������NaBr��c(Br��)����ʹ�ܽ�ƽ�������ƶ���c(Ag+)Ӧ��С������Ȼ���������ƶ������ܵ�b�㣬��C����
D.��ͼ��c���֪��t��ʱAgBr��Ksp= c(Ag+)c(Br��)=��7��10-7��2=4.9��10-13���ɷ���ʽ��֪��K= c(Cl��) / c(Br��)=Ksp(AgCl)/ Ksp(AgBr)= 4��10-10/4.9��10-13��816����D��ȷ��
��ѡD��


 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д� �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£��ں����ܱ������У��ܱ�ʾ��ӦX��g��+2Y��g��![]() 2Z��g��һ���ﵽ��ѧƽ��״̬���ǣ� ��
2Z��g��һ���ﵽ��ѧƽ��״̬���ǣ� ��
A. �����е�ѹǿ���ٷ����仯
B. X��Y��Z�����ʵ���֮��Ϊ1��2��2
C. X��Y��Z������֮��1��2��2
D. ��λʱ��������n mol Z��ͬʱ����n mol Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2S��һ�־綾���壬��ͼΪ����ĤH2Sȼ�ϵ�ص�ʾ��ͼ���ɶ�H2S������Դ�����á����������������

![]()
A. a�Ǹ�������ع���ʱ�����ӵ����������ǣ��缫a-����һ�缫b-����Ĥһ�缫a
B. ��ع���ʱ����ѧ��ת��Ϊ���ܺ�����
C. �缫b�Ϸ����ĵ缫��ӦʽΪO2+ 4e-+4H+=2H2O
D. ����·��ͨ��4mol����ʱ����4molH+������Ĥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�л�������Ľṹʽ������ģ�����£�

����л����ӽṹ�������ǿ�����ֶ��Ǻ˴Ź�����ͼ�Ǽ��������ģ����ĸ����ʵ�1H�˴Ź�����ͼ(��λ��ppm)��

�Իش��������⣺
��1��������ģ����ȣ��ṹʽ�е�Et��ʾ__________(������)�����л���ķ���ʽΪ______________��
��2���÷����й���__________�ֻ�ѧ������ͬ����ԭ�ӣ���ѧ������ͬ����ԭ�������________����������________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2O��H2O��2NaOH�ķ�Ӧ��������
A. ���Ϸ�Ӧ B. �ֽⷴӦ C. �û���Ӧ D. ���ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��Ȼ�ѧ����ʽ����������ȷ���ǣ�������
A. ������ȼ����Ϊ285.5kJ/mo1����ˮ�����Ȼ�ѧ����ʽΪ��2H2O��l���T2H2��g��+O2��g������H=+285.5kJ/mol
B. 1mol������ȫȼ������CO2��H2O��l��ʱ�ų�890kJ�����������Ȼ�ѧ����ʽΪ
![]() CH4��g��+O2��g���T
CH4��g��+O2��g���T![]() CO2��g��+H2O��l������H=-445kJ/mol
CO2��g��+H2O��l������H=-445kJ/mol
C. ��֪2C��s��+O2��g���T2CO��g������H=-221kJ/mol����C��ȼ����Ϊ110.5kJ/mol
D. ��֪�к���Ϊ57.3kJ/mol��HF��NaOH��Һ��Ӧ��H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ2NO2![]() 2NO+O2�ں����ܱ������з�Ӧ�������жϴ˷�Ӧ�ﵽ����ȵı�־�ǣ� ��
2NO+O2�ں����ܱ������з�Ӧ�������жϴ˷�Ӧ�ﵽ����ȵı�־�ǣ� ��
A. ��λʱ��������n mol O2 ��ͬʱ������2n molNO2 B. ��������ƽ����Է����������ٸı�
C. ����������ɫ���ٸı� D. NO2, NO, O2������֮����2:2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̫���ܵ���е�����̫���ܵ�ء��ྦྷ��̫���ܵ�ء�GaAs̫���ܵ�ؼ�ͭ�������ȶ���Ԫ�ع��ɱ�Ĥ̫���ܵ�ء��ش��������⣺
(1)��̬��ͭ����(Cu+)�ļ۲�����Ų�ʽΪ__________��
(2)�顢���ǵ������ڵ�����Ԫ�أ���֪��ĵ�һ������(947kJ��mo1��1)������(941k]��mol��l)�����ԭ�ӽṹ�ĽǶȼ��Խ���__________��
(3)H2O�ķе����H2Se�ķе㣬��ԭ����__________��
(4)GaCl3��AsF3�ķ������幹�ͷֱ���__________��__________��
(5)����(H3BO3)�������ܵ����H+����ˮ�����һ��OH������[B(OH)4]���������������ԡ�
��[B(OH)4] ����Bԭ�ӵ��ӻ�����Ϊ__________��
��[B(OH)4] ���ĽṹʽΪ__________��
(6)���ʯ�ľ�����ͼ�����Թ�ԭ�Ӵ�����ʯ�����е�̼ԭ�ӣ���õ�����裻�������ʯ������һ���̼ԭ�ӻ��ɹ�ԭ�ӣ���̼����ԭ�ӽ��棬���õ�̼���辧��(���ɰ)��

�ٽ��ʯ������衢̼������۵��ɸߵ��͵�����˳����__________(�û�ѧʽ��ʾ)
�ڽ��ʯ�ľ�������Ϊapm(lpm=10��12m)��1cm3�����ƽ������Ϊ__________g(ֻҪ������ʽ�������ӵ�������ֵΪNA)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڹ��˵������ȷ���ǣ� ��
A.���ڵؿ��еĺ�����������
B.������Ȼ���м��л���̬����������̬
C.�������ཫ̫����ת��Ϊ���ܵij��ò���
D.�赥�ʵĵ����������ڵ���;�Ե��֮��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com