
【题目】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒等多种元素构成薄膜太阳能电池。回答下列问题:
(1)基态亚铜离子(Cu+)的价层电子排布式为__________。
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能(947kJ·mo1-1)大于硒(941k]·mol-l)。请从原子结构的角度加以解释__________。
(3)H2O的沸点高于H2Se的沸点,其原因是__________。
(4)GaCl3和AsF3的分子立体构型分别是__________,__________。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4] -中B原子的杂化类型为__________。
②[B(OH)4] -的结构式为__________。
(6)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是__________(用化学式表示)
②金刚石的晶胞参数为apm(lpm=10-12m),1cm3晶体的平均质量为__________g(只要求列算式,阿伏加德罗常数的值为NA)。
【答案】3d10 砷的价电子排布式是4s24p3,4p轨道上的电子处于半充满状态,比较稳定, 气态原子失去一个电子需要的能量比较大 水分子间存在氢键 平面三角形 三角锥形 sp3 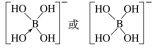 C>SiC>Si 9.6×1031/(a3NA)
C>SiC>Si 9.6×1031/(a3NA)
【解析】
(1)铜是29号元素,其原子核外有29个电子,根据构造原理知,其基态原子核外电子排布式为: 1s22s22p63s23p63d104s1或[Ar]3d104s1。
(2)砷的价电子排布式是4s24p3,4p轨道上的电子处于半充满状态,比较稳定,气态原子失去一个电子需要的能量比较大,而硒的价电子排布式是4s2 4p4, 4p轨道上失去一个电子才处于半充满状态,故第一电离能较小。
(3)H2O的沸点高于H2Se的沸点,是因为水分子间存在氢键。
(4)GaCl3中Ga原子的价层电子对数为3,没有孤电子对,而AsF3中As原子的价层电子对数为4,有一个孤电子对。
(5)①[B(OH)4]-中B的价层电子对=4+1/2(3+1-4×1)=4,所以采取sp3杂化。
②B原子是缺电子原子,所以该离子中还含有配位键。
(6)①根据键长C-C<C-Si<Si-Si判断。
②金刚石属于面心立方晶胞,根据均摊法计算。
(1)铜是29号元素,其原子核外有29个电子,根据构造原理知,其基态原子核外电子排布式为: 1s22s22p63s23p63d104s1或[Ar]3d104s1,则Cu+在基态时的价电子排布式为3d10, 故答案为:3d10。
(2)砷的价电子排布式是4s24p3,4p轨道上的电子处于半充满状态,比较稳定,气态原子失去一个电子需要的能量比较大,而硒的价电子排布式是4s2 4p4,4p轨道上失去一个电子才处于半充满状态,故第一电离能较小,故答案为:砷的价电子排布式是4s24p3,4p轨道上的电子处于半充满状态,比较稳定,气态原子失去一个电子需要的能量比较大。
(3)H2O的沸点高于H2Se的沸点,是因为水分子间存在氢键,故答案为:水分子间存在氢键。
(4)GaCl3中Ga原子的价层电子对数为3,没有孤电子对,而AsF3中As原子的价层电子对数为4,有一个孤电子对,故GaCl3空间构型为平面三角形,AsF3的空间构型为三角锥形;
故答案为:平面三角形;三角锥形。
(5)①[B(OH)4]-中B的价层电子对=4+1/2(3+1-4×1)=4,所以采取sp3杂化,故答案为:sp3。
②B原子是缺电子原子,所以该离子中还含有配位键,其结构式为: ,故答案为:
,故答案为: 。
。
(6)①形成的晶体都是原子晶体,由于键长C-C<C-Si<Si-Si,则熔点为金刚石>碳化硅>晶体硅,故答案为:C>SiC>Si。
②金刚石属于面心立方晶胞,即C原子处在立方体的8个顶点,6个面心,体内有4个,根据均摊法推知,一个晶胞中含有8个C原子,又因为一个C原子的质量为12/NAg,一个晶胞中所含C原子的质量为96/NA g,而一个晶胞的体积为(a×10-10)3 cm3,所以1cm3晶体的平均质量为9.6×1031/(a3 NA) g,故答案为:9.6×1031/(a3 NA)。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
B. 增大压强可加快SO2转化为SO3的速率
C. 黄绿色的氯水光照后颜色变浅
D. 在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。已知t℃时AgCl的Ksp=4×10-10,下列说法正确的是
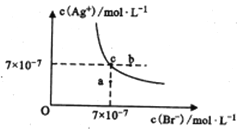
A. 图中a点对应的体系中将有AgBr沉淀生成
B. 加入NaBr固体,AgBr的溶解度减小,AgBr的Ksp也减小
C. 在AgBr饱和溶液中加入固体NaBr,可使溶液中c点变到b点
D. 在t℃时,AgCl(s)+Br-(aq) ![]() AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4 ═ FeSO4+H2↑的能量变化趋势,如图所示:
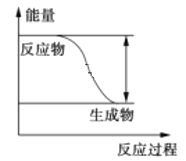
(1)该反应为______反应(填“吸热”或“放热”)
(2)若要使该反应的反应速率加快,下列措施可行的是______(选填A、B、C)。
A.改铁片为铁粉 B.改稀硫酸为98%的硫酸溶液 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______极(填“正”或“负”),铜片上产生的现象为______,该极上发生的电极反应为______,消耗5.6g Fe时转移的电子数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 44gCO2与C3H8的混合物中含有共用电子对数为9NA
B. 将标准状况下2.24LSO2通入水中完全溶解,溶液中HSO32-与SO32-总数为0.1NA
C. 硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA
D. 标准状况下,8.96L的平均相对分子质量为3.5的H2与D2混合物中含中子数0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是

A. 水合铜离子的模型如图1所示,1个水合铜离子中有4个配位键
B. CaF2晶体的晶胞如图2所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图3所示,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图4,为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
![]()
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O;
②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合价为:__________。
(2)用盐酸酸浸时发生反应的离子方程式为: __________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有_____________________。
②如何证明晶体已洗净?_______________________。
(4)TiO2具有很好的散射性,是一种有重要用途的金属氧化物。工业上可用TiCl4水解来制备,制备时需加入大量的水,同时加热,其目的是:_______________。
(5)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:________。
(6)流程中用盐酸酸浸,其实质是BaCO3溶解平衡的移动。若浸出液中c(Ba2+)=0.1mol/L,则c(CO32-)在浸出液中的最大浓度为__________ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钠用作甲状腺肿瘤防治剂、祛痰剂和利尿剂等。实验室用NaOH、单质碘和水合肼(N2H4·H2O)为原料可制备碘化钠。
资料显示:水合肼有还原性,能消除水中溶解的氧气;NaIO3是一种氧化剂。
回答下列问题:
(1)水合肼的制备:有关反应原理为:NaClO + 2NH3 = N2H4·H2O + NaCl。
①用下图装置制取水合肼,其连接顺序为_________(按气流方向,用小写字母表示)。




②装置A的作用是_______。
③开始实验时,先向氧化钙中滴加浓氨水,一段时间后再向B的三口烧瓶中滴加NaClO溶液。滴加NaClO溶液时不能过快的理由___________。
(2)碘化钠的制备
ⅰ.向三口烧瓶中加入8.4gNaOH及30mL水,搅拌、冷却,加入25.4g碘单质,开动磁力搅拌器,保持60~70℃至反应充分;
ⅱ.继续加入稍过量的N2H4·H2O(水合肼),还原NaIO和NaIO3,得NaI溶液粗品,同时释放一种空气中的气体;
ⅲ.向上述反应液中加入1.0g活性炭,煮沸半小时,然后将溶液与活性炭分离;
ⅳ.将步骤ⅲ分离出的溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得产品24.0g。
④步骤ⅰ适宜采用的加热方法是水浴加热, 该步骤反应完全的现象是_________。步骤ⅱ中IO3-参与反应的离子方程式为________________________________。
⑤步骤ⅲ “将溶液与活性炭分离”的方法是趁热过滤。
⑥本次实验产率为__________。实验发现,水合肼实际用量比理论值偏高,可能的原因是___________。
⑦某同学检验产品NaI中是否混有NaIO3杂质。取少量固体样品于试管中,加水溶解,滴加少量淀粉液后再滴加适量稀硫酸,片刻后溶液变蓝。得出NaI中含有NaIO3杂质。请评价该实验结论的合理性____________。(若认为合理写出离子方程式,若认为不合理说明理由)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com