
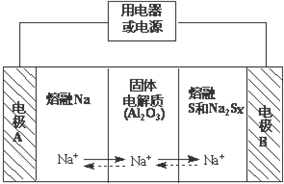
 钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展.钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展.钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |


科目:高中化学 来源: 题型:
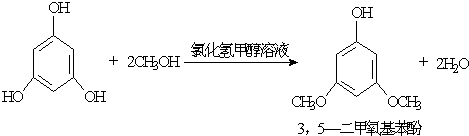
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/(g/cm3) | 溶解性 |
| 甲醇 | 64.7 | - | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | - | 0.7138 | 难溶于水 |
| 3,5-二甲氧基苯酚 | 172 | 36 | - | 易溶于甲醇、乙醚, 微溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
239 94 |
| A、原子序数是239 |
| B、质量数是94 |
| C、中子数是239 |
| D、质子数是94 |
查看答案和解析>>
科目:高中化学 来源: 题型:
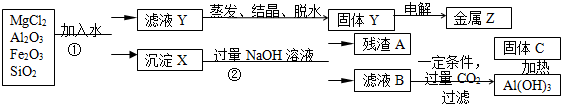
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、脱氧过程是吸热反应映,可降低温度,延长糕点保质期 |
| B、脱氧过程中铁作原电池负极,电极反应为:Fe-3e-═Fe3+ |
| C、脱氧过程中碳做原电池正极,电极反应为:O2+4 e-+4H+═2H2O |
| D、含有2.24g铁粉的脱氧剂,理论上最多能吸收氧气672 mL(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:
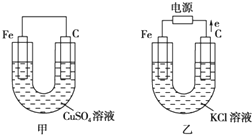 根据如图所提供的信息,在反应一段时间后:
根据如图所提供的信息,在反应一段时间后:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合溶液中由水电离出的c(OH?)<0.2mol?L-1HX溶液中由水电离出的c(H+) |
| B、c(Na+)=c(X?)+c(HX)=0.2mol?L-1 |
| C、c(Na+)-c(X?)=9.9×10-7mol?L-1 |
| D、c(OH?)+c(HX)=c(H+)=1×10-8mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用粮食酿酒的过程中,不可能生成乙酸 |
| B、乙醇和乙酸互为同分异构体 |
| C、氨基酸、蛋白质和纤维素均属于高分子化合物 |
| D、乙烯能使溴的四氯化碳溶液褪色,与乙烯分子含有碳碳双键有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1molH2O的体积约为22.4L |
| B、1L1mol/L的CaCl2溶液中含Cl-的数目为NA |
| C、在25℃、1.01×105Pa的条件下,2.24L H2中含有的分子数小于0.1NA |
| D、标准状况下,2.24 LCl2做成的氯水中含有0.1NA个Cl2分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com