
����Ŀ�������̵�������ʱN2ת��ΪNO����ҵ�̵����ϳɰ����ǹ̵�����Ҫ��ʽ���±��о��˲�ͬ�¶��´����̵���ҵ�̵��IJ���Kֵ��
N2+O2 | N2+3H2 | |||
�¶� | 25�� | 2000�� | 25�� | 400�� |
K | 3.84��10��31 | 0.1 | 5��108 | 1.88��104 |
����˵����ȷ����
A.�ڳ����£���ҵ�̵��dz�������
B.�������ͨ�����ģģ������̵����õ���Դ
C.�����̵��빤ҵ�̵���Kֵ���¶Ⱥ�ѹǿ�ȵ�Ӱ��ϴ�
D.�����̵������ȷ�Ӧ����ҵ�̵��Ƿ��ȷ�Ӧ
���𰸡�D
��������
�ɱ��и����IJ�ͬ�¶��µ�ƽ�ⳣ��ֵ���Եó��������̵���Ӧ�����ȷ�Ӧ����ҵ�̵��Ƿ��ȷ�Ӧ������һ����ѧ��Ӧ�Ƿ�����ʵ�ֹ�ҵ��������ƽ��ĽǶ������Dz����ģ���Ҫ�����ʵĽǶȷ��������һ����Ӧ�ڽ��º͵��������ܹ��Ը��ߵķ�Ӧ���ʽ��в����ܹ���ýϸߵ�ת���ʣ���ô�����ķ�Ӧ��������ʵ�ֹ�ҵ���ķ�Ӧ��
A������ƽ��Ƕȷ����������¹�ҵ�̵��ܹ���ø��ߵ�ƽ��ת���ʣ����ǹ�ҵ�̵�������Ҫ���������º������·�Ӧ����̫�ͣ�����ƽ��ת�����ٸ�����Ҳ�������Թ�ҵ�̵������ڸ��¸�ѹ�����������½��У�A�����
B�����������в�ͬ�¶��µ�ƽ�ⳣ����֪�������̵���Ӧ��ƽ�ⳣ����С�����Ի�ýϸߵ�ת���ʣ���˲��ʺ�ʵ�ִ��ģ�̵���B�����
C��ƽ�ⳣ������Ϊ��ֻ���¶��йصij�����C�����
D�����ڴ����̵���Ӧ���¶�Խ�ߣ�KԽ������Ϊ���ȷ�Ӧ�����ڹ�ҵ�̵���Ӧ���¶�Խ�ߣ�KԽС������Ϊ���ȷ�Ӧ��D����ȷ��
��ѡD��


 ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д� ���ɿ��ñ���ϵ�д�
���ɿ��ñ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��G��ҩ��ϳ��е�һ����Ҫ�м��壬������G��һ�ֺϳ�·�ߣ�

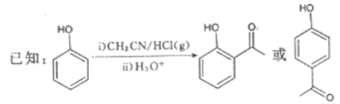
�ش��������⣺
��1��B�Ľṹ��ʽΪ__________���������������ŵ�����Ϊ__________��B����C�ķ�Ӧ����Ϊ__________��
��2��D��������__________��
��3����C��E�ϳ�F�Ļ�ѧ����ʽΪ________________________________________��
��4��D��ͬ���칹���У��ܷ���������Ӧ�ҷ��ӽṹ�к������Ļ���__________�֣����к˴Ź�����������6��壬�����֮��Ϊ1��1��1��1��1��1��ͬ���칹��Ľṹ��ʽΪ______________________ (һ�ּ���)��
��5�����������ϳ�·�ߣ���CH3CH2ClΪԭ��(�����Լ���ѡ)������Ʊ��Ͷ�ȩ(CH3CH=CH
CHO)�ĺϳ�·�ߡ�_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������װ����ȡ����������������������ʵ�顣��ͼ�ش��������⣺
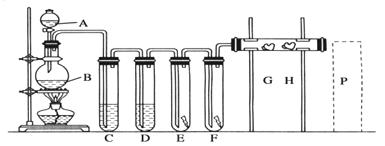
![]() ���������ƣ� ________��B�з�����Ӧ�Ļ�ѧ����ʽΪ____________��
���������ƣ� ________��B�з�����Ӧ�Ļ�ѧ����ʽΪ____________��
![]() Ϊ�˻�ô�������������� C��D��Ӧ�ֱ������Լ�CΪ_________��������________________________��D��Ϊ___________��
Ϊ�˻�ô�������������� C��D��Ӧ�ֱ������Լ�CΪ_________��������________________________��D��Ϊ___________��
![]() ��Ϊ��ɫ�ɲ�����F��Ϊ��ɫʪ�������ɹ۲쵽��ɫ������ɫ����______
��Ϊ��ɫ�ɲ�����F��Ϊ��ɫʪ�������ɹ۲쵽��ɫ������ɫ����______![]() ��E��
��E��![]()
![]() �ǽ��е���KI��Һ������G�����������������__________��H�ǽ���NaBr��Һ������H�����������ӷ���ʽΪ_________________��
�ǽ��е���KI��Һ������G�����������������__________��H�ǽ���NaBr��Һ������H�����������ӷ���ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����ɫ��������������Դ����ͼ����ɫ��Դ��������ȼ�ϵ�����Ĺ���ԭ��ʾ��ͼ(a��b��Ϊ�����Pt�缫)���õ�ع���ʱ������˵����ȷ����(����)

A. a�缫Ϊ�õ������
B. O2��b�缫�ϵõ��ӣ�������
C. ��ع���ʱ��a�缫��Ӧʽ��CH3OCH3��12e����3H2O===2CO2����12H��
D. ��ع���ʱ��ȼ�ϵ���ڲ�H����b�缫����a�缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ��H ����49.0 kJmol��1��һ�������£������Ϊ1 L���ܱ������г���1 mol CO2��3 mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯��������ͼ��ʾ�����������У���ȷ���� ( )
CH3OH(g) + H2O(g) ��H ����49.0 kJmol��1��һ�������£������Ϊ1 L���ܱ������г���1 mol CO2��3 mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯��������ͼ��ʾ�����������У���ȷ���� ( )

A. �����¶���ʹ![]() ����
����
B. ��Ӧ�ﵽƽ��״̬ʱ��CO2��ƽ��ת����Ϊ75%
C. 3 minʱ����CO2��Ũ�ȱ�ʾ������Ӧ���ʵ�����CH3OH��Ũ�ȱ�ʾ���淴Ӧ����
D. �ӷ�Ӧ��ʼ��ƽ�⣬H2��ƽ����Ӧ������(H2)��0.075 molL��1min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ǣ� ��
A. �ö��Ե缫��� Na2SO4��Һ���� 2 mol ����ת��ʱ���ɼ��� 18 g ˮ�ָ�
B. �ö��Ե缫��� CuSO4��Һ�������� 1 mol Cu(OH)2�ָ����ǰŨ��ʱ����·��ת���� 4 mol e��
C. �ö��Ե缫��� 1 mol CuSO4�� 1 mol NaCl �Ļ����Һ����Һ�� pH �ȼ�С������
D. Ҫ��ʵ�� Cu��H2SO4(ϡ) �T CuSO4��H2���ķ�Ӧ�����ڵ����н��У��� Cu Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����1molH2(g)�е�H��H��������436kJ ����������1molO2�еĹ��ۼ�������496kJ��������������������ȼ�յ������仯��ͼ��ʾ������˵����ȷ����
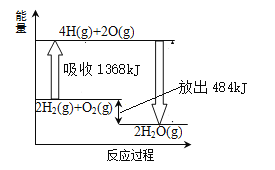
A.H2O(g)=H2(g)+1/2O2(l) ��H=+242kJ/mol
B.H2(g)+1/2O2(g)= H2O(l) ��H<-242kJ/mol
C.�γ�1molH2O(g)�еĻ�ѧ��������926kJ
D.2H2(g)+ O2 (g)= 2H2O (g) ��H=-1852kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaClO2����һ����Ҫ�ĺ�������������ˮ���ܽ�Ƚϴ�����ų�ClO2����һ�ָ�Ч��������������Ư���������ڸ�����ά��ijЩʳƷ��Ư�ס��������ⷨ�Ʊ�NaClO2�����ʵ��װ����ͼ��ʾ��
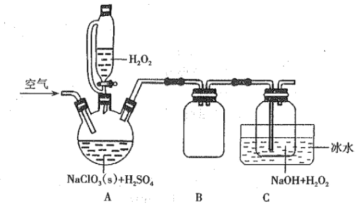
��֪��
��ClO2���۵�Ϊ-59�桢�е�Ϊ11������������ˮ������ˮ�������ֽ⣻����Ũ�Ƚϴ�ʱ�����ֽ⣬���ÿ�����CO2������������ϡ��ʱ����ը���͡�
��2ClO2+H2O2+2NaOH=2NaClO2+O2��+2H2O
��ش�
(1)����ͼ��װ������������Ӧ�ý��еIJ�����____��װ��B��������___����ˮԡ��ȴ����ҪĿ�IJ�����_������ĸ����
a������H2O2�ķֽ� b������ClO2���ܽ�� c������ClO2�ķֽ�
(2)ClO2�Ǻϳ�NaClO2����Ҫԭ�ϣ�д��������ƿ������ClO2�Ļ�ѧ����ʽ�� ____��
(3)װ��C�м���NaOH��Һ��Ŀ�ij�������Ӧ���⣬����Ϊ_____�����������ٹ�������춼��Ӱ��NaClO2�IJ��ʣ��Է���ԭ��________��
(4)����װ�ô��ڵ�����ȱ����_________��
(5)Ϊ��ֹ���ɵ�NaClO2���屻������ԭΪNaCl�����û�ԭ���Ļ�ԭ��Ӧ���С���H2O2�⣬������ѡ��Ļ�ԭ����_������ĸ��
A���������� B������ C���Ȼ����� D���������
(6)��mg NaClO3(s)�����Ƶô�����n g NaClO2(s)����NaClO2�IJ�����_��100%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ��
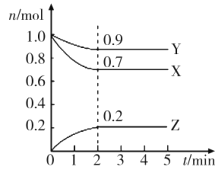
����ͼ��������գ�
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ___��
(2)��X��Y��Z��Ϊ���壬2minʱ��Ӧ�ﵽƽ�⣬��ʱ��ϵ��ѹǿ�뿪ʼʱ��ѹǿ֮��Ϊ___��
(3)��X��Y��Z��Ϊ���壬���ƽ��ʱ�������ڻ�������ƽ����Է�����������ʼͶ��ʱ___ (��������������С�����������)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com