
����Ŀ��ij�о�С����ϳɳ��ݼ������ɺ�Ⱦ���м���X��

��֪��Ϣ��

��1������˵����ȷ����___��
A��������B��C��ת���漰��ȡ����Ӧ B��������C��������
C���Լ�D�����Ǽ״� D�������ɵķ���ʽ��C10H10N2O3S
��2��������F�Ľṹ��ʽ��________��
��3�� д��E+G��H�Ļ�ѧ����ʽ______��
��4��д������ʽΪC6H13NO2��ͬʱ��������������ͬ���칹��Ľṹ��ʽ��д��2������_____��
�ٷ�������һ����Ԫ�����ҳɻ�ԭ������ຬ2����̼ԭ�ӣ�
��1H��NMR��IR��������������4�ֻ�ѧ������ͬ����ԭ�ӡ���N��O����û�й���������O��O������
��5�������CH3CH2OH�� Ϊԭ���Ʊ�X��
Ϊԭ���Ʊ�X�� ���ĺϳ�·�ߣ����Լ���ѡ���ϳ������õ������٢�������֪��Ϣ��������ͼ��ʾ����_____
���ĺϳ�·�ߣ����Լ���ѡ���ϳ������õ������٢�������֪��Ϣ��������ͼ��ʾ����_____
���𰸡�BC (CH3)2CHNH2 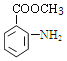 +��CH3��2CHNHSO2Cl��
+��CH3��2CHNHSO2Cl��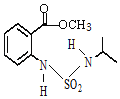 +HCl
+HCl 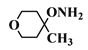 ��
��![]() ��
�� ��
�� CH3CH2OH
CH3CH2OH![]() CH3COOH
CH3COOH CH3COOCH2CH3
CH3COOCH2CH3
![]() CH3COCH2COOC2H5
CH3COCH2COOC2H5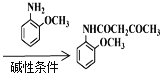
��������
��A�ķ���ʽ�������ɵĽṹ���ݹ��������̣���֪AΪ![]() ��A��������λ������Ӧ����BΪ
��A��������λ������Ӧ����BΪ![]() �������ɲ������ʻ����ǰ�����˵��B��C��������ӦΪ��������Ϊ�Ȼ�����������ԭΪ��������Ϊ�����ױ�����������B�ȷ���������Ӧ������ԭ��Ӧ����C��C��D����������Ӧ����E����B�ȷ���������Ӧ����
�������ɲ������ʻ����ǰ�����˵��B��C��������ӦΪ��������Ϊ�Ȼ�����������ԭΪ��������Ϊ�����ױ�����������B�ȷ���������Ӧ������ԭ��Ӧ����C��C��D����������Ӧ����E����B�ȷ���������Ӧ����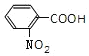 ��Ȼ������ԭ��Ӧ����CΪ
��Ȼ������ԭ��Ӧ����CΪ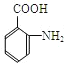 ����E��̼ԭ����Ŀ��֪DΪCH3OH����EΪ
����E��̼ԭ����Ŀ��֪DΪCH3OH����EΪ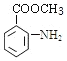 ����F�ķ���ʽ�������ɵĽṹ����֪��������̼���е�2��̼�ϣ���FΪ��CH3��2CHNH2��F����ȡ����Ӧ����GΪ��CH3��2CHNHSO2Cl��F��E����ȡ����Ӧ����HΪ
����F�ķ���ʽ�������ɵĽṹ����֪��������̼���е�2��̼�ϣ���FΪ��CH3��2CHNH2��F����ȡ����Ӧ����GΪ��CH3��2CHNHSO2Cl��F��E����ȡ����Ӧ����HΪ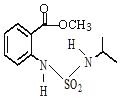 ��ͬʱ������HCl��H����ȡ����Ӧ�õ������ɣ�ͬʱ�����ɼ״���
��ͬʱ������HCl��H����ȡ����Ӧ�õ������ɣ�ͬʱ�����ɼ״���
��5���� ��CH3COCH2COOC2H5��Ӧ����
��CH3COCH2COOC2H5��Ӧ���� ����CH3COOC2H5�ڼ��������µõ�CH3COCH2COOC2H5���Ҵ������������ᣬ�������Ҵ���Ӧ��������������
����CH3COOC2H5�ڼ��������µõ�CH3COCH2COOC2H5���Ҵ������������ᣬ�������Ҵ���Ӧ��������������
(1)A.������B��C����������![]() ��������
�������� ��Ȼ������ԭ��Ӧ����CΪ
��Ȼ������ԭ��Ӧ����CΪ �����漰ȡ����Ӧ��A�����
�����漰ȡ����Ӧ��A�����
B. ������CΪ �����а������Ȼ����������ԣ�B����ȷ��
�����а������Ȼ����������ԣ�B����ȷ��
C. �ɷ�����֪�Լ�D�Ǽ״���C����ȷ��
D. �����ɵķ���ʽ��C10H13N2O3S����D����
�ʴ�ѡ��BC��
(2)������������֪��������F�Ľṹ��ʽ�ǣ�(CH3)2CHNH2��
(3)E+G��H����ȡ����Ӧ���仯ѧ����ʽ�� +(CH3)2CHNHSO2Cl��
+(CH3)2CHNHSO2Cl�� +HCl��
+HCl��
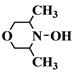
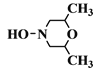
(4)C6H13NO2�����Ͷ�Ϊ1����������������ͬ���칹�壺�ٷ�������һ����Ԫ����˵��û�в����ͼ���Ҳû���������ҳɻ�ԭ������ຬ2����̼ԭ�ӣ���Ԫ���������������Ԫ��ȫΪ̼ԭ�ӣ�����Ԫ���к���һ��O������Ԫ���к���һ��N������Ԫ���к���һ��N��һ��O����1HNMR��IR��������������4�ֻ�ѧ������ͬ����ԭ�ӡ���NO����û�й�����(OO)������Ԫ���к���2��O������������NO����������������ͬʱ�˴Ź���������ʾ��4����ԭ�ӣ��÷��Ӿ����൱�ĶԳ��ԣ�����֪�������������⣬���������⣬���ܵĽṹ��ʽΪ��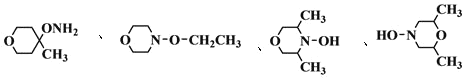 ��
��
(5)�� ��CH3COCH2COOC2H5��Ӧ����
��CH3COCH2COOC2H5��Ӧ���� ����CH3COOC2H5�ڼ��������µõ�CH3COCH2COOC2H5���Ҵ������������ᣬ�������Ҵ���Ӧ���������������ͺϳ�·������ͼΪ��
����CH3COOC2H5�ڼ��������µõ�CH3COCH2COOC2H5���Ҵ������������ᣬ�������Ҵ���Ӧ���������������ͺϳ�·������ͼΪ��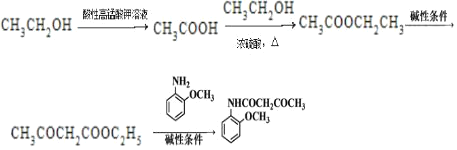 ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ĿǰӦ����㷺�Ľ������ϣ��˽������ʴ��ԭ�����������������Ҫ���壬�Ը�����Ʒ���п���ʴ���������ʵ��ӳ���ʹ��������
��1������ʴ����ǰ�������г��������������⡣�ֽ�һ����������������������У��������������Һ�з����Ļ��Ϸ�Ӧ�Ļ�ѧ����ʽΪ��________________________��
��2������ͼװ�ã�����ģ�����ĵ绯ѧ������

����XΪ̼����Ϊ���������ĸ�ʴ������KӦ����________����
����XΪп������K����M�����õ绯ѧ��������Ϊ________��
��3����ͼ����XΪ��ͭ�������к�ˮ�滻Ϊ����ͭ��Һ������K����N����һ��ʱ���������������3.2 gʱ��X�缫�ܽ��ͭ������________3.2 g(�<����>������)�����������ͭ����Ч��ֹ������ʴ�������������δ����ͭ����Ʋ����𣬶�ͭ���ȶ�п���������ױ���ʴ�����Ҫ˵��ԭ��_________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼú�������к��� SO2��Ϊ�����������������������ö��ַ���ʵ����������
��.(1)��ʪʽ���շ����������ռ��� SO2 ������Ӧ�Ӷ����������Լ����ʺ������÷����ռ�����_____(����ĸ���)��
a. ʯ���� b.CaCl2��Һ
(2)ij�������ú� SO2 ������������Cr2O72-�����Է�ˮ���������з�Ӧ��ĸ�Ԫ����Cr3+��ʽ���ڣ������������£�

���� SO2 ����������ˮʱ�������� SO2 ��_____�ԡ�
���������з�����Ӧ�����ӷ���ʽΪ_____��
��.ʯ��-ʯ�෨���ռ�dz��õ���������ʯ��-ʯ�෨�����շ�ӦΪCa(OH)2+SO2= CaSO3��+H2O�����ղ�����������ɹܵ���������������������ӦΪ2CaSO3+O2+4H2O =2CaSO4��2H2O����������ͼ��

�ռ�����շ�ӦΪ2NaOH+SO2=Na2SO3+H2O���÷����ص����������Ƽ���ǿ�����տ졢Ч�ʸߡ���������ͼ��

��֪��
�Լ� | Ca(OH)2 | NaOH |
�۸�(Ԫ/kg) | 0.36 | 2.9 |
���� SO2 �ijɱ�(Ԫ/mol) | 0.027 | 0.232 |
(3)ʯ��-ʯ�෨���ռ��ȣ�ʯ��-ʯ�෨���ŵ���_______��ȱ����_______��
(4)ijѧϰС����ʯ��-ʯ�෨���ռ�Ļ����ϣ����һ���Ľ��ġ���ʵ������ѭ������������������ͼ�еļס��ҡ�������_____��_____��_____(�ѧʽ)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɼ�������������ǡ���ȩ����������������ɵĻ�����֪������Ԫ�ص���������Ϊ44%������Ԫ�ص���������Ϊ�� ��
A. 48%B. 8%C. 56%D. 10%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���A1.44g��ȫȼ������2.16g H2O�����ɵ�CO2ǡ����200mL 1mol/LKOH��Һ�����������Σ���A�������м����������ͼ����ͼ��

��1����д��A�����ʽ_____________��
��2����д��A�ķ���ʽ______________��
��3����A��һ�ȴ���ֻ��һ�֣�A�Ľṹ��ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����( )
A.������SO2ͨ�뵽Ca(ClO)2��Һ�У�Ca(ClO)2 + SO2 + H2O �T CaSO3��+ 2HClO
B.�����£�����Ȼ����ҺpH<7����ΪNH4+ + 2H2O NH3��H2O + H3O+
C.������ʴ�����ĵ缫��ӦʽΪ��Fe - 3e- �T Fe3+
D.��̼��������Һ����ˮ�����е��Ȼ���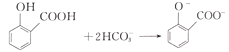
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������㷺�����ڶ�ֲ�����ڣ�����������������˵����ȷ����( )

A.b����NaOH����Һ�����·�����ȥ��Ӧ
B.��a��Ϊͬ���칹��Ķ�Ԫȡ���ķ��㻯������9��
C.b����������̼ԭ�ӿ��ܾ�����ͬһƽ����
D.a��c��������ˮ�����ӳɷ�Ӧ����1mol ���ӷֱ��������3 mol��1 mol Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL��FeBr2��Һ��ͨ���״���µ�C12 3.36 L��C12ȫ������ԭ�����Ҳ����Һ��c(Br�C)=c(Cl�C)����ԭFeBr2��Һ�����ʵ���Ũ����
A.3mol/LB.2mol/ LC.1.5 mol/ LD.0.75mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
�ٽ���������һ���Ǽ��������� �ڼ���������һ���ǽ���������
������������һ���Ƿǽ��������� �ܷǽ��������ﲻһ��������������
���ܵ����![]() �Ļ�����һ������ ��
�Ļ�����һ������ ��![]() ����һԪ��
����һԪ��
�ߺ�����Ԫ�صĻ����ﶼ�������� �����������ﲻһ������ˮ����������
A.2��B.3��C.4��D.5��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com