
【题目】实验室需要配制0.1molL-1NaOH溶液500mL,回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是___(填字母),配制上述溶液还需要用到的玻璃仪器是___(填仪器名称)。
(2)配制该NaOH溶液,需要用托盘天平称取NaOH固体___克。
(3)将NaOH固体溶解时用到玻璃棒,其作用是___。
(4)在配制过程中,下列实验操作会引起所配的NaOH溶液的浓度偏大的是___。
A.烧杯未进行洗涤
B.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
C.往容量瓶转移时,有少量液体溅出
D.在容量瓶中定容时俯视容量瓶刻度线
E.摇匀后静置,发现液面不到刻度线,再加水至刻度线
【答案】C 胶头滴管 2.0 加速溶解 BD
【解析】
(1)用固体氢氧化钠配制溶液,需要用到药匙、天平、量筒、胶头滴管、烧杯、玻璃棒、容量瓶等,如图所示的仪器中肯定不需要的是分液漏斗,配制溶液还需要用到的玻璃仪器是胶头滴管,故答案为:C;胶头滴管;
(2)配制该NaOH溶液,需要称取NaOH固体m(NaOH)=cVM=0.1molL-1×0.5L×40g/mol=2.0g,故答案为:2.0;
(3)溶解时,用到玻璃棒,其作用是搅拌加速溶解,故答案为:加速溶解;
(4)A.烧杯未进行洗涤,导致溶质减少,则所配的NaOH溶液的浓度偏小,故A错误;
B.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,则会导致定容时溶液体积偏小,则所配的NaOH溶液的浓度偏大,故B正确;
C.往容量瓶转移时,有少量液体溅出,则所配的NaOH溶液的溶质减少,浓度偏小,故C错误;
D.在容量瓶中定容时俯视容量瓶刻度线,则导致溶液体积偏小,所配的NaOH溶液的浓度偏大,故D正确;
E.摇匀后静置,发现液面不到刻度线,再加水至刻度线,则导致溶液被稀释,所配的NaOH溶液的浓度偏小,故E错误;
综上所述,故答案为:BD。


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】下列物质在常温下发生水解时,对应的离子方程式正确的是
①NaHCO3:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
②NH4Cl:NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
③CuSO4:Cu2++2H2O![]() Cu(OH)2+2H+
Cu(OH)2+2H+
④NaF:F-+H2O===HF+OH-
A. ①②B. ②③C. ①③D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基,I可以用E和H在一定条件下合成:
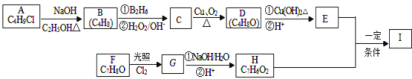
已知以下信息:
①A的核磁共振氢谱表明其只有一种化学环境的氢;
②R-CH=CH2![]() R-CH2CH2OH;
R-CH2CH2OH;
③化合物F苯环上的一氯代物只有两种;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。⑤CH3CHO+2Cu(OH)2+2NaOH![]() CH3COONa+Cu2O↓+3H2O。
CH3COONa+Cu2O↓+3H2O。
回答下列问题:
(1)A的化学名称为_______;
(2)D的结构简式为______;
(3)E中的官能团名称为_________________;
(4)F生成G的化学方程式为________________,该反应类型为_________________。
(5)I的结构简式为______________________________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有_______种(不考虑立体异构)。J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间反应的产物中一定不存在同分异构体的是
A. CH3-CH=CH2与HBr B. ![]() 与NaOH乙醇溶液共热
与NaOH乙醇溶液共热
C. CH3CH3与Cl2 D.  与NaHCO3溶液
与NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题。
(1)等物质的量的下列有机物完全燃烧,消耗O2最多的是_________;等质量的下列有机物完全燃烧,消耗O2最多的是_________。(请填字母)
A. CH4 B. C2H6 C. C3H8 D. C5H12
(2)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。则A的结构简式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对浓硫酸与木炭反应探究。
(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是___。
(2)试用如图所列各装置设计一个实验,来验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号)(_____)→(②)→(_____)→(_____)。
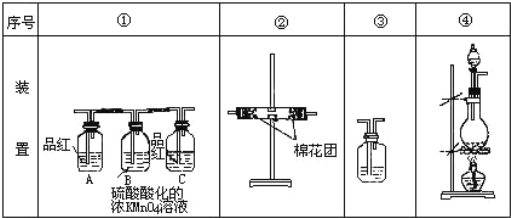
(3)实验时可观察到装置①中A瓶现象___,C瓶现象___,B瓶溶液的作用是___。
(4)装置②中所加的固体药品是___。
(5)装置③中所盛溶液是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物多为重要的化工原料。请回答下列问题:
I.多硫化物是含多硫离子(Sx2-)的化合物,可用作废水处理剂、硫化剂等。
(1)Na2S2的电子式为___。
(2)Na2S5(易溶于水)在酸性条件下可生成H2S和S,该反应的离子方程式为___。
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为___。
II.焦亚硫酸钠(Na2S2O5)是一种食品抗氧化剂,易溶于水。
(4)焦亚硫酸钠(Na2S2O5)中硫元素的化合价为___。
(5)向某些饮料中添加少量焦亚硫酸钠(Na2S2O5),可降低饮料中溶解氧的含量,发生反应的离子方程式为__。
(6)向饱和碳酸钠溶液中通入过量SO2可制得焦亚硫酸钠,发生反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。

有关上述两种化合物的说法正确的是
A. 常温下,1mol丁香酚只能与1molBr2反应
B. 丁香酚不能使FeCl3溶液发生显色反应
C. 1mol香兰素最多能与3mol氢气发生加成反应
D. 香兰素分子中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮的循环和转化对生产、生活有重要价值。
I.氮是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示:

设备1、3中发生反应的化学方程式分别是_________________、_________________;设备2中通入的物质A是__________。
II.氨氮废水的处理是当前科学研究的热点问题之一。氨氮废水中氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

(1)过程①的目的是将NH4+转化成NH3,并通过鼓入大量热空气将氨气吹出,写出NH4+转化成NH3的离子方程式:______________________________
(2)过程②中加入NaClO溶液可将氨氮化合物转化为无毒物质,反应后含氮元素、氯元素的物质的化学式分别为__________、__________。
(3)图中含余氯废水中含有NaClO,则X可选用__________(填序号)的溶液达到去除余氯的目的。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
写出该反应的离子方程式:___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com