
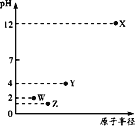
【题目】第三周期元素X、Y、Z、W的最高价氧化物分别溶于水得溶液,0.010mol/L的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是( )
A.Y可能是硅元素
B.简单离子半径:Z>W>X
C.气态氢化物的稳定性:Y>W
D.非金属性:Y>Z
【答案】B
【解析】
第三周期元素中,X最高价氧化物水化物的溶液的pH为12,氢氧根浓度为0.01mol/L,故为一元强碱,则X为Na,Y、W、Z对应的最高价氧化物水化物的溶液pH均小于7,均为酸,W最高价含氧酸溶液中氢离子浓度为0.01mol/L,故为一元强酸,则W为Cl元素;等浓度的最高价含氧酸中,Z电离出氢离子浓度比W的大、Y对应的酸性最弱,而原子半径Y>Z>Cl,故Z为S元素,Y为P元素,以此来解答。
由上述分析可知,X为Na、Y为P、Z为S,W为Cl,
A.Y不可能是Si元素,因为SiO2不溶于水,由分析可知Y是P元素,故A错误;
B.电子层越多,离子半径越大,具有相同排布的离子中原子序数大的离子半径小,则S2-、Cl-和Na+的离子半径为S2->Cl->Na+,故B正确;
C.Cl的非金属性比P强,则气态氢化物的稳定性HCl>PH3,故C错误;
D.S和P是同周期的主族元素,核电荷数大,元素的非金属性强,即S的非金属性大于P,故D错误;
故答案为B。


 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是( )
A.在催化剂存在条件下苯与溴反应制溴苯
B.ClCH2CH=CH2+NaOH![]() HOCH2CH=CH2+NaCl
HOCH2CH=CH2+NaCl
C.乙酸乙酯在碱性条件下水解
D.在一定条件下苯与氢气反应制环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,甲烷与氯气在光照条件下反应,不涉及的实验现象是( )
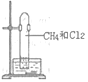
A.气体的黄绿色变浅至消失B.试管内壁上有油珠附着
C.试管内水面上升D.试管内有白烟生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸松油酯是松油醇的酯化产物,具有甜香气味,广泛应用于日用和食用香精中。乙酸松油酯的结构简式如图甲所示,下列说法正确的是
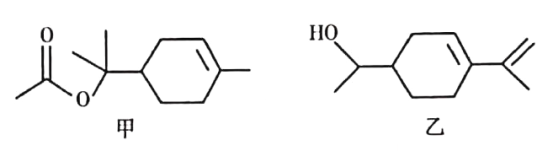
A. 乙酸松油酯的分子式为C12H22O2
B. 乙酸松油酯的水解产物松油醇与图乙所示物质互为同分异构体
C. 乙酸松油酯既易溶于水、也易溶于乙醇或油脂
D. 乙酸松油酯能使Br2的CCl4溶液或酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯时,经过配制混酸、硝化反应(50~60℃)、洗涤分离、干燥蒸馏等步骤,下列图示装置和原理能达到目的的
A. 配制混酸 B. 硝化反应
B. 硝化反应
C. 分离硝基苯 D. 蒸馏硝基苯
D. 蒸馏硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮(水中以NH3和NH4+形式存在的氮)含量是环境水体污染的一项重要指标,其氧化过程会造成水体中溶解氧浓度降低,导致水质下降,影响水生动植物的生长。
(1)水中NH3和NH4+两者的浓度比取决于水体的pH和水温。当pH偏高时,___比例较高,原因是___(请用离子方程式表示)。
(2)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH充分反应后,再向水中通入空气,可增大NH3的脱除率,用平衡移动原理解释其原因:___。
(3)在微生物作用下,蛋白质在水中分解产生的NH3能够被O2氧化生成亚硝酸(HNO2)。
___NH3+__O2→__HNO2+__________
①请将上述化学方程式补充完整,并配平。
②反应中氧化剂与还原剂的物质的量之比为___。
③若反应中有0.6mol电子发生转移,生成亚硝酸的质量为___。
(4)水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示。DO的测定原理如下:
①2Mn2++O2+4OH-→2MnO(OH)2↓
②MnO(OH)2+2I-+4H+→Mn2++I2+3H2O
③2S2O32-+I2→S4O62-+2I-
某小组同学取100.00mL水样经反应①和②后,取出20.00mL溶液,以淀粉作指示剂,用amol/LNa2S2O3溶液进行滴定,终点现象为___;滴定消耗Na2S2O3溶液bmL,水样的DO=____mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生如图所示一系列变化,则下列说法错误的是

A. A分子中所有原子均在同一平面内
B. A→B所用试剂为![]()
C. 分子式为![]() 的酯有3种
的酯有3种
D. 等物质的量的B、D分别与足量钠反应生成气体的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜在自然界中常以多种形态存在,现以孔雀石矿石[成分为Cu2(OH)2CO3、CuFeS2、SiO2、Fe2O3等]为原料生产主产品胆矾和副产品铁红的工艺流程如图:

(1)气体1的成分除H2O(g)外,还有CO2、SO2,写出步骤①中发生氧化还原反应的化学方程式为 _______________,若反应生成1mol SO2,则反应中转移的电子数为___________mol。滤液1的主要成分为__________(写化学式)
(2)目前工业生产中步骤③酸浸的百分率为70%,为进一步提高酸浸的百分率可采取的措施有_________________(答出两点)。
(3)步骤④调pH所用试剂为_____________ (写化学式)
(4)常温下滤液3的pH=4,Ksp[Fe(OH) 3]=4×10-38,则滤液3中c(Fe3+)=___________。
(5)步骤⑤操作为_______________________________________________________.。
(6)假设使用孔雀石矿石质量为m kg,步骤③酸浸的百分率为70%,经滤渣2所得铁红的质量为n kg,则:
①铁红的用途之一为________,
②孔雀石矿石中铁元素的含量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 100℃时,0.01 mol·L-1 NaOH 溶液中水电离的 c(H+)=10-10 mol·L-1,该温度下将 pH=8 的 NaOH溶液 V1 L 与 pH=5 的 H2SO4 溶液 V2 L 混合,所得溶液 pH=7,则 V1∶V2 为
A.2∶9B.1∶9C.1∶1D.1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com