



 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| A、从左到右,原子半径逐渐增大 |
| B、从左到右,元素原子氧化性减弱,还原性增强 |
| C、从左到右,元素最高正价从+1递增到+7(O,P除外),负价由-4递变到-1 |
| D、从左到右,元素最高价氧化物对应的水化物的碱性增强,酸性减弱(O,F除外) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、当有01mol电子转移时,a极产生1.21LO2(标准状况下) |
| B、b极上发生的电极反应是:4H2O+4e-=2H2↑+4OH- |
| C、c极发生的电极反应是:O2+2H2O+4e-=4OH- |
| D、d极上进行氧化反应,B中的H+可以通过隔膜进入A |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5-3 | +7-1 | +5-3 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
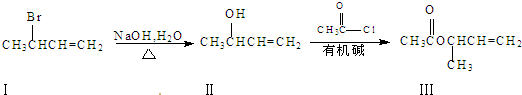
查看答案和解析>>
科目:高中化学 来源: 题型:
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com