
 ;
; ;
; ,
, ;
; ;
; ;
;
| ||
| ||
| △ |
| ||
| ||
| △ |
| ||
| ||


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
| A、正反应和逆反应的速率都为零 |
| B、容器内各物质的浓度不随时间变化 |
| C、容器内X、Y、Z的浓度之比为1:2:2 |
| D、单位时间消耗0.1mol X同时生成0.2mol Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 回答下列问题:
回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
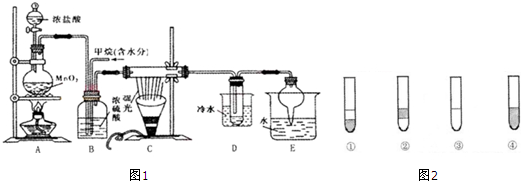
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 药品 | 选用试剂 | 操作方法 |
| A | 乙烷(乙炔) | 酸性高锰酸钾溶液 | 洗气 |
| B | 乙烷(乙烯) | 氢气 | 高温、高压、催化剂 |
| C | 乙酸乙酯(乙酸) | 浓的氢氧化钠溶液 | 分液 |
| D | 硝基苯(硝酸) | 氢氧化钠溶液 | 分液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com