
【题目】Ⅰ.在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%。

(1)当温度由T1变化到T2时,平衡常数关系K1___________K2(填“>”,“<”或“=”),焓变△H___________0.(填“>”或“<”)
(2)该反应在T1温度下5.0min达到平衡,这段时间内N2的化学反应速率为___________,N2的转化率___________;
(3)T1温度下该反应的化学平衡常数K1=___________;
(4)T1温度时,若测得高炉中c(N2)=0.5mol/L,c(H2)=0.5mol/L,c(NH3)=0.5mol/L在这种情况下,该反应是否处于平衡状态___________(填是或否),此时反应速率是v正___________v逆(填>,<,=);
Ⅱ.根据最新研究报道,在常温常压和光照条件下N2在催化剂表面与水发生反应:2N2(g)+6H2O(l)=4NH3(g)+3O2(g)。
(1)此反应的△S 0(填“>”或“<”)。
已知2CO(g)+2NO(g)=N2(g)+2CO2(g) △H="-a" kJ·mol-1
2NO(g)+O2(g)=2NO2(g) △H ="-b" kJ·mol-1;CO的燃烧热△H ="-c" kJ·mol-1。
(2)写出消除汽车尾气中NO2的污染时,NO2与CO的反应的热化学反应方程式
【答案】(每空2分共18分)
Ⅰ.(1)>;<;
(2)0.008mol/(L.min);40%;
(3)18.3;
(4)否;>;
Ⅱ.(1)>;
(2)4CO(g)+2NO2(g)=N2(g)+4CO2(g)△H="-a+b-2c" kJmol-1。
【解析】试题分析:Ⅰ.(1)由图可知,温度越高,平衡时NH3的浓度越小,说明升高温度平衡向逆反应进行,平衡常数减小,故平衡常数关系K1>K2,而升高温度平衡向吸热反应移动,故正反应为放热反应,则△H<0,故答案为:>;<;
(2)将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,温度为T1时平衡混合气体中氨气的体积分数为25.0%,则:
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
开始(mol):1 3 0
变化(mol):n 3n 2n
平衡(mol):1-n 3-3n 2n
所以![]() =25%,解得n=0.4,故v(N2)=
=25%,解得n=0.4,故v(N2)=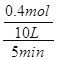 =0.008mol/(L.min),
=0.008mol/(L.min),
N2的转化率=![]() ×100%=40%,故答案为:0.008mol/(L.min);40%;
×100%=40%,故答案为:0.008mol/(L.min);40%;
(3)T1温度下该反应的化学平衡常数K1=![]() =
=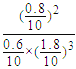 ≈18.3,故答案为:18.3;
≈18.3,故答案为:18.3;
(4)此时浓度商Qc=![]() =4<K=18.3,未处于平衡状态,反应向正反应进行,则v正>v逆,故答案为:否;>;
=4<K=18.3,未处于平衡状态,反应向正反应进行,则v正>v逆,故答案为:否;>;
Ⅱ.(1)反应2N2(g)+6H2O(l)=4NH3(g)+3O2(g)中,气体物质的量增加熵增,故答案为:>;
(2)因为①2CO(g)+2NO(g)═N2(g)+2CO2(g)△H="-a" kJmol-1;
②2NO(g)+O2(g)═2NO2(g) △H="-b" kJmol-1;CO的燃烧热△H="-c" kJmol-1,即:③CO(g)+![]() O2(g)=CO2(g)△H=-ckJ/mol,根据盖斯定律可知,
O2(g)=CO2(g)△H=-ckJ/mol,根据盖斯定律可知,
目标反应4CO(g)+2NO2(g)=N2(g)+4CO2(g)为①-②+2×③,
所以4CO(g)+2NO2(g)=N2(g)+4CO2(g)△H="-a+b-2c" kJmol-1.
故答案为:4CO(g)+2NO2(g)=N2(g)+4CO2(g) △H="-a+b-2c" kJmol-1。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】某种橡胶分解产物为碳氢化合物,对这种碳氢化合物作如下实验:
① 若取一定量完全燃烧,使燃烧后的气体通过干燥管,干燥管增重0.72 g,再通过石灰水,石灰水增重2.2 g。
② 经测定,该碳氢化合物(气体)的密度是相同条件下氢气密度的34倍。
③ 该碳氢化合物0.1 mol能和32 g溴起加成反应.
④ 经分析,在③的生成物中,溴原子分布在不同的碳原子上,且溴代物中有一个碳原子在支链上。下列说法正确的是( )
A.该碳氢化合物为2-甲基-1,3-戊二烯
B.该碳氢化合物与溴单质1:1加成时可以生成3种不同的产物
C.该碳氢化合物与溴单质1:1加成时可以生成2种不同的产物
D.该碳氢化合物与足量氢气加成时可以生成正戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
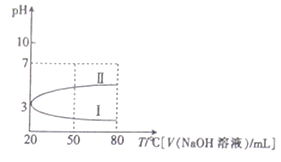
【题目】0.1mol·L-1NH4Al(SO4)2溶液的pH随温度变化的关系如曲线1所示,下列说法中正确的是
A. 0.1mol·L-1NH4Al(SO4)2溶液c(NH4+)大于等浓度的NH4HSO4溶液中c(NH4+)
B. 向100mL0.1mol·L-1NH4Al(SO4)2溶液中逐滴滴加80mL0.05 mol·L-1NaOH 溶液时,溶液pH的变化如曲线II
C. 升高温度,NH4Al(SO4)2溶液的pH减小,是因为促进了NH4Al(SO4)2的电离
D. 20℃时,0.1mol·L-1NH4Al(SO4)2溶液中:2c(SO42-)-c(NH4+)-3c(Al3+)=10-3mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于仪器使用的说法正确的是( )
A. 配制一定物质的量浓度的溶液时应先用该液体润洗容量瓶
B. 振荡分液漏斗时应关闭其玻瑞塞和活塞
C. 蒸发结晶时蒸发皿应放在泥三角上
D. 锥形瓶用作反应容器时一定不能加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
下列说法正确的是

A. 电池内的O2-由电极乙移向电极甲
B. 电池总反应为N2H4+2O2=2NO+2H2O
C. 当甲电极上有1molN2H4消耗时,乙电极上有1mol被氧化
D. 电池外电路的电子由电极乙移向电极甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I-
A. ①③ B. ①②③ C. ③④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.10mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂。重复上述滴定操作2~3 次,记录数据如下。
(1)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 。
A.滴定前平视读数,终点读数时仰视读数
B.锥形瓶水洗后未用待测盐酸润洗
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.标准液漏滴在锥形瓶外一滴
E.滴定前仰视读数 ,终点滴定后俯视读数
F.碱式滴定管尖嘴部分有气泡,滴定后消失
(2)若在达到滴定终点时,不慎多加了一滴NaOH溶液(一滴溶液体积约为0.05mL)继续加水到50 mL,所得溶液的pH为 。
(3)如图是向20mL的盐酸中逐渐加入0.1mol/L NaOH溶液时,溶液的pH变化图像,当滴加NaOH溶液为10mL时,该混合液的pH= ,(含lg表达式),若用该NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是 。

A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(4)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:

①滴定时,滴定终点时滴定现象是_____________。
②该草酸溶液的物质的量浓度为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物的核磁共振氢谱中出现三组峰的是( )
A. 2,2,3,3一四甲基丁烷 B. 2,3,4一三甲基戊烷
C. 3,4一二甲基己烷 D. 2,5一二甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸的性质有:①酸性、②强氧化性、③脱水性、④难挥发性等。乙醇、溴化钠和浓硫酸混合共热制备溴乙烷时,会有多个副反应发生,此过程中浓硫酸显示的性质是
A.①②③④ B.①和② C.只有① D.①和④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com