
| ���� |
| ����NaOH��Һ |
| �������� |
| ����NaOH��Һ |
| 5.6g |
| 8.0g |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
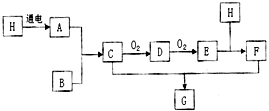 ��֪ͼ��H�dz�����ɫҺ�壬B�ǿ����к����������ʣ�A��BҪ�ڸ��¸�ѹ���ܺϳ�C��F��һ��ǿ�
��֪ͼ��H�dz�����ɫҺ�壬B�ǿ����к����������ʣ�A��BҪ�ڸ��¸�ѹ���ܺϳ�C��F��һ��ǿ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
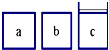 ��ͼ��ʾ����ͬ�����a��b��c���ܱ�����������c������һ������a��b������Ϊ������������ʼ���������ж�������ͬ����SO2��O2ʹ������ѹǿ��ȣ�һ�������·���2SO2+O2?2SO3�ķ�Ӧ���ʣ�
��ͼ��ʾ����ͬ�����a��b��c���ܱ�����������c������һ������a��b������Ϊ������������ʼ���������ж�������ͬ����SO2��O2ʹ������ѹǿ��ȣ�һ�������·���2SO2+O2?2SO3�ķ�Ӧ���ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��10 mL 2 mol?L-1 |
| B��20 mL 2 mol?L-1 |
| C��10 mL 4 mol?L-1 |
| D��20 mL 3 mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��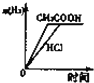 ��ͼ���߱�ʾ�������������ʵ���Ũ�ȵ�����ʹ�����Һ�зֱ��������þ�۲���H2�����ʵ����ı仯 |
B�� ��ʾ��0.01mol?L-1 NaOH��Һ���˵�ϡ�����еĵζ����� |
C�� Ϊˮ�ĵ������ߣ���z����x�㣬�ɲ�����ˮ�м�������NaOH����ķ��� |
D��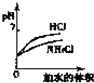 ͼ�����߱�ʾ��pH��ͬ��NH4Cl��Һ������ϡ����ͬ����ʱ������pH�ı仯 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com