
【题目】(1)相同质量的O2和O3,分子数之比为______;O原子数之比为_____;同温同压下密度比为_____。
(2)标准状况下;1.806×l023个CO2分子的体积为____L,与_____g H2O含有O 原子数目相同,此CO2气体与足量的Na2O2固体完全反应后,固体的质量增加______g。
(3)将4g NaOH固体溶于水配成500mL 溶液,所得溶液的物质的量浓度为___mol/L。
① 若从中取出10mL,加水稀释到50mL,则稀释后NaOH 溶液的物质的量浓度为___mol/L。
② 若从中取出10mL,需要加入0.5mol/L盐酸_______mL 才能恰好反应。
(4)标准状况下,将VL某气体(相对分子质最为M)溶解在aL水中(水的密度近似为1g/mL) , 所得溶液的密度为ρg/mL,则溶质的物质的量浓度为______mol/L。
【答案】 3:2 1:1 2:3 6.72 10.8 8.4 0.2 0.04 4 1000ρV/(VM+22400a)
【解析】(1)O2和O3均为氧元素组成的单质,相同质量的O2和O3含有的氧原子数目相等,则分子数之比为![]() :
: ![]() =3:2;O原子数之比为1:1;同温同压下密度比为
=3:2;O原子数之比为1:1;同温同压下密度比为![]() :
:![]() =2:3;
=2:3;
(2)含有1.806×l023个CO2分子的CO2物质的量为![]() =0.3mol,则标准状况下1.806×l023个CO2分子的体积为0.3mol×22.4L/mol=6.72L,与0.3mol×2×18g/mol=10.8g H2O含有O 原子数目相同;
=0.3mol,则标准状况下1.806×l023个CO2分子的体积为0.3mol×22.4L/mol=6.72L,与0.3mol×2×18g/mol=10.8g H2O含有O 原子数目相同;
2CO2+2Na2O2=2Na2CO3+O2 固体增重质量
2mol 2nol 56g
0.3mol m
m=![]() =8.4g,
=8.4g,
故0.3molCO2气体与足量的Na2O2固体完全反应后,固体的质量增加8.4g;
(3)4g NaOH的物质的量为![]() =0.1mol,溶于水配成500mL 溶液,所得溶液的物质的量浓度为
=0.1mol,溶于水配成500mL 溶液,所得溶液的物质的量浓度为![]() =0.2mol/L;
=0.2mol/L;
① 溶液是均一稳定的混合物,则从中取出10mL的NaOH浓度仍为0.2mol/L,加水稀释到50mL,溶液稀释过量中溶质不变,则稀释后NaOH 溶液的物质的量浓度为![]() =0.04mol/L;
=0.04mol/L;
② 已知NaOH+HCl=NaCl+H2O,则NaOH和HCl等物质的量反应,故从中取出10mL,需要加入0.5mol/L盐酸![]() =0.004L=4mL才能恰好反应;
=0.004L=4mL才能恰好反应;
(4)标准状况下,VL某气体的物质的量为![]() =
=![]() mol,质量为
mol,质量为![]() mol×Mg/mol=
mol×Mg/mol=![]() g,则溶解在aL水中(水的密度近似为1g/mL),所得溶液的物质的量浓度为
g,则溶解在aL水中(水的密度近似为1g/mL),所得溶液的物质的量浓度为 =
=![]() mol/L。
mol/L。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】11.0 g铁铝混合物与足量的盐酸反应,生成标准状况下的氢气8.96 L,则混合物中Fe与Al的物质的量之比( )
A. 1:2 B. 2:1 C. 1:1 D. 2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是一种常见的滴定剂和重要化工原料。实验室制备硫代硫酸钠的流程如下:

回答下列问题:
(1)“溶解”使用的水必须先煮沸一段时间,然后冷却至室温待用。其目的是____________。
(2)“反应”中的化学方程式为_____________________________________________。
(3)设计如图所示装置制备硫代硫酸钠晶体:

①B瓶的作用是___________________。
②实验中先打开________(填“A”或“C”)处分液漏斗的活塞。.
③装置D用于处理尾气,可选用的最合理装置为______________(填标号)。

(4)为了探究粗产品中的杂质,进行如下假设并进行实验:
①该粗产品中可能含有的杂质是Na2CO3、NaHCO3、Na2SO3、NaHSO3、S、Na2S和_____________
等其中的一种或几种。
②取少量产品于试管,加入足量稀硫酸,将气体通入CuSO4溶液中,未产生黑色沉淀。据此,______(填“能”,或“不能”)认为粗产品中一定没有Na2S,理由是 _____________________________。
③请选择下列试剂设计实验方案,检验产品中含有Na2CO3或NaHCO3。
限选试剂:3 molL-1H2SO4溶液、1 mol L-1 NaOH溶液、酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水。
实验方案 | _______. |
实验现象 | _______. |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示的变化,其中A为X、Y组成的双原子分子,B和C均为10电子分子。下列说法不正确的是

A.X元素位于第ⅥA族 B.A不能溶于B中
C.A和C不可能发生氧化还原反应 D.B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.20molL﹣1的H2SO4溶液中,H+的物质的量浓度为( )
A. 0.10 molL﹣1 B. 0.20 molL﹣1 C. 0.40 molL﹣1 D. 0.50 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 将0.1molCl2通入一定量水中,HClO、Cl-、ClO-粒子数之和为0.2NA
B. 12gNaHSO4固体中含阳离子数为0.1NA
C. 将1molFe(OH)3加入到含3molHI的溶液完全反应后,溶液中所含I- 的数目为3NA
D. 已知合成氨反应N2(g)+3H2(g) ![]() 2NH3(g) △H= —92.4 kJ·mol-1,当该反应生成NA个NH3分子时,反应放出的热量大于46.2kJ
2NH3(g) △H= —92.4 kJ·mol-1,当该反应生成NA个NH3分子时,反应放出的热量大于46.2kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现钼酸钠可减缓金属的腐蚀速率。工业上利用钼精矿(主要成分是不溶于水的MoS2,含少量重金属化合物)制备钼酸钠晶体( Na2MoO4·2H2O)的途径如图所示:
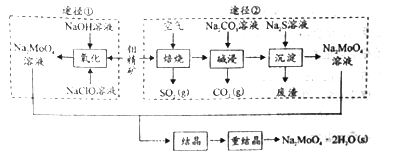
回答下列问题:
Ⅰ.(1)下列标志中,应贴在保存NaClO容器上的是____________。

(2)为了提高焙烧效率,除增大空气量外还可以采用的措施有__________________。
(3)途径①制备钼酸钠溶液,同时有SO42-生成,该反应的离子方程式为_____________。
(4)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因是________________________。
(5)“结晶”前测得部分离子浓度c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L,需加入Ba(OH)2固体除去SO42-。当BaMoO4开始沉淀时,SO42-的去除率为______%。(保留三位有效数字)。
Ⅱ.(1)碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异,其原因可能是_____。
(2)若缓释剂钼酸钠-月桂酰肌氨酸总浓度为300mg·L-1,则缓蚀效果最好时钼酸钠的物质的量浓度为_________(保留三位有效数字)。[已知:Ksp(BaSO4)=1.1×10-10、Ksp(BaMoO4)=4.0×10-8,加入 Ba(OH)2固体引起溶液体积变化可忽略]。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在配制一定物质的量浓度的NaOH溶液时,造成实验结果可能偏高的是( )
A. 转移时有溶液洒落在外 B. 定容时观察液面俯视
C. 有少量NaOH溶液残留在烧杯里 D. 容量瓶中原来有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:

请回答下列问题:
(1)写出B2O3与NH3反应生成BN的方程式___________________________
(2)基态N原子的价层电子排布式为_________。
(3)B、N、O相比,第一电离能最大的是_______,BN中B元素的化合价为_____
(4)SO42–中S原子的杂化轨道类型为_______,O—S—O的键角是_______,写出一个与SO42–等电子体的微粒_______。
(5)BF3能与NH3反应生成BF3NH3,BF3分子的分子构型为_______,BF3NH3中BF3与NH3之间通过___________(填“离子键”、“ 配位键”或“氢键”) 结合。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com