
| A、1g H2和8g O2 |
| B、0.1 mol HCl和2.24 L He |
| C、150℃、1.01×105 Pa时,18 L H2O和18 L CO2 |
| D、常温常压下,28 g CO和6.02×1022个CO分子 |
| m |
| M |
| m |
| n |
| N |
| NA |
| 1g |
| 2g/mol |
| 8g |
| 32g/mol |


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol/L |
| B、0.2 mol/L |
| C、0.3 mol/L |
| D、0.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、直径介于1nm~100nm之间的微粒称为胶体 |
| B、胶体加入电解质可产生沉淀,而溶液不能 |
| C、可用渗析法分离Fe(OH)3胶体和FeCl3溶液的混合物 |
| D、胶体区别于其它分散系的本质特性是丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用惰性电极电解500mL饱和食盐水时,若溶液的pH值变为14时,则电极上转移的电子数目为NA |
| B、1 mol O22-中的电子数为18NA |
| C、7.8gNa2O2加入足量的水中,转移的电子数为0.2NA |
| D、在标准状况下,各为l mol的二氧化硫、三氧化硫的体积均约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2++2OH-═Ca(OH)2↓ CaCO3+2NaOH═Ca(OH)2↓+Na2CO3 |
| B、CO32++2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O |
| C、Ca2++CO32-═CaCO3↓ Ca (NO3)2+NaCO3═CaCO3+2NaNO3 |
| D、H++OH-═H2O 2KOH+H2SO4═K2SO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
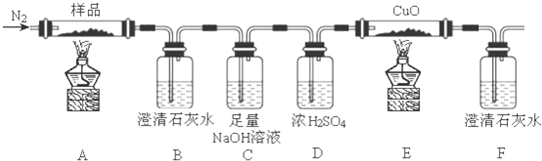
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com