



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
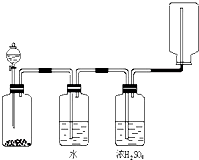
| A��������������� |
| B���������ƺ�Ũ�������ɶ������� |
| C��̼��ƺ��������ɶ�����̼ |
| D���Ȼ��ƺ�Ũ���������Ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������Һ�м��뱥�ͣ�NH4��2SO4��Һ���������������ټ�ˮҲ���ܽ� |
| B���˹��ϳɵľ����������Եĵ�����-�ᾧţ�ȵ�����1965���ҹ���ѧ�����Ⱥϳ� |
| C��������������ʱ���ս���ë����ζ |
| D��ŨHNO3����Ƥ���ϣ�ʹƤ���ʻ�ɫ��������ŨHNO3�͵����ʷ�����ɫ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ף�P����Cl2������Ӧ����PCl3��PCl5����Ӧ���̺������Ĺ�ϵ����ͼ��ʾ��ͼ�еġ�H��ʾ����1mol��������ݣ���֪PCl5�ֽ�����PCl3��Cl2���÷ֽⷴӦ�ǿ��淴Ӧ������˵����ȷ���ǣ�������
���ף�P����Cl2������Ӧ����PCl3��PCl5����Ӧ���̺������Ĺ�ϵ����ͼ��ʾ��ͼ�еġ�H��ʾ����1mol��������ݣ���֪PCl5�ֽ�����PCl3��Cl2���÷ֽⷴӦ�ǿ��淴Ӧ������˵����ȷ���ǣ�������| A�������������䣬�����¶�������PCl5������ |
| B����Ӧ2P��s��+5Cl2��g��=2PCl5��g����Ӧ�ķ�Ӧ�ȡ�H=-798KJ?mol-1 |
| C��P��Cl2��Ӧ����PCl3���Ȼ�ѧ����ʽΪ��2P��s��+3Cl2��g��=2PCl3��g����H=-306KJ?mol-1 |
| D��PCl5�ֽ�ΪPCl3��Cl2���Ȼ�ѧ����ʽΪPCl5��g��=PCl3��g��+Cl2��g����H=-93KJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ģ��ҹ�����ط������˺��飬���⺵���ʩ֮һ���õ⻯�������˹����� |
| B��ʯӢɰ����������ȡ�ߴ��ȵĹ裬���ǽ�̫����ת��Ϊ���ܵij��ò��� |
| C������̫���ܡ����ܺ����ܵ���Դ�����ʯ��Դ������ʵ�֡���̼���á� |
| D����øϴ�·�ȥ�������ʡ�����Ч���ܺã���������ϴ��ë֯Ʒ����֯Ʒ������֯Ʒ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1g H2��8g O2 |
| B��0.1 mol HCl��2.24 L He |
| C��150�桢1.01��105 Paʱ��18 L H2O��18 L CO2 |
| D�����³�ѹ�£�28 g CO��6.02��1022��CO���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com