
【题目】I.有200 mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol·L-1,c(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为___________________mL
II.焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为 NH4C1+ CuO→Cu+CuCl2+ N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。:____________
(2)该反应中,氧化剂和还原剂的物质的量之比为:___________。
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为_______L。
【答案】80.0 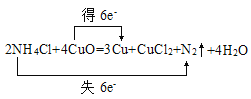 3∶2 1.12
3∶2 1.12
【解析】
I.根据电荷守恒计算混合溶液中n(Al3+),向MgCl2和AlCl3的混合溶液加入NaOH溶液,使Mg2+全部转化为沉淀分离出来,Al3+应恰好转化为![]() ,反应后溶液为NaCl、NaAlO2的混合液,根据钠离子守恒n(NaOH)=n(NaCl)+n(NaAlO2),再结合氯离子守恒、Al原子守恒可知n(NaOH)=n(Cl-)+n(Al3+),再根据
,反应后溶液为NaCl、NaAlO2的混合液,根据钠离子守恒n(NaOH)=n(NaCl)+n(NaAlO2),再结合氯离子守恒、Al原子守恒可知n(NaOH)=n(Cl-)+n(Al3+),再根据![]() 计算;
计算;
II.(1)根据Cu元素的化合价降低、N元素的化合价升高,利用电子守恒及质量守恒定律来配平反应;
(2)该反应中氧化剂为CuO,还原剂为NH4Cl,由(1)中双线桥可知,氧化剂和还原剂的物质的量之比为3:2;
(3)生成1个N2分子转移电子数为6,若反应中电子转移了0.3mol,则产生的N2的物质的量为![]() =0.05mol,带入V=nVm计算。
=0.05mol,带入V=nVm计算。
I.溶液中n(Cl)=0.2L×1.3mol/L=0.26mol,
溶液中n(Mg2+)=0.2mol/L×0.2L=0.04mol,
根据电荷守恒,溶液中n(Al3+)=![]() =0.06mol,
=0.06mol,
将200mL此溶液中的Mg2+转化为Mg(OH)2沉淀并分离析出,反应后溶液为NaCl、NaAlO2的混合液,根据钠离子守恒:n(NaOH)=n(NaCl)+n(NaAlO2),再结合氯离子守恒、Al原子守恒可知:n(NaOH)=n(Cl)+n(Al3+)=0.26mol+0.06mol=0.32mol,所以至少需要4mol/L氢氧化钠溶液的体积为:![]() =0.08L=80mL;
=0.08L=80mL;
II.(1)根据Cu元素的化合价由+2价降至0价,得到2mol电子生成1molCu,N元素的化合价由-3价升至0价,失去6mol电子生成1molN2,利用电子守恒及质量守恒定律来配平反应得2NH4Cl+4CuO=3Cu+CuCl2+N2↑+4H2O,双线桥法标出电子转移情况为: ;
;
(2)该反应中氧化剂为CuO,还原剂为NH4Cl,由(1)中双线桥可知,4molCuO参与反应,做氧化剂的为3mol,氧化剂和还原剂的物质的量之比为3:2;
(3)生成1个N2分子转移电子数为6,若反应中电子转移了0.3mol,则产生的N2的物质的量为![]() =0.05mol,则产生的N2在标准状况下的体积V=nVm=0.05mol×22.4L/mol=1.12L。
=0.05mol,则产生的N2在标准状况下的体积V=nVm=0.05mol×22.4L/mol=1.12L。


科目:高中化学 来源: 题型:
【题目】如图是某另类元素周期表的一部分,下列说法正确的是( )

A. 简单阴离子的半径大小:X>Y>Z
B. 单质的氧化性:X>Y>Z
C. Y的氢化物只有一种
D. X的最高价氧化物对应的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四种短周期元素A,B,C,D,已知:①C,D在同一周期,A,B在同一主族;②它们可以组成化合物A2C、B2C2、DC2、D2A4等;③B的阳离子与C的阴离子的核外电子排布相同;④B2C2同A2C或DC2反应都生成气体C2,B与A2C反应生成气体A2,A2与气体C2按体积比2∶1混合后点燃发生爆炸,其产物是一种常温下常见的无色无味的液体。请回答:
(1)写出元素符号:A________、B________、C________、D________。
(2)在A2C、B2C2、DC2和D2A4中,同时含有离子键和非极性共价键的化合物的电子式为__________;按原子轨道重叠方式,其非极性键的类型是________。化合物DC2的结构式__________。
(3)A2C分子的电子式____________,按原子轨道重叠方式,其共价键的类型是____________。D2A4是平面形分子,其分子中含有______个σ键,______个π键。
(4)写出化学方程式或离子方程式:
B2C2与A2C反应的化学方程式:___________________________________________;
B2C2与DC2反应的化学方程式:___________________________________________;
B与A2C反应的离子方程式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.碳酸钙与醋酸反应:CO32-+2CH3COOH=CO2↑+H2O+2CH3COO-
B.在NaHCO3溶液中加入过量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.用氨水吸收少量的二氧化硫:NH3·H2O+SO2=NH4++HSO3-
D.纯碱溶液中滴加少量硫酸,边加边振荡:2H++CO32-=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干种离子,离子浓度均为0.1mol/L,某同学进行了如下实验:(已知:稀HNO3可与Fe2+发生氧化还原反应产生NO气体,Fe2+被氧化为Fe3+),下列说法正确的是

A.无法确定原试液中是否含有Al3+、Cl-
B.滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C.原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
D.无法确定沉淀C的成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微型银-锌电池可用作电子仪器的电源,其电极分别是![]() 和
和![]() ,电解质为
,电解质为![]() 溶液,电池总反应为
溶液,电池总反应为![]() ,下列说法正确的是( )
,下列说法正确的是( )
A. 电池工作过程中,![]() 溶液浓度降低
溶液浓度降低
B. 电池工作过程中,电解液中![]() 向负极迁移
向负极迁移
C. 负极发生反应![]()
D. 正极发生反应![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机酸有机酯在生产中具有广泛的应用,回答下列问题:
(1)硫酸氢乙酯( )可看作是硫酸与乙醇形成的单酯,工业上常通乙烯与浓硫酸反应制得,该反应的化学方程式为_________,反应类型为__________,写出硫酸与乙醇形成的双酯—硫酸二乙酯(
)可看作是硫酸与乙醇形成的单酯,工业上常通乙烯与浓硫酸反应制得,该反应的化学方程式为_________,反应类型为__________,写出硫酸与乙醇形成的双酯—硫酸二乙酯(![]() )的结构简式_____。
)的结构简式_____。
(2)磷酸三丁酯常作为稀土元素富集时的萃取剂,工业上常用正丁醇与三氯氧磷(![]() )反应来制备,该反应的化学方程式为__________,反应类型为________。写出正丁醇的任意一个醇类同分异构体的结构简式___________。
)反应来制备,该反应的化学方程式为__________,反应类型为________。写出正丁醇的任意一个醇类同分异构体的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】18-Ⅰ分子中只有两种不同化学环境的氢,且数目比为3:2的化合物(________)
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
Ⅱ奥沙拉秦是曾用于治疗急、慢性溃疡性结肠炎的药物,其由水杨酸为起始物的合成路线如下:
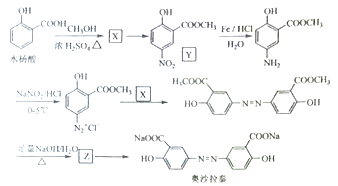
回答下列问题:
(1)X的结构简式为____;由水杨酸制备X的反应类型为_____。
(2)由X制备Y的反应试剂为_________。
(3)工业上常采用廉价的![]() ,与Z反应制备奥沙拉秦,通入的
,与Z反应制备奥沙拉秦,通入的![]() 与Z的物质的量之比至少应为____。
与Z的物质的量之比至少应为____。
(4)奥沙拉秦的分子式为______,其核磁共振氢谱为______组峰,峰面积比为______。
(5)若将奥沙拉秦用![]() 酸化后,分子中含氧官能团的名称为____。
酸化后,分子中含氧官能团的名称为____。
(6)W是水杨酸的同分异构体,可以发生银镜反应;W经碱催化水解后再酸化可以得到对苯二酚。W的结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g) =2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g) =2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g) =3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:__________。
(2)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO3—的原理如图所示。

①电源正极为____(填“A”或“B”),阴极的电极反应式为___________________________。
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为___g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com