
【题目】将E(g)和F(g)加入密闭容器中,在一定条件下发生反应:E(s)+4F(g)G(g),已知该反应的平衡常数如表所示。下列说法正确的是( )
温度/℃ | 25 | 80 | 230 |
平衡常数/(L3·mol-3) | 5×104 | 2 | 1.9×10-5 |
A.上述反应是熵增反应
B.25 ℃时,反应G(g)E(s)+4F(g)的平衡常数是0.5 mol3·L-3
C.在80 ℃时,测得某时刻,F、G的浓度均为0.5 mol·L-1,则此时v正>v逆
D.恒温恒容下,向容器中再充入少量G(g),达新平衡时,G的体积百分含量将增大
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.0.5molO3的质量为16.0g
B.2molH2SO4的摩尔质量为196gmol-1
C.NO的摩尔质量与相对分子质量相等
D.40gNaOH溶于水配成1L溶液,则c(NaOH)=1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”、“战略金属”。
(1)基态钛原子核外共有_______种运动状态不相同的电子,价电子排布式_______;与钛同周期的元素中,基态原子的未成对电子数与钛相同的有________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是_________。
(3)TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是_______;TiCl4稳定性比CCl4差,试从结构分析其原因:_______。
(4)钙钛矿材料是一类有着与钛酸钙相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。钛酸钙晶体结构如图所示。其中,A代表Ca2+,Ti原子位于由O原子构成的正八面体的中心,则钛酸钙的化学式为______,Ca2+的配位数是________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高能锂电池的总反应式为:2Li+FeS=Fe+Li2S[LiPF6SO(CH3)2为电解质],用该电池为电源进行如图的电解实验,电解一段时间测得甲池产生标准状况下H24.48L。下列有关叙述不正确的是
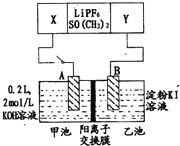
A.从隔膜中通过的离子数目为0.4NA
B.若电解过程体积变化忽略不计,则电解后甲池中溶液浓度为4mol/L
C.A电极为阳极
D.电源正极反应式为:FeS+2Li++2e-=Fe+Li2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.已知:HI(g)![]() 1/2H2(g)+1/2I2(s) △H =-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量
1/2H2(g)+1/2I2(s) △H =-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量
B.已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol,则氢气的燃烧热为ΔH=-285.8 kJ/mol
C.肼(N2H4)是一种用于火箭或燃料电池的原料,已知2H2O(g)+ O2(g)=2H2O2(l)△H=+108.3kJ/mol①N2H4(l) + O2(g)=N2(g) + 2H2O(g)△H=-534.0kJ/mol②。则有反应:N2H4(l) + 2H2O2(l) =N2(g)+ 4H2O(l)△H=-642.3kJ/mol
D.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l)ΔH=-57.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(Ⅰ)、(Ⅱ)反应在一定条件下焓变及平衡常数如下:
2H2(g)+S2(g)2H2S(g) ΔH1 K1 (Ⅰ)
3H2(g)+SO2(g)2H2O(g)+H2S(g) ΔH2 K2 (Ⅱ)
(1)用ΔH1、ΔH2表示反应4H2(g)+2SO2(g)=S2(g)+4H2O(g)的ΔH=________。
(2)回答下列反应(Ⅰ)的相关问题:
①温度为T1,在1 L恒容容器中加入1.8 mol H2、1.2 mol S2,10 min时反应达到平衡。测得10 min内v(H2S)=0.08 mol·L-1·min-1,则该条件下的平衡常数为________。
②温度为T2时(T2>T1),在1 L恒容容器中也加入1.8 mol H2、1.2 mol S2,建立平衡时测得S2的转化率为25%,据此判断ΔH1________0(填“>”或“<”),与T1时相比,平衡常数K1__(填“增大”“减小”或“不变”)。
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是________________(写出主要反应的离子方程式),该溶液中,c(Na+)______2c(SO32-)+c(HSO3-)(填“>”“<”或“=”)。
②在某NaHSO3、Na2SO3混合溶液中HSO3-、SO32-物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO32-的水解平衡常数=________。
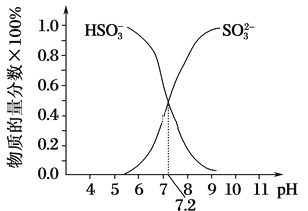
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001 mol·L1酸性KMnO4溶液滴定未知浓度的无色NaHSO3溶液。反应的离子方程式为2![]() +5
+5![]() +H+
+H+![]() 2Mn2++5
2Mn2++5![]() +3H2O。
+3H2O。
请完成下列问题:
(1)该滴定实验所需仪器和用品是____________。
A 酸式滴定管(50 mL)B 碱式滴定管(50 mL) C 量筒(10 mL) D 锥形瓶 E 铁架台 F 滴定管夹 G 烧杯 H 白纸 I 胶头滴管 J 漏斗
(2)实验中用_____(填“酸”或“碱”)式滴定管盛装酸性KMnO4溶液,原因是_______。
(3)本实验_______(填“需要”或“不需要”)使用指示剂,滴定终点的现象是__________。
(4)①滴定前平视液面,刻度为a mL,滴定后俯视刻度为b mL,则(ba) mL比实际消耗KMnO4溶液的体积_____(填“大”或“小”),根据(ba) mL计算得到的待测液浓度比实际浓度_____(填“高”或“低”)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测液浓度值会____(填“偏小”“偏大”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子化合物M的合成路线如下:
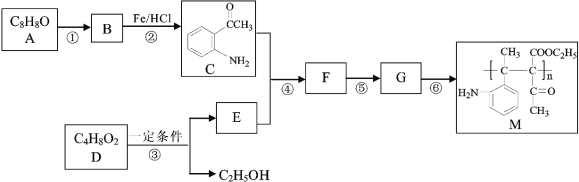
已知:![]()
(1)A中含氧官能团的名称是______。
(2)H是A的同分异构体,能与FeCl3显示特殊的紫色,核磁共振氢谱显示H有5组峰,则其结构简式为____________________。
(3) B的结构简式为______,G的结构简式为__________________。
(4) 已知D为乙酸乙酯,2 D → E + C2H5OH,F中含有醇羟基,⑤的反应类型为_____。
(5) 写出④的反应方程式___________________________________________。
(6) 以乙醛为原料,写出合成D的流程图______。(其他无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有黄绿色气体乙为Cl2,金属单质A、B和气体甲、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)
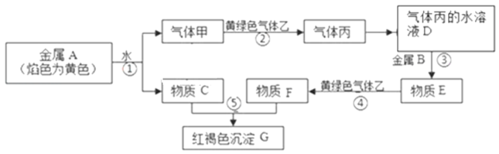
(1)丙的化学式为___;
(2)F溶液常用于腐蚀印刷电路板,请写出相关的离子方程式:___;
(3)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是___;
a.碘水 b.氯水 c.Na2SO3溶液 d.KSCN溶液
(4)C溶液中加入过量的Al2O3固体的离子反应方程式为___;向反应后的溶液中通入过量的CO2气体的离子反应方程式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com