
ΓΨΧβΡΩΓΩΡ≥Μ·―ß Β―ι–ΓΉιΒΡΆ§―ßΈΣΧΫΨΩΚΆ±»ΫœSO2ΚΆ¬»Υ°ΒΡΤ·ΑΉ–‘Θ§…ηΦΤΝΥ»γœ¬ΒΡ Β―ιΉΑ÷ΟΓΘ
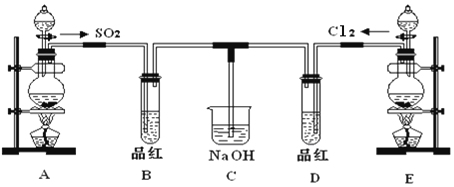
Θ®1Θ© Β―ι “”ΟΉΑ÷ΟA÷Τ±ΗSO2ΓΘΡ≥Ά§―ß‘Ύ Β―ι ±ΖΔœ÷¥ρΩΣAΒΡΖ÷“Κ¬©ΕΖΜν»ϊΚσΘ§¬©ΕΖ÷–“ΚΧεΈ¥Νςœ¬Θ§Ρψ»œΈΣ‘≠“ρΩ…Ρή «__________________ΓΘ
Θ®2Θ© Β―ι “”ΟΉΑ÷ΟE÷Τ±ΗCl2Θ§ΤδΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ__________________________ΘΜ»τ”–8molΒΡHCl≤ΈΦ”Ζ¥”ΠΘ§‘ρΉΣ“ΤΒΡΒγΉ”Ήή ΐΈΣ________ΓΘ
Θ®3Θ©ΗΟΉΑ÷Ο÷–«β―θΜ·ΡΤ»ή“ΚΒΡΉς”Ο «___________________ΓΘ
Θ®4Θ©Ά®ΤχΚσBΓΔDΝΫΗω ‘Ιή÷–ΒΡœ÷œσ______________ΓΘΆΘ÷ΙΆ®ΤχΚσΘ§‘ΌΗχBΓΔDΝΫΗω ‘ΙήΖ÷±πΦ”»»Θ§ΝΫΗω ‘Ιή÷–ΒΡœ÷œσΖ÷±πΈΣBΘΚ________Θ§DΘΚ________ΓΘ
Θ®5Θ©Νμ“ΜΗω Β―ι–ΓΉιΒΡΆ§―ß»œΈΣSO2ΚΆ¬»Υ°ΕΦ”–Τ·ΑΉ–‘Θ§Εΰ’ΏΜλΚœΚσΒΡΤ·ΑΉ–‘ΩœΕ®ΜαΗϋ«ΩΓΘΥϊΟ«ΫΪ÷ΤΒΟΒΡSO2ΚΆCl2Α¥1ΘΚ1Ά§ ±Ά®»κΒΫΤΖΚλ»ή“Κ÷–Θ§ΫαΙϊΖΔœ÷Ά …Ϊ–ßΙϊ≤Δ≤ΜœώœκœσΒΡΡ«―υΓΘ«κΡψΖ÷ΈωΗΟœ÷œσΒΡ‘≠“ρΘ®”ΟΜ·―ßΖΫ≥Χ Ϋ±μ ΨΘ©____________________ΓΘ
ΓΨ¥πΑΗΓΩΖ÷“Κ¬©ΕΖΜν»ϊΈ¥¥ρΩΣMnO2+4HCl(≈®)![]() MnCl2+2H2O+Cl2Γϋ4NAΈ≤Τχ¥ΠάμΆ …Ϊ±δΈΣΚλ…ΪΈό±δΜ·SO2+Cl2+2H2OΘΫ2HCl+H2SO4
MnCl2+2H2O+Cl2Γϋ4NAΈ≤Τχ¥ΠάμΆ …Ϊ±δΈΣΚλ…ΪΈό±δΜ·SO2+Cl2+2H2OΘΫ2HCl+H2SO4
ΓΨΫβΈωΓΩ
ΉΑ÷ΟA…ζ≥…ΒΡΕΰ―θΜ·ΝρΤχΧεΆ®ΙΐΉΑ÷ΟB÷–ΒΡΤΖΚλ»ή“ΚΘ§Εΰ―θΜ·ΝρΨΏ”–Τ·ΑΉ–‘Θ§Ω…“‘ Ι»ή“ΚΆ …ΪΘ§Ά …ΪΚσΒΡ»ή“ΚΦ”»» ±”÷Μ÷Η¥‘≠ά¥ΒΡΚλ…ΪΓΘ¬»ΤχΚΆΥ°Ζ¥”Π…ζ≥…ΒΡ¥Έ¬»ΥαΨΏ”–Τ·ΑΉ–‘Θ§“ρΕχ¬»ΤχΆ®»κΤΖΚλ»ή“Κ÷–“≤Ρή ΙΤΖΚλΆ …ΪΘ§¥Έ¬»ΥαΒΡΤ·ΑΉ≤ΜΩ…ΡφΘ§Φ”»» ±Θ§≤ΜΡήΜ÷Η¥Κλ…ΪΘ§ Θ”ύΕΰ―θΜ·ΝρΚΆ¬»ΤχΆ®ΙΐΉΑ÷ΟCΈϋ ’Θ§Ζά÷ΙΈέ»ΨΩ’ΤχΘ§Ψί¥Υ≈–ΕœΓΘ
Θ®1Θ©»ϊΉ”ΟΜ”–»Γœ¬ά¥Θ§¥ρΩΣΜν»ϊ ±Θ§Ω’ΤχΈόΖ®Ϋχ»κΖ÷“Κ¬©ΕΖΡΎ≤ΩΘ§‘λ≥…Ζ÷“Κ¬©ΕΖΡΎΒΡ―Ι«Ω–Γ”Ύ¥σΤχ―Ι«ΩΘ§“ΚΧεΈόΖ®Νς≥ωΘΜ
Θ®2Θ© Β―ι “÷Τ±Η¬»ΤχΒΡΖ¥”ΠΖΫ≥Χ ΫΈΣMnO2+4HCl(≈®)![]() MnCl2+2H2O+Cl2ΓϋΘ§Ζ¥”Π÷–ΟΩ”–4mol HCl≤Έ”κΖ¥”ΠΘ§±Μ―θΜ·ΒΡ¬»Μ·«β «2molΘ§2molHCl±Μ―θΜ·ΒγΉ”ΉΣ“ΤΈΣ2molΘ§»τ”–8molΒΡHCl≤ΈΦ”Ζ¥”ΠΘ§‘ρΉΣ“ΤΒΡΒγΉ”Ήή ΐΈΣ4NAΘΜ
MnCl2+2H2O+Cl2ΓϋΘ§Ζ¥”Π÷–ΟΩ”–4mol HCl≤Έ”κΖ¥”ΠΘ§±Μ―θΜ·ΒΡ¬»Μ·«β «2molΘ§2molHCl±Μ―θΜ·ΒγΉ”ΉΣ“ΤΈΣ2molΘ§»τ”–8molΒΡHCl≤ΈΦ”Ζ¥”ΠΘ§‘ρΉΣ“ΤΒΡΒγΉ”Ήή ΐΈΣ4NAΘΜ
Θ®3Θ©Εΰ―θΜ·ΝρΚΆ¬»ΤχΨυ «”–ΕΨΤχΧεΘ§–η“ΣΈ≤Τχ¥ΠάμΘ§Υυ“‘ΉΑ÷Ο÷–«β―θΜ·ΡΤ»ή“ΚΒΡΉς”Ο «Έ≤Τχ¥ΠάμΘ§Ζά÷ΙΈέ»ΨΩ’ΤχΘΜ
Θ®4Θ©SO2ΨΏ”–Τ·ΑΉ–‘Θ§Εΰ―θΜ·ΝρΆ®»κΤΖΚλ»ή“Κ÷–Θ§ΤΖΚλΆ …ΪΘΜSO2ΒΡΤ·ΑΉΨΏ”–Ω…Ρφ–‘Θ§Ά …ΪΚσΒΡ»ή“ΚΦ”»» ±”÷Μ÷Η¥‘≠ά¥ΒΡΚλ…ΪΓΘ¬»ΤχΚΆΥ°Ζ¥”Π…ζ≥…ΒΡ¥Έ¬»ΥαΨΏ”–Τ·ΑΉ–‘Θ§“ρΕχ¬»ΤχΆ®»κΤΖΚλ»ή“Κ÷–“≤Ρή ΙΤΖΚλΆ …ΪΘ§¥Έ¬»ΥαΒΡΤ·ΑΉ≤ΜΩ…ΡφΘ§Φ”»» ±Θ§≤ΜΡήΜ÷Η¥Κλ…ΪΘΜ
Θ®5Θ©¬»ΤχΨΏ”–Ϋœ«ΩΒΡ―θΜ·–‘Θ§Εΰ―θΜ·ΝρΨΏ”–Ϋœ«ΩΒΡΜΙ‘≠–‘Θ§‘ΎΥ°»ή“Κ÷–ΝΫ’Ώ1ΘΚ1ΖΔ…ζΖ¥”ΠSO2+Cl2+2H2OΘΫ2HCl+H2SO4Θ§…ζ≥…ΈοΕΦΈόΤ·ΑΉ–‘Θ§“ρΕχSO2ΚΆCl2Α¥1ΘΚ1Ά§ ±Ά®»κΒΫΤΖΚλ»ή“Κ ±Θ§ΤΖΚλ»ή“Κ≤Δ≤ΜΆ …ΪΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ―θΜ·ΜΙ‘≠ΒΈΕ® Β―ι”κ÷–ΚΆΒΈΕ® Β―ιάύΥΤΘ§œ÷”Ο0.1000mol/LΒΡΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΒΈΕ®Έ¥
÷Σ≈®Ε»ΒΡΈό…Ϊ―«ΝρΥα«βΡΤ»ή“ΚΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©ΒΈΕ®«Α»σœ¥ΒΈΕ®ΙήΒΡ≤ΌΉςΖΫΖ®__________ΓΘ
Θ®2Θ©Ρ≥Ά§―ß≤βΒΟΒΡ Β―ι ΐΨί»γœ¬±μ
1 | 2 | 3 | 4 | |
―«ΝρΥα«βΡΤ»ή“ΚΧεΜΐmL | 25.00 | 25.00 | 25.00 | 25.00 |
ΒΈΕ®Ιή≥θΧεΜΐmL | 0.00 | 1.02 | 1.00 | 0.80 |
ΒΈΕ®ΙήΡ©ΧεΜΐmL | 40.02 | 41.00 | 41.00 | 42.90 |
«σ¥ΐ≤β“Κ―«ΝρΥα«βΡΤΒΡΈο÷ ΒΡΝΩ≈®Ε»________ΓΘ
Θ®3Θ©ΒΈΕ®«ΑΤΫ ”ΗΏΟΧΥαΦΊ“ΚΟφΘ§¥οΒΈΕ®÷’ΒψΚσ―ω ”“ΚΟφΘ§‘ρΦΤΥψ÷Β±» ΒΦ ÷Β___Θ®ΧνΓΑΤΪΗΏΓ±ΜρΓΑΤΪΒΆΓ±ΜρΓΑ≤Μ±δΓ±Θ© ΓΘ
Θ®4Θ©≥ΘΈ¬œ¬0.1000mol/L―«ΝρΥα»ή“Κ÷–H2SO3 HSO3- SO32-»ΐ’ΏΥυ’ΦΈο÷ ΒΡΝΩΖ÷ ΐ(a)ΥφpH±δΜ·ΒΡΙΊœΒ»γΆΦΥυ ΨΘ§“―÷Σlg2=0.3Θ§‘ρ‘≠―«ΝρΥα«βΡΤ»ή“ΚΒΡpH=_______ΘΚ
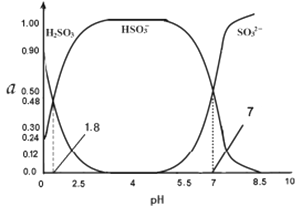
Θ®5Θ©»Γ…œ ω―«ΝρΥα«βΡΤ»ή“Κ1LΘ§œ»Φ”»κ«β―θΜ·ΡΤΙΧΧεΘ§ Ι»ή“ΚΒΡpH=10Θ§Θ®ΦΌΕ®Φ”ΙΧΧεΚσ»ή“ΚΒΡΧεΜΐ≤Μ±δΘ©Θ§‘ρΗΟ»ή“ΚΡή»ήΫβΝρΥα±ΒΒΡΈο÷ ΒΡΝΩn=______Θ®“―÷ΣΗΟΈ¬Ε» ±KSpΘ®BaSO4Θ©=1.0ΓΝ10-10 KSp(BaSO3Θ©=1.0ΓΝ10-8 Θ©ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
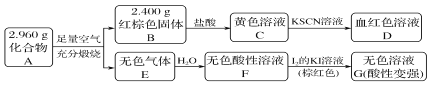
ΓΨΧβΡΩΓΩ¥≈–‘≤ΡΝœA «”…ΝΫ÷÷‘ΣΥΊΉι≥…ΒΡΜ·ΚœΈοΘ§Ρ≥―–ΨΩ–ΓΉιΑ¥»γΆΦΝς≥ΧΧΫΨΩΤδΉι≥…ΘΚ
«κΜΊ¥πΘΚ
Θ®1Θ©AΒΡΉι≥…‘ΣΥΊΈΣ________(”Ο‘ΣΥΊΖϊΚ≈±μ Ψ)Θ§Μ·―ß ΫΈΣ_____________________ΓΘ
Θ®2Θ©»ή“ΚCΩ…»ήΫβΆ≠Τ§Θ§άΐΨΌΗΟΖ¥”ΠΒΡ“ΜΗω ΒΦ ”Π”Ο________ΓΘ
Θ®3Θ©“―÷ΣΜ·ΚœΈοAΡή”κœΓΝρΥαΖ¥”ΠΘ§…ζ≥…“Μ÷÷Β≠ΜΤ…Ϊ≤Μ»ήΈοΚΆ“Μ÷÷ΤχΧε(±ξΩωœ¬ΒΡΟήΕ»ΈΣ1.518 gΓΛLΘ≠1)Θ§ΗΟΤχΧεΖ÷Ή”ΒΡΒγΉ” ΫΈΣ________ΓΘ–¥≥ωΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ____________________ΓΘ
–¥≥ωFΓζGΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ___________________________________ΓΘ
…ηΦΤ Β―ιΖΫΑΗΧΫΨΩ»ή“ΚG÷–ΒΡ÷ς“ΣΈΔΝΘ(≤ΜΩΦ¬«H2OΓΔHΘΪΓΔKΘΪΓΔIΘ≠) _____________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©”Ο0.lmolΓΛL-1NaOH»ή“ΚΖ÷±πΒΈΕ®ΧεΜΐΨυΈΣ20.00mLΓΔ≈®Ε»ΨυΈΣ0.1molΓΛL-1ΒΡ―ΈΥαΚΆ¥ΉΥα»ή“ΚΘ§ΒΟΒΫΒΈΕ®Ιΐ≥Χ÷–»ή“ΚpHΥφΦ”»κNaOH»ή“ΚΧεΜΐΕχ±δΜ·ΒΡΝΫΧθΒΈΕ®«ζœΏΓΘ
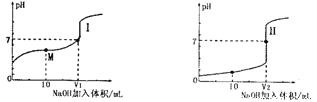
ΔΌΒΈΕ®¥ΉΥαΒΡ«ζœΏ «__________(ΧνΓΑIΓ±ΜρΓΑΔρΓ±)ΓΘ
ΔΎV1ΚΆV2ΒΡΙΊœΒΘΚV1______V2(ΧνΓΑ>Γ±ΓΔΓΑ=Γ±ΜρΓΑ<Γ±)
ΔέMΒψΕ‘”ΠΒΡ»ή“Κ÷–Θ§ΗςάκΉ”ΒΡΈο÷ ΒΡΝΩ≈®Ε»”…¥σΒΫ–ΓΒΡΥ≥–ρ «_______________ΓΘ
Θ®2Θ©ΈΣΝΥ―–ΨΩ≥ΝΒμ»ήΫβΤΫΚβΚΆ≥ΝΒμΉΣΜ·Θ§Ρ≥Ά§―ß≤ι‘ΡΉ Νœ≤Δ…ηΦΤ»γœ¬ Β―ιΓΘΉ ΝœΘΚAgSCN «ΑΉ…Ϊ≥ΝΒμ
≤ΌΉς≤Ϋ÷η | œ÷œσ |
≤Ϋ÷η1ΘΚœρ2mL0.005molΓΛL-1AgNO3»ή“Κ÷– Φ”»κ2mL0.005molΓΛL-1KSCN»ή“ΚΘ§Ψ≤÷Ο | ≥ωœ÷ΑΉ…Ϊ≥ΝΒμ |
≤Ϋ÷η2ΘΚ»ΓlmL…œ≤ψ«ε“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”1 ΒΈ2 molΓΛL-1Fe(NO3)3»ή“Κ | »ή“Κ±δΚλ…Ϊ |
≤Ϋ÷η3ΘΚœρ≤Ϋ÷η2ΒΡ»ή“Κ÷–Θ§ΦΧ–χΦ”»κ5ΒΈ3molΓΛL-1 AgNO3»ή“Κ | ≥ωœ÷ΑΉ…Ϊ≥ΝΒμΘ§»ή“ΚΚλ…Ϊ±δ«≥ |
≤Ϋ÷η4ΘΚœρ≤Ϋ÷η1”ύœ¬ΒΡΉ«“Κ÷–Φ”»κ5ΒΈ3 molΓΛL-1 KI»ή“Κ | ≥ωœ÷ΜΤ…Ϊ≥ΝΒμ |
ΔΌ–¥≥ω≤Ϋ÷η2÷–»ή“Κ±δΚλ…ΪΒΡάκΉ”ΖΫ≥Χ Ϋ______________________ΓΘ
ΔΎ”ΟΜ·―ßΤΫΚβ‘≠άμΫβ Ά≤Ϋ÷η3ΒΡ Β―ιœ÷œσ______________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A.”≤÷§ΥαΗ ”ΆθΞ τ”ΎΗΏΦΕ÷§ΖΨΥαΗ ”ΆθΞΘ§ «Χλ»ΜΗΏΖ÷Ή”Μ·ΚœΈο
B.Κ§ΒμΖέΜρœΥΈ§ΥΊΒΡΈο÷ Ω…“‘÷Τ‘λΨΤΨΪ
C.ΦΠΒΑ«εΒΡ»ή“Κ÷–Φ”»κΝρΥαΆ≠»ή“ΚΘ§ΦΠΒΑ«εΡΐΨέΘ§ΒΑΑΉ÷ ±δ–‘
D.≤ΜΆ§÷÷άύΒΡΑ±ΜυΥαΡή“‘≤ΜΆ§ΒΡ ΐΡΩΚΆΥ≥–ρ±Υ¥ΥΫαΚœΘ§–Έ≥…ΗϋΗ¥‘”ΒΡΕύκΡΜ·ΚœΈο
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΗΏΧζΥαΦΊ(K2FeO4) «“Μ÷÷”≈ΝΦΒΡΥ°¥ΠάμΦΝΓΘ25ΓφΘ§ΤδΥ°»ή“Κ÷–Φ”ΥαΜρΦνΗΡ±δ»ή“ΚΒΡpH ±Θ§Κ§ΧζΝΘΉ”ΒΡΈο÷ ΒΡΝΩΖ÷ ΐΠΡ(X)ΥφpHΒΡ±δΜ·»γΆΦΥυ Ψ[“―÷ΣΠΡ(X)=  ]ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
]ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «

A. K2FeO4ΓΔH2FeO4ΕΦ τ”Ύ«ΩΒγΫβ÷
B. 25ΓφΘ§H2FeO4+H+![]() H3FeO4+ΒΡΤΫΚβ≥Θ ΐK>100
H3FeO4+ΒΡΤΫΚβ≥Θ ΐK>100
C. ”…BΒψ ΐΨίΩ…÷ΣΘ§H2FeO4ΒΡΒΎ“Μ≤ΫΒγάκ≥Θ ΐKa1=4.15ΓΝ10-4
D. A.C ΝΫΒψΕ‘”Π»ή“Κ÷–Υ°ΒΡΒγάκ≥ΧΕ»: C
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩA,B,C,DΨυΈΣΤχΧεΘ§‘Ύ2AΘΪB![]() 3CΘΪ5DΖ¥”Π÷–Θ§±μ ΨΗΟΖ¥”ΠΥΌ¬ ΉνΩλΒΡ «
3CΘΪ5DΖ¥”Π÷–Θ§±μ ΨΗΟΖ¥”ΠΥΌ¬ ΉνΩλΒΡ «
A. Π‘(A)ΘΫ 0.5 molΘ·(LΓΛΘσ) B. Π‘(C)ΘΫ 0.8 molΘ·(LΓΛΘσ)
C. Π‘(B)ΘΫ 0.3 molΘ·(LΓΛΘσ) D. Π‘(D)ΘΫ 1 molΘ·(LΓΛΘσ)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈΣ≤βΕ®Cl2ΓΔBr2ΒΡ―θΜ·–‘«Ω»θΘ§…ηΦΤΝΥ»γœ¬ Β―ιΘΚ(Ω…Ι©―Γ‘ώΒΡ ‘ΦΝ”–ΘΚ¬»Υ°ΓΔδεΥ°ΓΔNaCl»ή“ΚΓΔNaBr»ή“ΚΓΔΨΤΨΪΓΔΥΡ¬»Μ·ΧΦ)ΓΘ Β―ι≤Ϋ÷η»γœ¬ΆΦΘ§Χν–¥ΆΦ÷–ΒΡΩ’ΑΉΓΘ
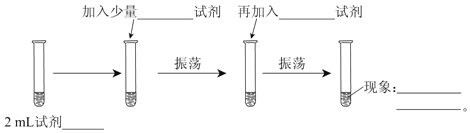
Θ®1Θ©2 mL ‘ΦΝ_______________ΘΜ
Θ®2Θ©Φ”»κ…ΌΝΩ___________ ‘ΦΝΘΜ
Θ®3Θ©‘ΌΦ”»κ___________ ‘ΦΝΘΜ
Θ®4Θ©œ÷œσ_____________________________________________________ΓΘ
Θ®5Θ©Ω…“‘÷ΛΟςCl2ΒΡ―θΜ·–‘____________(Χν«Ω”ΎΓΔ»θ”Ύ)Br2ΒΡ―θΜ·–‘ΓΘ
Θ®6Θ©ΖΔ…ζΖ¥”ΠΒΡάκΉ”Ζ¥”ΠΖΫ≥Χ ΫΈΣ_______________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ΘΈ¬œ¬Θ§œ¬Ν–”–ΙΊάκΉ”≈®Ε»ΦΑpH¥σ–ΓΒΡ±»ΫœΘ§’ΐ»ΖΒΡ «Θ® Θ©
A. NH4+≈®Ε»œύΆ§ΒΡœ¬Ν–»ή“ΚΘΚΔΌ(NH4)2Fe(SO4)2 ΔΎ(NH4)2CO3 Δέ(NH4)2SO4Θ§»ή“Κ≈®Ε»”…¥σΒΫ–ΓΒΡΥ≥–ρ «ΘΚΔέΘΨΔΎΘΨΔΌ
B. ”…pHΘΫ3ΒΡCH3COOH»ή“Κ”κpHΘΫ11ΒΡNaOH»ή“ΚΒ»ΧεΜΐΜλΚœΘ§ΤδάκΉ”≈®Ε»≤ΜΩ…Ρή «ΘΚc(CH3COO-)ΘΨc(Na+)ΘΨc(H+)ΘΨc(OH-)
C. pHΘΫ13ΒΡBa(OH)2»ή“Κ”κpHΘΫ1ΒΡHCl»ή“ΚΒ»ΧεΜΐΜλΚœΚσΘ§ΜλΚœ»ή“ΚΒΡpHΘΨ7
D. pHΘΫ12ΒΡBa(OH)2»ή“Κ”κpHΘΫ14ΒΡNaOH»ή“ΚΒ»ΧεΜΐΜλΚœΘ§ΜλΚœ»ή“ΚΒΡpHΖΕΈß «13ΘΦpHΘΦ14
ΓΨ¥πΑΗΓΩD
ΓΨΫβΈωΓΩΔΌ(NH4)2Fe(SO4)2»ή“Κ÷–Fe2+ΒΡΥ°ΫβΕ‘”ΎοßΗυάκΉ”ΒΡΥ°ΫβΤπΒΫ“÷÷ΤΉς”ΟΘ§ ΔΎ(NH4)2CO3 ÷–ΧΦΥαΗυάκΉ”Υ°ΫβΕ‘”ΎοßΗυάκΉ”ΒΡΥ°ΫβΤπΒΫ¥ΌΫχΉς”ΟΘ§Δέ(NH4)2SO4»ή“Κ÷–ΝρΥαΗυάκΉ”Ε‘οßΗυάκΉ”ΒΡΥ°ΫβΈό”ΑœλΘ§Υυ“‘»ή“Κ÷–οßΗυάκΉ”ΒΡΥ°Ϋβ≥ΧΕ»ΒΡ¥σ–ΓΥ≥–ρΈΣΘΚΔΎΘΨΔέΘΨΔΌΓΘ‘ρ“Σ¥οΒΫœύΆ§ΒΡοßΗυάκΉ”≈®Ε»Θ§Υ°Ϋβ≥ΧΕ»¥σΒΡ»ή“ΚΘ§Έο÷ ΒΡ≈®Ε»”ΠΗΟ‘Ϋ¥σΘ§Φ¥»ή“Κ≈®Ε»”…¥σΒΫ–ΓΒΡΥ≥–ρ «ΘΚΔΎΘΨΔέΘΨΔΌΓΘ―ΓœνA¥μΈσΓΘ”…pHΘΫ3ΒΡCH3COOH»ή“Κ”κpHΘΫ11ΒΡNaOH»ή“ΚΒ»ΧεΜΐΜλΚœΘ§”…”Ύ¥ΉΥαΒΡ≈®Ε»‘Ε¥σ”Ύ«β―θΜ·ΡΤΒΡ≈®Ε»Θ§Υυ“‘÷–ΚΆ“‘ΚσΒΟΒΫ¥ΉΥαΡΤΘ®Ϋœ…ΌΘ©ΚΆ¥ΉΥαΘ®ΫœΕύΘ©ΒΡΜλΚœ»ή“ΚΘ§»ή“Κœ‘Υα–‘Θ§Φ¥c(H+)ΘΨc(OH-)Θ§ΗυΨίΒγΚ… ΊΚψΒΟΒΫΘΚc(CH3COO-)ΘΨc(Na+)ΓΘ”÷“ρΈΣΡΤάκΉ” «¥ΉΥαΡΤΆξ»ΪΒγάκ…ζ≥…ΒΡΘ§«βάκΉ” Ι¥ΉΥαΈΔ»θΒγάκΒΟΒΫΒΡΘ§Υυ“‘”–c(CH3COO-)ΘΨc(Na+)ΘΨc(H+)ΘΨc(OH-)ΓΘ―ΓœνB¥μΈσΓΘpHΘΫ13ΒΡBa(OH)2»ή“Κ”κpHΘΫ1ΒΡHCl»ή“ΚΒ»ΧεΜΐΜλΚœΘ§ΝΫ»ή“ΚΒΡ«β―θΗυάκΉ”ΚΆ«βάκΉ”ΒΡ≈®Ε»Η’ΚΟœύΒ»Θ§Β»ΧεΜΐΜλΚœΘ§«ΓΚΟ÷–ΚΆΘ§»ή“Κœ‘÷––‘ΓΘ―ΓœνC¥μΈσΓΘpHΘΫ12ΒΡBa(OH)2»ή“Κ”κpHΘΫ14ΒΡNaOH»ή“ΚΒ»ΧεΜΐΜλΚœΘ§Τδ![]() Θ§Υυ“‘
Θ§Υυ“‘![]() Θ§
Θ§ ![]() Θ§―ΓœνD’ΐ»ΖΓΘ
Θ§―ΓœνD’ΐ»ΖΓΘ
ΓΨΧβ–ΆΓΩΒΞ―ΓΧβ
ΓΨΫα χΓΩ
14
ΓΨΧβΡΩΓΩ “Έ¬œ¬Θ§œ¬Ν–»ή“Κ÷–ΝΘΉ”≈®Ε»ΙΊœΒ’ΐ»ΖΒΡ «Θ® Θ©
A. Na2C2O4»ή“ΚΘΚc(OH-)=c(H+)+c(HC2O4-)+c(H2C2O4)
B. 20mL0.1molL-1CH3COONa»ή“Κ”κ10mL0.1molL-1HCl»ή“ΚΜλΚœΚσ»ή“Κ≥ Υα–‘Θ§ΥυΒΟ»ή“Κ÷–ΘΚc(CH3COO-)ΘΨc(Cl-)ΘΨc(CH3COOH)ΘΨc(H+)
C. CH3COONaΚΆCaCl2ΜλΚœ»ή“ΚΘΚc(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
D. pH=2ΒΡ―ΈΥα”κpH=12ΒΡΑ±Υ°Β»ΧεΜΐΜλΚœΘ§ΥυΒΟ»ή“Κ÷–ΘΚc(Cl-)+c(H+)ΘΨc(NH4+)+c(OH-)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com