
【题目】下列说法能用平衡移动原理解释的是
A.在电解水实验中,加入硫酸钠可以提高电解效率
B.碳酸氢钠溶液与硫酸铝溶液混合有沉淀和气体生成
C.在一定温度下某容器内发生下列反应:I2(g)+H2(g) ![]() 2HI(g) △H<0,缩小容器的体积,混合气体颜色加深
2HI(g) △H<0,缩小容器的体积,混合气体颜色加深
D.在双氧水中加FeCl3溶液可使产生O2速率加快
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 连接仪器、________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______。装置A中试剂是_______。
③ 能说明碳的非金属性比硅强的实验现象是_________。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 | ____ | ____ |
写出其中SO2显示还原性生成沉淀的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在初始温度为500℃、容积恒定为10L的三个密闭容器中,如图充料发生反应:CO2 (g) +3H2 (g) ![]() CH30H(g)十H2 O (g)△H= -25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是
CH30H(g)十H2 O (g)△H= -25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是

A. 刚开始反应时速率:甲>乙
B. 平衡后反应放热;甲>乙
C. 500℃下该反应平衡常数:K =3×102
D. 若a≠0,则0.9<b<l
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是( )

A. b电极是阴极B. a电极与电源的正极相连
C. 电解过程中水是氧化剂D. b电极附近溶液的pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是________。
(2)烧杯间填满碎纸条的作用是________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________(填“偏大”、“偏小”或“无影响”)。
(4)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1 NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐酸浓度的作用是______,当室温低于10 ℃时进行实验,对实验结果会造成较大的误差,其原因是_____________。
(5)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求得的中和热________(填“相等”或“不相等”),简述理由: ______________。
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系mA(g)+nB(g)![]() pC(g)+qD(g);ΔH<0。有下列判断,其中正确的是( )
pC(g)+qD(g);ΔH<0。有下列判断,其中正确的是( )
A.若温度不变,将容器的体积增大为原来的两倍,此时A物质的浓度变为原来的0.48倍,则m+n>p+q
B.若平衡时A、B的转化率相等,说明反应开始时A、B的物的量之比为n:m
C.若温度不变而压强增大为原来的两倍,则达到新的平衡时平衡混合物的体积小于原体积的![]()
D.若平衡体系共有amol气体,再向其中加入bmolB,当达到新平衡时共有(a+b)mol气体,则m+n=p+q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种常见的短周期元素,可形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的离子和Z的离子具有相同的电子层结构,X离子比Y离子多一个电子层,试回答:
(1)X、Y、Z的单质的晶体分别属于_______晶体,________晶体,_____晶体
(2)Z2Y2的电子式为___________,Z2Y2溶于水的化学方程式为__________。
(3)XY3在标准状态下是针状晶体,它属于___________晶体,XY3的水溶液与Z2Y2反应可生成一种具有漂白性的氧化剂H2Y2,其化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如下图所示的转化关系:
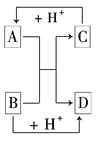
(1)如果A、B、C、D均是10电子的粒子,请写出:
A的结构式_____________;D的电子式____________;
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A与B在溶液中反应的离子方程式:____________________________________
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)________>________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六种短周期元素,aA、bB、cC、dD、eE、fF,已知原子序数大小关系是:a<e<c<b<f<d,且a+b=(c+d)/2;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻。
(1)B、C、D三种元素形成的六原子核的化合物和水反应的离子方程式是:_______________。
(2)A、C形成的四原子核化合物甲的电子式为_______,该化合物呈弱酸性,试写出这种化合物的电离方程式:_______________。
(3)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:__________________________________________________。
(4)写出A、C、D形成的六原子核化合物乙的水溶液和甲的水溶液反应的化学方程式:_______________________________________________________。
(5)写出E和F形成的化合物和化合物A2C反应的化学方程式:____________。
(6)A、E形成的四原子核化合物丙容易液化,其原因是:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com