
【题目】下列关系曲线不能正确反映其对应变化关系的是( )
A. 加热KClO3和MnO2固体混合物
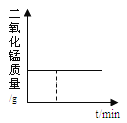
B. 向Ca(OH)2溶液中通入CO2至过量(碳酸钙遇到溶有二氧化碳的水,能生成可溶性碳酸氢钙)
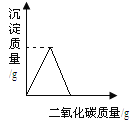
C. 向一定浓度的NaOH溶液中加水稀释
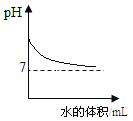
D. 将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al
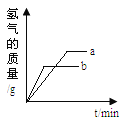
【答案】D
【解析】
A.加热KClO3和MnO2固体混合物过程中,由于二氧化锰作催化剂,质量始终不变,故A关系正确;B.氢氧化钙能和二氧化碳反应生成碳酸钙沉淀和水,碳酸钙和水、二氧化碳反应生成碳酸氢钙,反应的化学方程式及其质量关系为:Ca(OH)2+CO2═CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,由以上质量关系可知,反应过程中二氧化碳和碳酸钙的质量比都是44:100,因此图象关于y轴的一条平行线对称,故B关系正确;C.向一定浓度的NaOH溶液中加水稀释时,碱性减弱,pH减小,但是不能减小到7,故C关系正确;D.将等质量的Mg和Al分别与过量等浓度的盐酸反应时,由于镁比铝活泼,因此镁和稀盐酸反应需要时间短,并且最终铝和稀盐酸反应生成的氢气多,因此a为铝,b为镁,故D关系不正确。答案选D。


科目:高中化学 来源: 题型:
【题目】X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的化学式可表示为( )
A.XY
B.XY2
C.XY4
D.X2Y3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2 mol A与2 mol B混合于2 L的密闭容器中,发生反应:2A(g)+3B(g)![]() 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=0.2 mol·L-1·s-1
B.z=3
C.B的转化率为25%
D.C平衡时的浓度为0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 油脂都不能使溴水褪色
B. 氨基酸是两性化合物,能与酸、碱反应生成盐
C. 福尔马林可用作食品防腐剂
D. 蔗糖和麦芽糖的水解产物都是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L容积不变的容器中,发生N2+3H2 ![]() 2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是
2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是
A. 1.6 mol B. 2.8 mol
C. 3.2 mol D. 3.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4===2PbSO4+2H2O。
正极电极反应式为______________。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu===2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为_____________,当线路中转移0.2 mol电子时,则被腐蚀铜的质量为_____________g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为______________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的总反应化学方程式是:________________。
②电池工作一段时间后硫酸溶液的浓度_____________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝碱式碳酸盐MgaAlb(OH)c(CO3)d·xH2O是一种不溶于水的新型无机阻燃剂,其受热分解产物中的MgO、Al2O3熔点较高且都不燃烧,有阻燃作用。完成下列填空:
(1)组成镁铝碱式碳酸盐的三种非金属元素的原子半径从小到大的顺序是______________。碳原子最外层电子排布式是________________,铝原子核外有_________种能量不同的电子。
(2)将MgaAlb(OH)c (CO3)d·x H2O表示成氧化物的形式:2aMgO·bAl2O3·2dCO2·(________)H2O;
(3)焦炭与石英高温下在氮气流中发生如下反应,工业上可由此制得一种新型陶瓷材料氮化硅(Si3N4):3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g) + Q (Q>0)。
Si3N4(s)+6CO(g) + Q (Q>0)。
①该反应中,氧化产物是________________________。若测得反应生成4.48 L CO气体(标准状况下),则转移的电子的物质的量为_____________。
②该反应的平衡常数表达式K=_____________________________;若升高温度,K值____________(填“增大”、“减小”或“不变”)。
③该反应的速率与反应时间的关系如右图所示,t4时刻引起正逆反应速率变化的原因是___________________________(写出一种即可)。
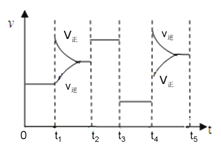
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验、反应物用量和反应停止的时间数据如下表:
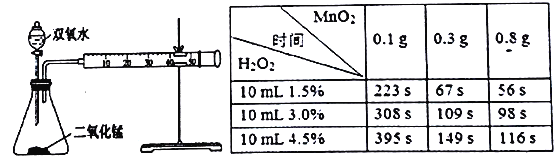
请回答下列问题:
(1)盛装双氧水的化学仪器名称是__________。
(2)如何检验该套装置的气密性__________。
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而___________。
(4)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入_______g的二氧化锰为较佳选择。
(5)某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越大,所需要的时间就越长,其反应速率越慢”的结论,你认为是否正确___________,理由是_________。(提示:H2O2的密度可认为近似相等)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com