
【题目】在密闭容器中的一定量混合气体发生反应:xA(g) +yB(g)![]() z C(g),平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍。再达平衡时,测得A的浓度为0.30 mol/L。下列有关判断正确的是( )
z C(g),平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍。再达平衡时,测得A的浓度为0.30 mol/L。下列有关判断正确的是( )
A.x+y < zB.平衡向正反应方向移动
C.C的体积分数下降D.B的转化率升高
【答案】C
【解析】
xA(g)+yB(g)zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,若平衡不移动,A的浓度为0.25mol/L,而再达平衡时,测得A的浓度为0.30mol/L,则说明体积增大(压强减小)平衡逆向移动,据此分析解答。
由信息可知,平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时测得A的浓度为0.30mol/L,体积增大,相当于压强减小,平衡逆向移动。
A.减小压强,平衡向气体体积增大的方向移动,说明逆反应方向为体积增大的方向,则x+y>z,故A错误;
B.由上述分析可知,平衡逆向移动,故B错误;
C.平衡逆向移动,C的体积分数减小,故C正确;
D.平衡逆向移动,B的转化率降低,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+H+-Mn2++CO2↑+H2O(未配平)
Ⅰ.甲同学研究外界因素对反应速率影响,设计如下实验方案:
用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
A | 2mL | 20 | |
B | 2mL | 20 | 10滴饱和MnSO4溶液 |
C | 2mL | 30 | |
D | 1mL | 20 | V1mL蒸馏水 |
E | 0.5mL | 20 | V2mL蒸馏水 |
(1)完成上述实验方案设计,其中:V1= ______ ,V2= ______ ;
(2)如果研究温度对化学反应速率的影响,使用实验 ______ 和 ______ .
(3)甲同学在做A组实验时,发现反应开始时速率较慢,随后加快.他分析认为高锰酸钾与 草酸溶液的反应放热,导致溶液温度升高,反应速率加快;从影响化学反应速率的因素看,你猜想还可能是 ______ ;
Ⅱ.乙同学利用如图测定反应速率

回答下列问题
(4)实验时要检查装置的气密性,简述操作的方法是 ______ ;
(5)乙同学通过生成相同体积的CO2来表示反应的速率,需要 ______ 仪来记录数据.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年,我国科学家屠呦呦因在青蒿素发现和治疗中的贡献,获得了诺贝尔生理学或医学奖。由植物黄花蒿叶中提取的青蒿素还可合成用于抗氯喹恶性疟及凶险型疟疾的蒿甲醚,其合成路线如下:
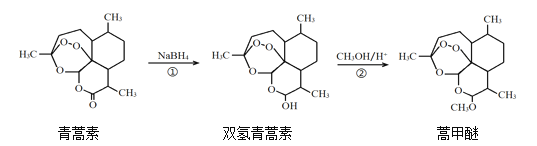
下列说法正确的是( )
A.青蒿素的分子式是C15H21O4
B.青蒿素在NaOH溶液中可以发生水解反应
C.反应②有H2O生成
D.反应①氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离出的c(H+)=l ×10-13 mol·L-1,下列说法正确的是
A.在该溶液中一定能同时大量存在Cu2+、NO3-、Cl-、Na+等离子
B.在该溶液中有可能同时大量存在K+、NO3-、HCO3-、Na+等离子
C.该溶液的pH可能为13,也可能为1
D.该溶液中 c(OH-)=l×10-1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行下列实验:

下列说法正确的是( )
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 乙针筒里的现象 |
A | H2S | CuSO4溶液 | 产生黑色沉淀 |
B | H2S | FeSO4溶液 | 产生黑色沉淀 |
C | SO2 | H2S | 出现淡黄色固体 |
D | SO2 | 紫色石蕊溶液 | 先变红后褪色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应2Ag+Cl2=2AgCl设计的一种原电池的装置如图。下列说法正确的是
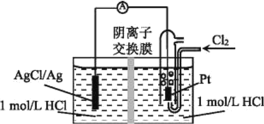
A.负极反应为Cl2+2e-=2Cl-
B.放电时,离子交换膜右侧溶液中有白色沉淀生成
C.理论上,可以用NaCl溶液代替盐酸
D.当电路中有0.01 mole-转移时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃能在臭氧作用下发生键的断裂,形成含氧衍生物:

 +R3COOH
+R3COOH
根据产物的结构可以推测原烯烃的结构.
(1)现有一化学式为C10H18的烃A,经过臭氧作用后可以得到 CH3COOH和B(结构简式如图).

A的结构简式是________________________
(2)A经氢化后得到的烷烃的命名是___________.
(3)烃A的一种同类别同分异构体,经过臭氧作用后,所有产物都不具有酸性.该同分异构体的结构简式是__________.
(4)以B为原料通过三步反应可制得化学式为(C6H10O2)n的聚合物,其路线如下:

写出该聚合物的结构简式:________________.
在进行第二步反应时,易生成一种含八元环的副产物,其结构简式为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,发生如下反应:4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)
完成下列填空:
(1)写出该反应的平衡常数表达式K=______。若只改变一个影响化学平衡的因素,则下列关于平衡常数K与化学平衡移动关系的叙述正确的是______(填序号)。
a.K值不变,平衡不移动
b.K值变化,平衡一定移动
c.平衡移动,K值可能不变
d.平衡移动,K值一定变化
(2)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是_____(填序号)。
a.υ正(NO2)=2υ正(NO)
b.NO和Cl2的物质的量之比不变
c.混合气体密度保持不变
d.c (NO2):c (NO):c (Cl2)=4:2:1
(3)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和适量NaCl固体,10min时反应达到平衡.测得10min内υ(NO2)=0.015mol/(Lmin),则平衡后n (Cl2)=______mol,此时NO2的转化率为а1;保持其它条件不变,扩大容器的体积,当反应再次达到平衡时NO2的转化率为а2,则а2_____а1(选填“>”、“<”或“=”)。
实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH→NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得到1L溶液A,溶液B为0.1mol/L的CH3COONa溶液。
(4)两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为________________。
(5)可使溶液A和溶液B的pH相等的方法是__________(填序号)。
a.向溶液A中加适量水
b.向溶液A中加适量NaOH
c.向溶液B中加适量水
d.向溶液B中加适量NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+I2(g)![]() 2HI(g)△H=-14.9kJ·mol-1。某温度下,在体积均为2.0L的甲、乙两个恒容密闭容器中充入反应物,其起始物质的量如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的是( )
2HI(g)△H=-14.9kJ·mol-1。某温度下,在体积均为2.0L的甲、乙两个恒容密闭容器中充入反应物,其起始物质的量如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的是( )
起始物质的量 | n(H2)/mol | n(I2)/mol | n(HI)/mol |
甲 | 0.02 | 0.02 | 0 |
乙 | 0.04 | 0.04 | 0 |
A. 平衡时,乙中H2的转化率是甲中的2倍
B. 平衡时,甲中混合物的颜色比乙中深
C. 平衡时,甲、乙中热量的变化值相等
D. 该温度下,反应的平衡常数K=0.25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com